Đề thi thử THPT Quốc gia năm 2017 môn Hóa học trường THPT Nguyễn Thị Minh Khai, Hà Tĩnh (Lần 1)
Đề thi thử THPT Quốc gia 2017 môn Hóa học
Mời các bạn tham khảo: Đề thi thử THPT Quốc gia năm 2017 môn Hóa học trường THPT Nguyễn Thị Minh Khai, Hà Tĩnh (Lần 1) để hệ thống lại kiến thức môn học và rèn luyện kỹ năng giải đề, quý thầy cô có thêm tài liệu phục vụ quá trình ôn tập cho học sinh cũng như tích lũy thêm kinh nghiệm ra đề thi.
Đề thi thử THPT Quốc gia năm 2017 môn Hóa học trường THPT chuyên Đại học Vinh (Lần 4)
Đề thi thử THPT Quốc gia năm 2017 môn Hóa học trường THPT Trung Giã, Hà Nội (Lần 2)
| SỞ GIÁO DỤC & ĐÀO TẠO HÀ TĨNH TRƯỜNG THPT N.T.MINH KHAI Đề thi có 4 trang |
ĐỀ THI THỬ THPT QUỐC GIA LẦN I Mã đề 001 |
Cho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; P = 31; S = 32; Cl = 35,5; K = 39; Fe = 56; Cu = 64; Ag = 108; Ba = 137.
Câu 1: Polietilen (PE) được điều chế bằng phản ứng trùng hợp monome nào sau đây?
A. CH2=CHCH3. B. CH2=CH2. C. CH2=CH-CH=CH2. D. C6H5CH=CH2.
Câu 2: Tính chất hóa học đặc trưng của kim loại là
A. tính dẻo. B. tính dẫn điện. C. tính oxi hóa. D. tính khử.
Câu 3: Công thức cấu tạo thu gọn của metyl axetat là
A. CH3COOCH3 B. CH3COOC2H5. C. CH3COOC2H3. D. HCOOCH3.
Câu 4: Để khử ion Cu2+ trong dung dịch CuSO4 có thể dùng kim loại
A. Fe. B. Ag. C. Au. D. Cu.
Câu 5: Để chứng minh tính lưỡng tính của NH2-CH2-COOH (X), ta cho X tác dụng với
A. HCl, NaOH. B. HNO3, CH3COOH. C. Na2CO3, HCl. D. NaOH, NH3.
Câu 6: Trong số các kim loại nhóm IIA, dãy các kim loại đều phản ứng với nước ở nhiệt độ thường tạo thành dung dịch kiềm là:
A. Mg, Ca, Ba. B. Be, Mg, Ba. C. Ca, Sr, Ba. D. Ca, Sr, Mg.
Câu 7: Tỉ lệ số người chết về bệnh phổi do hút thuốc lá gấp hàng chục lần số người không hút thuốc lá. Chất gây nghiện và gây ung thư có trong thuốc lá là
A. moocphin. B. nicotin. C. aspirin. D. cafein.
Câu 8: Kim loại Al không phản ứng với chất nào sau đây?
A. Dung dịch HCl. B. Dung dịch H2SO4 loãng.
C. Dung dịch NaOH. D. Dung dịch H2SO4 đặc nguội.
Câu 9: Chất nào sau đây không bị oxi hóa khi phản ứng với dung dịch HNO3 loãng?
A. Fe(OH)2. B. Fe2O3. C. FeO. D. Fe3O4
Câu 10: Trong điều kiện thường, chất ở trạng thái khí là
A. anilin. B. glyxin. C. metylamin. D. etanol.
Câu 11: Chất rắn không tan trong dung dịch NaOH là
A. Al2O3 B. Mg. C. Al. D. Al(OH)3
Câu 12: Thuỷ phân hoàn toàn 11,44 gam este no, đơn chức, mạch hở X với 100ml dung dịch NaOH 1,3M (vừa đủ) thu được 5,98 gam một ancol Y. Công thức cấu tạo của X là
A. CH3CH2COOCH3. B. HCOOC2H5. C. CH3COOC2H5. D. CH3COOCH3
Câu 13: Cho các nhận định sau:
(a) Kim loại Al có tính lưỡng tính vì Al tan được trong các dung dịch axit mạnh và kiềm.
(b) NaHCO3 là chất lưỡng tính.
(c) Công thức của phèn chua là: Na2SO4.Al2(SO4)3.24H2O.
(d) Al(OH)3 là hiđroxit lưỡng tính, trong đó tính bazơ trội hơn tính axit.
(e) Bột nhôm oxit và bột sắt (gọi là hỗn hợp tecmit) để thực hiện phản ứng nhiệt nhôm dùng hàn đường ray.
Số nhận định sai là
A. 1. B. 3. C. 4. D. 2.
Câu 14: Một cốc nước có chứa: 0,03 mol Na+, 0,02 mol Ca2+, 0,01 mol Mg2+, 0,06 mol HCO3- và 0,01 mol Cl-, 0,01 mol SO42-. Đun nóng cốc nước trên hồi lâu thì sẽ thu được
A. nước cứng tạm thời. B. nước mềm. C. nước cứng toàn phần. D. nước cứng vĩnh cửu.
Câu 15: Cho viên Zn nguyên chất vào hỗn hợp dung dịch gồm các ion Cu2+, Ni2+, Ag+, Pb2+, NO3- ở điều kiện thường đến dư Zn, thứ tự các ion kim loại lần lượt bị khử là:
A. Cu2+, Ni2+, Ag+, Pb2+. B. Cu2+, Ag+, Pb2+, Ni2+
C. Ag+, Cu2+, Ni2+, Pb2+ D. Ag+, Cu2+, Pb2+, Ni2+
Câu 16: Cho dãy các chất sau: Cu, Al, nước brom, FeCl3, HCl. Số chất trong dãy tác dụng được với dung dịch Fe(NO3)2 là
A. 3. B. 1. C. 2. D. 4.
Câu 17: Cho sơ đồ chuyển hóa
![]()
Các chất Y và T lần lượt là:
A. Fe và NaNO3. B. Fe2O3 và Cu(NO3)2.
C. Fe và AgNO3. D. Fe2O3 và AgNO3.
Câu 18: Cho các chuyển hóa sau:
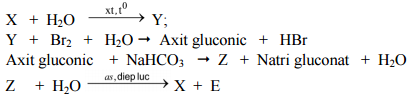
Các chất X, Y lần lượt là:
A. saccarozơ, glucozơ. B. tinh bột, glucozơ. C. xenlulozơ, glucozơ. D. tinh bột, fructozơ.
Câu 19: Cho hỗn hợp X gồm 2 kim loại Al, Fe. Nếu cho m gam X vào dung dịch HCl dư, sau phản ứng thu được 1,5V lit khí. Mặt khác, nếu cho m gam X vào dung dịch NaOH dư, sau phản ứng thu được V lit khí (biết thể tích khí đo ở cùng điều kiện) Phần trăm khối lượng Fe trong hỗn hợp X là
A. 75,68%. B. 39,13%. C. 60,87%. D. 59,09%.
Câu 20: Cho các polime sau: tơ nilon-6,6; poli(vinyl clorua); tơ nitron, cao su buna. Trong đó, số polime được điều chế bằng phản ứng trùng hợp là
A. 1. B. 2. C. 3. D. 4.
Câu 21: Đốt cháy hoàn toàn V lít hỗn hợp X gồm metylamin, đimetylamin bằng oxi vừa đủ được V1 lít hỗn hợp Y gồm khí và hơi. Dẫn toàn bộ Y qua bình H2SO4 đặc dư thấy thoát ra V2 lít hỗn hợp khí Z (các thể tích đo cùng điều kiện). Mối quan hệ giữa V, V1, V2 là
A. V = 2V2 - V1. B. 2V = V1 - V2. C. V = V1 - 2V2. D. V = V2 - V1.
Câu 22: Cho dãy các chất: H2NCH(CH3)COOH, anilin, CH3COOC2H5, CH3NH3Cl. Số chất trong dãy phản ứng với dung dịch KOH đun nóng là
A. 3. B. 2. C. 1. D. 4.
Câu 23: Dãy các kim loại đều có thể được điều chế bằng phương pháp điện phân dung dịch muối của chúng là:
A. Fe, Cu, Ag. B. Al, Fe, Cr. C. Mg, Zn, Cu. D. Ba, Ag, Au.
Câu 24: Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi ở bảng sau:
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
Z |
Quỳ tím |
Quỳ tím chuyển màu xanh |
|
X, Y |
Dung dịch AgNO3 trong NH3 đung nóng |
Kết tủa Ag trắng sáng |
|
Y |
Cu(OH)2 |
Dung dịch xanh lam |
|
T |
Nước brom |
Kết tủa trắng |
Các chất X, Y, Z, T lần lượt là
A. etyl fomat, fructozơ, anilin, phenol.
B. etyl axetat, glucozơ, etyl amin, anilin.
C. etyl axetat, glucozơ, etyl amin, alanin.
D. etyl fomat, glucozơ, etylamin, anilin.
Câu 25: Hòa tan hết 46,8 gam hỗn hợp X gồm FeS2 và CuS trong dung dịch có chứa a mol HNO3 (đặc nóng) thu được 104,16 lít NO2 (đo ở đktc, sản phẩm khử duy nhất của N+5) và dung dịch Y. Pha loãng Y bằng nước được dung dịch Z. Biết Z phản ứng tối đa với 7,68 gam Cu giải phóng khí NO (sản phẩm khử duy nhất) và Z tạo kết tủa trắng (không tan trong axit mạnh) khi thêm dung dịch BaCl2 vào. Giá trị của a là
A. 4,82. B. 4,62. C. 4,65. D. 4,68.
Câu 26: Đốt cháy hoàn toàn 22,9 gam hỗn hợ p X gồm hai este đơn chức, mạch hở tạo bởi cùng một ancol Y (My > 32) với hai axit cacboxylic kế tiếp nhau trong dãy đồng đẳng, thu đượ c 1,1 mol CO2 và 0,85 mol H2O. Mặt khác, toàn bộ lượng X trên phản ứng hết với 300 ml dung dịch NaOH 1 M thu đượ c dung dịch Y. Cô cạn dung dịch Y thu đượ c m g chất rắn khan. Giá trị của m là
A. 23,9. B. 20,4. C. 26,9. D. 19,0.
Câu 27: Cho m gam bột Al tan trong 200 ml dung dịch HNO3 3M thu được 0,04 mol NO; 0,03 mol N2O và dung dịch X (không có NH4NO3). Thêm 200 ml dung dịch NaOH 2M vào dung dịch X thu được kết tủa có khối lượng là
A. 9,36 gam. B. 2,43 gam. C. 2,34 gam. D. 6,76 gam.
Câu 28: Thủy phân hoàn toàn m gam hỗn hợp gồm peptit X và peptit Y bằng dung dịch NaOH thu được 151,2 gam hỗn hợp gồm các muối natri của Gly, Ala và Val. Mặt khác, để đốt cháy hoàn toàn m gam hỗn hợp X, Y ở trên cần 107,52 lít khí O2 (đktc) và thu được 64,8 gam H2O. Giá trị của m là
A. 102,4. B. 97,0. C. 92,5. D. 107,8.
Câu 29: Cho m gam Mg vào dung dịch chứa 0,1 mol AgNO3 và 0,25 mol Cu(NO3)2, sau một thời gian thu được 19,44 gam kết tủa và dung dịch X chứa 2 muối. Tách lấy kết tủa, thêm tiếp 8,4 gam bột sắt vào dung dịch X, sau khi các phản ứng hoàn toàn thu được 9,36 gam kết tủa. Giá trị của m là
A. 4,64. B. 4,8. C. 4,32. D. 5,28.
Câu 30: Điện phân dung dịch chứa CuSO4 và NaCl với điện cực trơ, cường độ dòng điện không đổi 2A, hiệu suất 100%. Kết quả thí nghiệm được ghi trong bảng sau:
|
Thời gian điện phân (giây) |
t |
t + 2895 |
2t |
|
Tổng số mol khi ở 2 điện cực |
a |
a + 0,03 |
2,125a |
|
Số mol Cu ở catot |
b |
b + 0,02 |
b + 0,02 |
Nếu dừng điện phân ở thời điểm 5404 giây rồi nhúng thanh sắt dư vào dung dịch, sau khi phản ứng hoàn toàn, khối lượng thanh sắt thay đổi như thế nào?
A. Tăng 0,032 gam. B. Giảm 0,256 gam. C. Giảm 0,56 gam D. Giảm 0,304 gam.
Câu 31: Cho rất từ từ 100 ml dung dịch hỗn hợp gồm Na2CO3 x (M) và NaHCO3 y (M) vào 100 ml dung dịch HCl 2 M thu được 2,688 lit CO2 (đktc). Nếu làm ngược lại thu được 2,24 lit CO2 (đktc). Giá trị x, y lần lượt là:
A. 1,5M và 1,5M. B. 1M và 0,5M. C. 0,5M và 1M. D. 1M và 2M.
Câu 32: Thủy phân hoàn toàn chất béo X trong môi trường axit thu được glixerol và hỗn hợp hai axit béo gồm axit oleic và axit linoleic. Đốt cháy hoàn toàn m gam X cần vừa đủ 2,385 mol O2, thu được 1,71 mol CO2. Mặt khác, m gam X phản ứng tối đa với V ml dung dịch Br2 2M. Giá trị của V là
A. 75. B. 90. C. 100. D. 60.
Câu 33: Thự c hiện các thí nghiệm sau:
(a) Đốt dây sắt dư trong khí clo.
(b) Đốt nóng hỗn hợp bột Fe và S (trong điều kiện không có oxi).
(c) Cho FeO vào dung dịch HNO3 (loãng dư).
(d) Cho Mg dư vào dung dịch Fe2(SO4)3.
(e) Cho Fe vào dung dịch H2SO4 (loãng, dư).
Có bao nhiêu thí nghiệm sau khi phản ứng hoàn toàn thu được muối sắt(II)?
A. 2. B. 3. C. 4. D. 1.
Câu 34: Tiến hành các thí nghiệm sau:
(a) Cho lá sắt vào dung dịch HCl có thêm vài giọt dung dịch CuSO4.
(b) Cho lá sắt vào dung dịch FeCl3.
(c) Cho lá thép vào dung dịch CuSO4.
(d) Cho lá sắt vào dung dịch CuSO4.
(e) Cho thanh Zn tiếp xúc với thanh Fe rồi nhúng vào dung dịch HCl.
Số thí nghiệm xảy ra ăn mòn điện hóa là
A. 5. B. 3. C. 4. D. 2.
Câu 35: Cho các phát biểu sau:
(a) Cho xenlulozơ vào ống nghiệm chứa nước Svayde, khuấy đều thấy xenlulozơ tan ra.
(b) Tơ visco, tơ axetat là tơ tổng hợp.
(c) Tơ nitron (hay olon) được dùng để dệt vải may quần áo ấm hoặc bện thành sợi "len" đan áo rét.
(d) Đun nóng tinh bột trong dung dịch axit vô cơ loãng sẽ thu được fructozơ.
(e) Trong phản ứng tráng gương, glucozơ đóng vai trò chất oxi hóa.
Số phát biểu đúng là
A. 3. B. 5. C. 4. D. 2.
Câu 36: Khi nhỏ từ từ đến dư dung dịch NaOH vào dung dịch hỗn hợp gồm x mol H2SO4 và y mol AlCl3, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
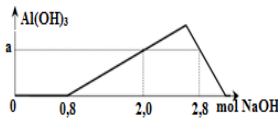
Tỉ lệ x : y và giá trị của a (mol) lần lượt là
A. 1 : 1 và 0,3. B. 4 : 3 và 0,3. C. 4 : 3 và 0,4. D. 2 : 3 và 0,4.
Câu 37: Cho 0,2 mol α-aminoaxit X có mạch cacbon không phân nhánh tác dụng với 100 ml dung dịch HCl 1 M thu được dung dịch A, dung dịch A tác dụng đủ với 250 ml dung dịch NaOH 2M thu được dung dịch B, cô cạn dung dịch B còn lại 41,25 gam chất rắn khan. Công thức cấu tạo của X là
A. CH3CH(NH2)COOH. B. HOOCCH2CH(NH2)COOH.
C. NH2CH2COOH. D. HOOCCH2CH2CH(NH2)COOH.
Câu 38: Chất A có công thức phân tử là C2H7O2N. Cho 7,7 gam A tác dụng với 200 ml dung dịch NaOH 1M thu được dung dịch X và khí Y (làm xanh quỳ ẩm), tỉ khối của Y so với H2 nhỏ hơn 10. Cô cạn dung dịch X thu được m gam chất rắn. Giá trị của m là
A. 10,70. B. 8,2. C. 12,20. D. 14,60.
Câu 39: Lên men m kg glucozơ chứa trong nước quả nho được 100 lít rượu vang 100. Biết hiệu suất phản ứng lên men đạt 95%, ancol etylic nguyên chất có khối lượng riêng là 0,8 g/ml. Giả thiết rằng trong nước quả nho chỉ có đường glucozơ. Giá trị của m gần nhất với giá trị nào sau đây?
A. 17,0. B. 17,5. C. 16,5. D. 15,0.
Câu 40: Hợp chất X có thành phần gồm C, H, O chứa vòng benzen. Cho 5,16 gam X vào 120 ml dung dịch NaOH 1 M (dư 20% so với lượng cần phản ứng) đến phản ứng hoàn toàn, thu được dung dịch Y. Cô cạn Y thu được m gam chất rắn khan. Mặt khác, đốt cháy hoàn toàn 5,16 gam X cần vừa đủ 6,272 lít O2 (đktc), thu được 12,32 gam CO2. Biết X có công thức phân tử trùng với công thức đơn giản nhất. Giá trị của m là
A. 8,88 B. 9,24. C. 8,08 D. 9,6
Đáp án đề thi thử THPT Quốc gia năm 2017 môn Hóa học
|
1, B 2, D 3, A 4, A 5, A 6, C 7, B 8, D 9, B 10, C |
11, B 12, C 13, B 14, B 15, D 16, A 17, C 18, B 19, C 20, C |
21, C 22, A 23, A 24, D 25, D 26, B 27, D 28, A 29, A 30, D |
31, B 32, D 33, A 34, C 35, D 36, D 37, B 38, C 39, C 40, A |