Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hải Phòng


Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hải Phòng được VnDoc tổng hợp. Đề thi gồm 40 câu hỏi trắc nghiệm nằm trong bài thi phân môn môn thi Hóa học, nội dung đề thi đảm bảo bám sát cấu trúc đề minh họa của bộ GD&ĐT đưa ra trước đó.
Hy vọng với Đề thi thử THPT quốc gia 2020 môn Hóa của các trường đưa ra sẽ giúp các em ôn luyện đề tốt hơn, chuẩn bị cho kì thi THPT quốc gia môn Hóa học.
Đề tải đề thi xin vui lòng kéo xuống ấn link tải về bên dưới
Đề thi thử THPT Quốc gia năm 2020 môn Hóa
1. Đáp án đề thi thử THPT Quốc gia 2020 môn Hóa Sở Hải Phòng
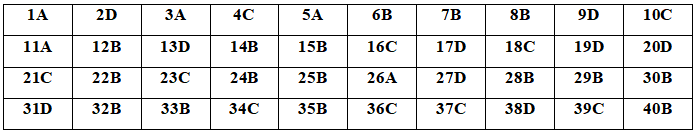
2. Hướng dẫn giải đề thi thử THPT Quốc gia 2020 môn Hóa Sở Hải Phòng
Câu 1. Este nào sau đây tác dụng với dung dịch NaOH thu được CH3COONa?
A. CH3COOC2H5.
B. HCOOC2H5.
C. C2H5COOCH3
D. HCOOCH3.
Hướng dẫn giải
CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
Câu 13. Thuỷ phân chất nào sau đây trong dung dịch NaOH, thu được glixerol và C17H35COONa?
A. (C17H31COO)2C2H4
B. (C17H35COO)2C2H4
C. (C17H31COO)3C3H5
D. (C17H35COO)3C3H5
Hướng dẫn giải
(C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3
Câu 19. Phát biểu nào sau đây sai?
A. Cho dung dịch Al2(SO4)3 tác dụng với dung dịch BaCl2 thu được kết tủa trắng.
B. Để bảo quản kim loại kiềm, người ta ngâm chúng trong dầu hoả.
C. Cho đinh sắt vào dung dịch H2SO4 loãng thì sắt bị ăn mòn hoá học.
D. Điện phân dung dịch CuSO4 với điện cực trợ thì ở anot thu được Cu.
Hướng dẫn giải
A. Đúng Ba2+ + SO42- → BaSO4
B. Đúng
C. Fe + H2SO4 → FeSO4 + H2
D. Sai: thu được Cu ở catot
Câu 21. Cho m gam glucozơ lên men thành 0,8 mol ancol etylic với hiệu suất 75%. Giá trị của m là
A. 72.
B. 54.
C. 96.
D. 102.
Hướng dẫn giải
C6H12O6 → 2C2H5OH + 2CO2
0,4 mol 0,8 mol
H = 75% => mC6H12O6 = 0,4 .180 : 75% = 96 gam
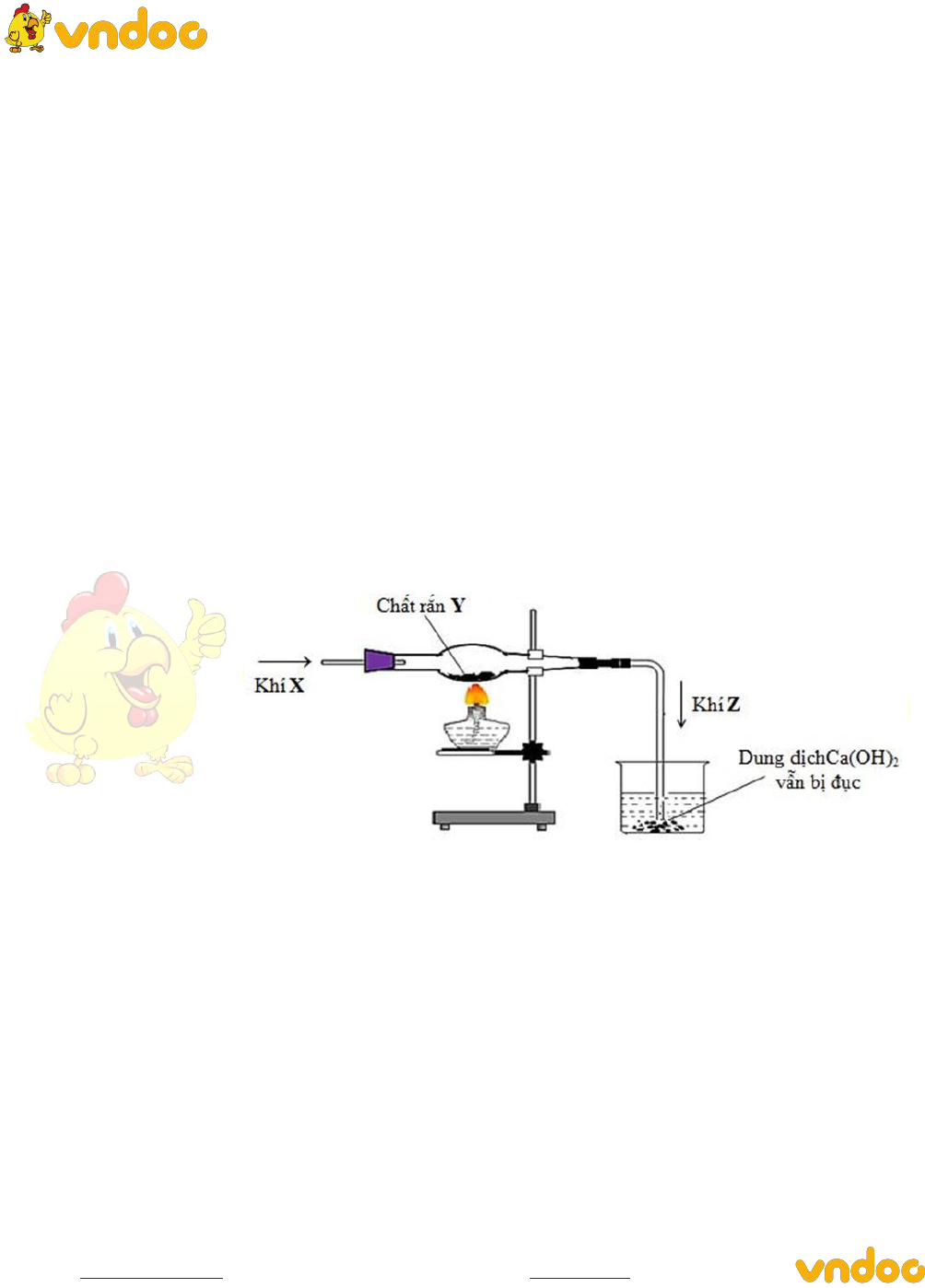
Câu 23. Thực hiện thí nghiệm như hình vẽ sau:
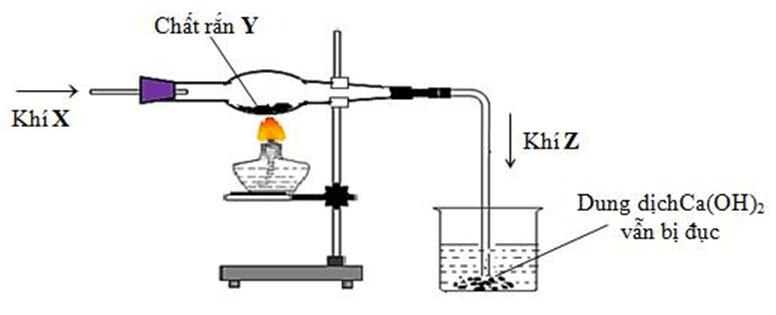
Khí X và chất rắn Y lần lượt là
A. H2 và CuO.
B. H2 và Al2O3.
C. CO và CuO.
D. CO và Al2O3.
Hướng dẫn giải
Câu 24. Cho 37,6 gam hỗn hợp gồm CaO, CuO và Fe2O3 tác dụng vừa đủ với 0,6 lít dung dịch HCl 2M. Cô cạn dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là
A. 61,0.
B. 70,6.
C. 49,3.
D. 80,2.
Hướng dẫn giải
mHCl = 1,2 mol => nH2O = 0,6 mol
BTKL : m oxit + mHCl = mmuối + mH2O => m muối = 70,6 gam
Câu 27. Cho 2,4 gam bột Mg tác dụng đủ với V ml dung dịch CuSO4 0,5M. Giá trị của V là
A. 100.
B. 400.
C. 300.
D. 200.
Hướng dẫn giải
nCuSO4 = nMg = 0,1 mol => V = 200 ml
Câu 28. Phản ứng nhiệt nhôm hoàn toàn 0,015 mol Fe3O4 cần khối lượng Al tham gia phản ứng là
A. 0,81 gam.
B. 1,08 gam.
C. 2,70 gam.
D. 0,54 gam.
Hướng ẫn giải
BTE: 3nAl = 8nFe3O4 => nAl = 0,04 => mAl = 1,08 gam
Câu 29. Cho 30,45 gam Gly-Ala-Gly tác dụng vừa hết với V ml dung dịch HCl 1M. Giá trị của V là
A. 200.
B. 450.
C. 300.
D. 100.
Hướng dẫn giải
nHCl = 3nGly-Ala-Gly = 0,45 mol => V = 450 ml
Câu 30. Chất nào sau đây không tạo kết tủa khi cho vào dung dịch Mg(HCO3)2?
A. K3PO4
B. HNO3
C. Ca(OH)2
D. Na2CO3.
Hướng dẫn giải
Câu 32. Cho các phát biểu sau:
a) Để xử lý nước thải có tính axit người ta thường dùng phèn chua.
b) Nhiệt phân hoàn toàn (NH4)2CO3 thu được ure.
c) Lưỡi cày bằng gang cắm trong ruộng ngập nước có xảy ra ăn mòn điện hóa.
d) Cho dung dịch FeCl2 vào dung dịch AgNO3 dư, thu được kết tủa gồm AgCl và Ag.
e) Cho a mol NaHSO4 vào dung dịch chứa a mol Ba(OH)2 thu được dung dịch chỉ chứa một chất tan.
Số phát biểu đúng là
A. 4.
B. 3.
C. 5.
D. 2.
Hướng dẫn giải
a) Sai: dùng Ca(OH)2
b) Sai: (NH4)2CO3 2NH3 + CO2 + 2H2O
c) Đúng: điện cực Fe-C
d) Đúng: FeCl2 + 3AgNO3 → Fe(NO3)3 + 2AgCl + Ag
e) Đúng : Ba(OH)2 + NaHSO4 → BaSO4 + NaOH + H2O
Câu 33. Cho 0,25 mol hỗn hợp E gồm hai este X (C9H10O2), Y (C3H6O2, không có phản ứng tráng bạc) tác dụng được tối đa với dung dịch chứa 0,3 mol NaOH, thu được dung dịch Z chứa m gam hỗn hợp muối. Giá trị của m là
A. 26,3.
B. 27,0.
C. 31,1.
D. 22,9.
Hướng dẫn giải
nNaOH > nE nên X là este củ a phenol. Y không tráng bạc nên có cấu tạo là CH3COOCH3
nE = nX + nY = 0, 25; nNaOH = 2nX + nY = 0,3 => nX = 0, 05; nY = 0, 2
nH2O = 0,05, nCH3OH = 0,2 mol
BTKL: mE + mNaOH = mH2O + mCH3OH + mmuối => mmuối = 27 gam
Câu 34. Thuỷ phân hoàn toàn triglixerit X trong dung dịch NaOH dư thu được 4,6 gam glixerol và m gam hỗn hợp hai muối natri stearat và natri oleat có tỉ lệ mol tương ứng là 1 : 2. Giá trị của m là
A. 45,9.
B. 45,8.
C. 45,7
D. 45,6.
Hướng dẫn giải
Muối natri stearat và natri oleat có tỉ lệ mol tương ứng là 1:2
=> X là (C17H35COO)(C17H33COO)2C3H5
nX = nC3H5(OH)3 = 0,05 mol => nC17H35COONa = 0,05 mol , nC17H33COONa = 0,1 mol
=> mmuối = 45,7 gam
Câu 35. Cho 0,1 mol hỗn hợp gồm CO2 và H2O qua than nung đỏ thu được 0,16 mol hỗn hợp khí X gồm CO, CO2, H2. Dẫn toàn bộ X qua dung dịch chứa hỗn hợp KHCO3 (x mol) và K2CO3 (y mol), thu được dung dịch Y chứa 12,76 gam chất tan, khí thoát ra còn CO và H2. Cô cạn Y, nung đến khối lượng không đổi thu được 9,66 gam rắn. Giá trị của x là
A. 0,05.
B. 0,02
C. 0,01.
D. 0,04
Hướng dẫn giải
nC = 0,16 - 0,1 = 0,06 mol
BT E: 4nC = 2nCO + 2nH2 => nCO + nH2 = 0,12 mol => nCO2 (X) = nX - (nCO + nH2) = 0,04 mol
Y chứa KHCO3 (a) và K2CO3 (b) => 100a + 138b = 12, 76
Khi nung nK2CO3 = 0,5a + b = 0,07 => a = 0,01; b - 0,02
Bảo toàn K: x +2y = a +2b
Bảo toàn C: x + y + 0,04 = a + b => x = 0,02; y = 0,06
.....................................
Dưới đây là một số đề thi thử THPT Quốc gia năm 2020 môn Hóa của các Sở, Trường THPT mới nhất trên cả nước, mời các bạn tham khảo.
- Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Vĩnh Phúc lần 2
- Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Trường THPT Chuyên Hạ Long, Quảng Ninh
- Bộ đề thi thử THPT quốc gia năm 2020 môn Hóa học (Có đáp án)
VnDoc.com xin gửi Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hải Phòng tới bạn đọc để bạn đọc cùng tham khảo. Với 40 câu hỏi trắc nghiệm trong thời gian 50 phút, đề thi này được đánh giá là vừa sức với tất cả các bạn học sinh dùng để xét tốt nghiệp cũng như vào các trường Đại học.
Trên đây VnDoc.com vừa giới thiệu Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hải Phòng tới các bạn, mong rằng qua bài viết này các bạn có thể học tập tốt hơn môn Hóa Học. Mời các bạn cùng tham khảo thêm các môn Sinh học 12, Tiếng Anh 12, Thi thpt Quốc gia môn Toán, Thi THPT Quốc gia môn Vật Lý,....
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu ôn tập THPT Quốc gia miễn phí trên Facebook: Quyết tâm đỗ Đại Học Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu, đề thi mới nhất.