Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hà Nội lần 3



Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hà Nội lần 3 được VnDoc tổng hợp, biên soạn kèm đáp án, hướng dẫn giải. Đề thi gồm 40 câu hỏi trắc nghiệm nằm trong bài thi phân môn Khoa học tự nhiên môn thi Hóa học, đề thi đưa ra vẫn đảm bảo bám sát cấu trúc đề minh họa của bộ GD&ĐT đưa ra trước đó.
Hy vọng với đề thi thử THPT Quốc gia năm 2020 môn Hóa của các trường đưa ra sẽ giúp các em ôn luyện đề tốt hơn, chuẩn bị cho kì thi THPT quốc gia.
Để xem và tải đầy đủ chi tiết đề thi , hướng dẫn giải xin vui lòng ấn tải link phía dưới
Đề thi thử THPT Quốc gia năm 2020 môn Hóa
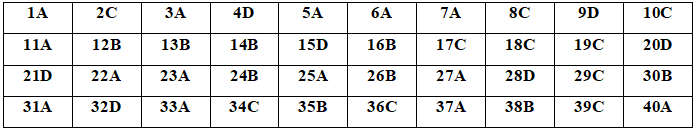
Đáp án đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hà Nội lần 3
Hướng dẫn giải đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hà Nội lần 3
Câu 9. Trong phèn chua có chứa loại muối nhôm nào sau đây?
A. AlCl3
B. AlBr3
C. Al(NO3)3
D. Al2(SO4)3
Hướng dẫn giải
Công thức phèn chua: K2SO4.Al2(SO4)3.24H2O
Câu 12. Kim loại Fe không tan trong dung dịch nào sau đây?
A. HCl.
B. HNO3 đặc, nguội
C. Fe2(SO4)3.
D. H2SO4 loãng
Hướng dẫn giải
Fe, Cr, Al không phản ướng với HNO3 đặc, nguội
Câu 15. Oxit nào sau đây bị khử bởi khí CO ở nhiệt độ cao?
A. Na2O.
B. Al2O3
C. MgO.
D. Fe2O3.
Hướng dẫn giải
Fe2O3 + CO Fe + CO2
Câu 16. Cho các polime sau: poli(vinyl clorua); poli(metyl metacrylat); poli(etylen terephtalat); poliacrilonitrin. Số polime được điều chế bằng phản ứng trùng hợp là?
A.1
B.3.
C.2
D.4
Câu 17. Cho 18,75 gam H2NCH2COOH phản ứng hết với dung dịch KOH, thu được dung dịch chứa m gam muối. Giá trị của m là
A. 37,50.
B. 24,25.
C. 28,25.
D. 32,75.
Hướng dẫn giải
H2NCH2COOH + KOH →H2NCH2COOK + H2O
0,25 → 0,25 => m muối = 0,25 x 113 = 28,25 gam
Câu 20. Ngâm một lá kẽm trong 100 ml dung dịch AgNO3 0,1M. Giả sử toàn bộ lượng kim loại Ag sinh ra đều bám hết vào lá kẽm. Khi phản ứng kết thúc, nhấc lá kẽm ra, làm khô, khối lượng lá kẽm tăng thêm
A. 0,430 gam
B. 0,215 gam
C. 1,080 gam
D. 0,755 gam
Hướng dẫn giải
Ta có:
Zn + 2Ag+ → 2Ag + Zn2+
0,01 ← 0,01 0,01 0,01
Khối lượng Zn tăng thêm là: m = 0,01 x 108 - 0,05 x 65 = 0,755 gam
Câu 22. Cho dung dịch NaOH đến dư vào dung dịch muối X thu được kết tinh trắng. Muối X là:
A. Mg(NO3)2
B. K2CO3
C. FeCl3
D. CuSO4
Hướng dẫn giải
A: kết tủa trắng tinh
B: kết tủa đỏ nâu
C: kết tủa xanh
Câu 25. Đun nóng 200 ml dung dịch glucozơ a mol/lít với lượng dư dung dịch AgNO3 trong NH3. Sau khi phản ứng xảy ra hoàn toàn, thu được 21,6 gam Ag. Giá trị của a là
A. 0,5.
B. 0,2
C. 0,1
D. 1,0
Hướng dẫn giải
Glu + AgNO3 → 2Ag
0,1 mol ← 0,2 mol
=> CM = 0,5M
Câu 27. Đốt cháy hoàn toàn m gam Al trong khí O2 dư, thu được 10,2 gam Al2O3. Giá trị của m là
A. 5,40
B. 1,35.
C. 4,80.
D. 2,70.
Hướng dẫn giải
4Al + 3O2 2Al2O3
0,2 mol ← 0,1 mol
=> mAl = 5,4 gam
Câu 30. Sau khi kết thúc các phản ứng, thí nghiệm nào sau đây thu được muối sắt(III)
A. Cho lượng dư bột sắt vào dung dịch HNO3 đặc nóng
B. Cho bột sắt vào dung dịch AgNO3 dư
C. Nung nóng hỗn hợp bột sắt và lưu huỳnh bột (không có không khí)
D. Cho FeCO3 vào dung dịch H2SO4 loãng dư
Hướng dẫn giải
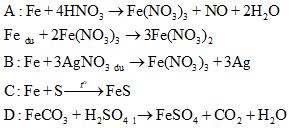
Câu 31. Đun nóng a gam hỗn hợp E chứa triglixerit X và các axit béo với 200 ml dung dịch NaOH 1M (vừa đủ), thu được glixerol và hỗn hợp muối Y. Hiđro hóa hoàn toàn Y cần vừa đủ 0,1 mol H2 chỉ thu được muối natri panmitat. Đốt cháy 0,07 mol E thu được 1,645 mol CO2. Biết các phản ứng xảy ra hoàn toàn. Giá trị của a là
A. 52,14
B. 54,56
C. 50,16
D. 55,40
Hướng dẫn giải
Ta thấy: Y gồm các muối 16C nên X sẽ có 51C và các axit béo (Gọi chung là M) có cùng 16C
Số C = nCO2/nE = 1,645/0,07 = 23,5 => nX: nM = 3:11
Đặt n X = 3a => nA = 11a
=>nNaOH = 3 x 3a + 11 a= 0,2 => a = 0,01
=> n H2O = 0,11 mol và nC3H5(OH)3 = 0,03 mol
Muối gồm: C15H31COONa (0,2 mol) và H2 (-0,1)
=> m muối = 0,2 x 278 = 55,4 gam
BTKL: mE + mNaOH = mmuối+ mH2O + mC3H5(OH)3
=> mE = 55,4 + 0,11 x 18 + 0,03 x 92 - 0,2 x 40 = 52,14 gam
Câu 32. Cho m gam hỗn hợp X gồm CuO; Fe2O3; FeO tác dụng vừa đủ với 100 ml dung dịch chứa H2SO4 1M và HCl 1M. Để khử hoàn toàn m gam hỗn hợp X (nung nóng) cần tối thiểu V lít khí CO (đktc). Giá trị của V là
A. 4,48.
B. 6,72.
C. 2,24
D. 3,36.
Hướng dẫn giải
nH+ = 0,1 x 2 + 0,1 = 0,3 mol
2H+ + O2- → H2O
0,3 → 0,15
CO + [O] → CO2
0,15 ← 0,15
=> V = 0,15 x 22,4 = 3,36 lít
Câu 33. Tiến hành thí nghiệm theo các bước sau:
Bước 1: Nhỏ 3 giọt dung dịch anilin vào ống nghiệm chứa 2 ml nước cất, lắc đều, sau đó để yên
Bước 2: Nhúng giấy quỳ tím vào dung dịch trong ống nghiệm, sau đó nhấc giấy quỳ ra
Bước 3: Nhỏ tiếp 1 ml dung dịch HCl đặc vào ống nghiệm, lắc đều sau đó để yên
Bước 4: Nhỏ tiếp 1 ml dung dịch NaOH đặc vào ống nghiệm, lắc đều, sau đó để yên
Cho các phát biểu sau
a) Kết thúc bước 1, anilin hầu như không tan và lắng xuống đáy ống nghiệm
b) Kết thúc bước 2, giấy quỳ tím chuyển thành màu xanh do anilin có tính bazơ
c) Kết thúc bước 3, thu được dung dịch trong suốt
d) Kết thúc bước 4, trong ống nghiệm có anilin tạo thành
Số phát biểu đúng là
A. 3
B. 2
C. 1
D. 4
Câu 34. Cho 0,06 mol hỗn hợp hai este đơn chức X và Y tác dụng vừa đủ với dung dịch KOH thu được hỗn hợp Z gồm các chất hữu cơ. Đốt cháy hoàn toàn Z thu được H2O; 0,144 mol CO2 và 0,036 mol K2CO3. Làm bay hơi Z thu được m gam chất rắn. Giá trị của m là
A. 6,840
B. 5,040
C. 6,624
D. 5,472
Hướng dẫn giải
Ta có nKOH = 2nK2CO3 = 0,036 x 2 = 0,072 mol
neste (0,06) <n KOH (0,072) < 2neste => nên hỗn hợp 2 este đơn chức ban đầu gồm
este ancol + KOH
0,048 mol
Este phenol + 2KOH
0,012
BTNT: nC = nCO2 + nK2CO3 = 0,18 => Số C = 3
=> HCOOCH3 (0,048 mol) và CxHyO2 (0,012 mol)
nC = 0,048 . 2 + 0,012.x = 0,18 mol => x = 7 (HCOOC6H5)
Chất rắn gồm HCOOK (0,06) và C6H5OK ( 0,012 mol) => m rắn = 6,624 gam
...............
Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hà Nội lần 3 là đề thi thử THPT Quốc gia năm 2020 của sở Hà Nội. Đề thi đưa ra dựa trên phát triển nội dung từ đề thi minh họa Bộ GD&ĐT đã đưa ra. Đề thi thử lần 3 này, được đánh giá là khó hơn các đề thi thử lần 1, lần 2. Hy vọng với Đề thi thử Hà Nội môn Hóa 2020 này giúp các bạn học sinh thêm nguồn tài liệu ôn tập luyện đề tốt nhất.
VnDoc đã gửi Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hà Nội lần 3 tới bạn đọc. Để có kết quả cao hơn trong kì thi, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Thi thpt Quốc gia môn Toán, Thi THPT Quốc gia môn Sinh học, Thi THPT Quốc gia môn Vật Lý, Thi THPT Quốc gia môn Tiếng Anh mà VnDoc tổng hợp và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu ôn tập THPT Quốc gia miễn phí trên Facebook: Quyết tâm đỗ Đại Học Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu, đề thi mới nhất.