Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Thái Bình



Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Thái Bình được VnDoc tổng hợp, biên soạn kèm đáp án, hướng dẫn lời giải chi tiết. Đề thi gồm 40 câu hỏi trắc nghiệm, bám sát cấu trúc đề thi thử của bộ GD&ĐT đưa ra trước đó. Hy vọng với Đề thi thử môn Hóa 2020 của các trường đưa ra sẽ giúp các em ôn luyện đề tốt hơn, chuẩn bị cho kì thi THPT quốc gia môn Hóa học.
Đề thi thử THPT quốc gia 2020 môn Hóa Sở GD&ĐT Thái Bình
1. Đáp án đề thi thử THPT Quốc gia năm 2020 môn Hóa Sở Thái Bình
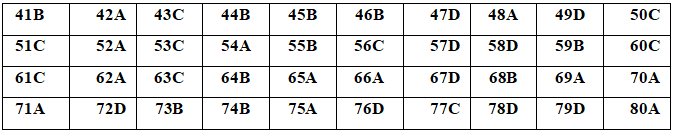
2. Hướng dẫn giải chi tiết đề thi thử THPT Quốc gia 2020 môn Hóa Sở Thái Bình
Câu 41: Thủy phân este CH3COOCH2C6H5 (mùi thơm hoa nhài) trong dung dịch NaOH, ancol thu được có công thức là
A. CH3OH.
B. C6H5CH2OH.
C. C6H5OH.
D. C2H5OH.
Hướng dẫn giải
CH3COOCH2C6H5 + NaOH → CH3COONa + C6H5CH2OH
Câu 50: Chất làm mất màu nước brom ngay ở nhiệt độ thường là
A. metan.
B. toluen.
C. etilen.
D. benzen.
Hướng dẫn giải
C2H4 + Br2 → C2H4Br2
Câu 54: Kim loại sắt phản ứng với chất nào sau đây tạo muối sắt (III)?
A. Khí Cl2 (đun nóng).
B. Dung dịch H2SO4 loãng.
C. Dung dịch HCl.
D. Lưu huỳnh (đun nóng).
Hướng dẫn giải
A :2Fe + 3Cl2 → 2FeCl3
B; C :Fe + 2H+ Fe2+ + H2
D :Fe + S FeS
Câu 56: Kim loại không tác dụng với dung dịch H2SO4 loãng, nguội là
A. Mg.
B. Al.
C. Cu.
D. Zn.
Hướng dẫn giải
Kim loại Cu đứng sau hidro nên không tác dụng được với H2SO4 loãng, nguội
Câu 58: Cho m gam bột Fe vào dung dịch CuSO4 dư, kết thúc phản ứng thu được 5,12 gam Cu. Giá trị của m là
A. 3,36.
B. 5,60.
C. 2,24.
D. 4,48.
Hướng dẫn giải
nFe=nCu=0,08 mol => mFe= 0,08.56 = 4,48 gam
Câu 59: Cho 6,72 gam Fe tác dụng với oxi chỉ thu được 9,28 gam hỗn hợp X chỉ chứa 3 oxit. Hòa tan X cần vừa đủ V ml dung dịch H2SO4 1M (loãng). Giá trị của V là
A. 120.
B. 160.
C. 320.
D. 80.
Hướng dẫn giải
Câu 64: Để tráng một chiếc gương soi, ta đun dung dịch chứa 36 gam glucozơ với lượng vừa đủ dung dịch AgNO3 trong NH 3. Khi phản ứng xảy ra hoàn toàn, khối lượng bạc (gam) thu được là
A. 21,6.
B. 43,2
C. 54,0.
D. 10,
Hướng dẫn giải
nGlu = 36/180 = 0,2 mol
nAg=2nGlu = 0,2 .2 = 0,4 mol => mAg = 0,4.108 = 43,2 gam
Câu 67: Hỗn hợp X gồm glyxin, alanin, valin, axit glutamic, metylamin và etylamin. Đốt cháy hoàn toàn 0,16 mol hỗn hợp X cần dùng vừa đủ 0,57 mol O2, sản phẩm cháy gồm CO2, H2O và N2 (trong đó số mol CO2 là 0,37 mol). Nếu cho lượng X ở trên vào dung dịch KOH dư thấy có m gam KOH tham gia phản ứng. Giá trị của m là
A. 2,24.
B. 2,8.
C. 3,36.
D. 3,92
Hướng dẫn giải
Gly = NH3 + CH2 + CO2
Ala = NH3 + 2CH2 + CO2
Val = NH3 + 4CH2 + CO2
CH3NH2 = NH3 + CH2
C2H5NH2 = NH3 + 2CH2
Quy đổi hỗn hợp X thành NH3 (0,16 mol), CH2 (x mol), CO2 (y mol)
nO2 = 0,16 .0,75 + 1,5 x = 0,57 => x = 0,3 mol
nCO2 = x + y = 0,37 => y = 0, 07=> nKOH = y = 0,07 => m = 3,92 gam
Câu 68: Chất X (CnH2n+4O4N2) là muối amoni của axit cacboxylic đa chức, chất Y (CmH2m-3O6N5) là pentapeptit được tạo bởi một aminoaxit. Cho 0,26 mol E gồm X và Y tác dụng tối đa với dung dịch chứa 0,7 mol NaOH, đun nóng thu được etylamin và dung dịch T chỉ chứa 62,9 gam hỗn hợp muối. Phần trăm khối lượng của Y trong E có giá trị gần nhất với giá trị nào sau đây?
A. 47,24%
B. 36,58%.
C. 38,42%.
D. 42,78%
Hướng dẫn giải
nE = nX + nY = 026 mol, nNaOH = 2nX + 5nY = 0,7 mol => nX 0,2 mol, nY = 0,06 mol
Muối gồm A(COONa)2 0,2 mol; NH2-B-COONa (0,06.5 = 0,3 mol)
mmuối = 0,2.(A + 134) + 0,3.(B + 83) = 62,9 => 2A + 3B = 112 => A = 14; B =28
E gồm CH2(COONH3C2H5)2 (0,2); (Ala)5 (0,06) => %m Y =36,58%
Câu 69: Hỗn hợp X gồm axit oleic, axit stearic và một triglixerit. Đốt cháy hoàn toàn m gam hỗn hợp X cần vừa đủ 1,445 mol O2 thu được 1,02 mol CO2. Mặt khác m gam hỗn hợp X làm mất màu vừa đủ 6,4 gam brom trong CCl4. Nếu cho m gam hỗn hợp X phản ứng với dung dịch NaOH đun nóng (vừa đủ) thu glixerol và dung dịch chứa hai muối. Khối lượng axit stearic trong m gam hỗn hợp X là
A. 4,26.
B. 2,13.
C. 2,272.
D. 2,84.
Hướng dẫn giải
nBr2 = 0,04 mol
Quy đổi X thành C17H33COOH (0,04); C17H35COOH (a); C3H5(OH)3 (b); H2O (-3b)
nO2 = 0, 04.25,5 + 26a + 3,5b =1, 445
nCO2 = 0,04 .18 + 18a + 3b = 1,02 => a = 0,015 mol, b = 0,01 mol
TH1: Chất béo là: (C17H33COO)3C3H5 (0,01 mol) => m = 284a = 4,26 gam
TH2: Chất béo là: (C17H33COO)2(C17H35COO)C3H5 (0,01 mol)
=> m = 284(a - 0,01) = 1,42 gam
Câu 70: Hỗn hợp X gồm ba este mạch hở. Cho 0,055 mol X phản ứng vừa đủ với 0,09 gam H2 (xúc tác Ni, t°), thu được hỗn hợp Y. Cho toàn bộ Y phản ứng vừa đủ với 65 ml dung dịch KOH 1M, thu được hỗn hợp Z gồm hai muối của hai axit cacboxylic no, có mạch cacbon không phân nhánh và 3,41 gam hỗn hợp T gồm hai ancol no, đơn chức. Mặt khác, đốt cháy hoàn toàn 0,1 mol X cần vừa đủ 11,2 lít O2 (đktc). Tổng khối lượng của 2 muối trong hỗn hợp có giá trị là
A. 5,72.
B. 7,97.
C. 4,68.
D. 7,24.
Hướng dẫn giải
nY = nX = 0,055 mol nKOH = 0,065 mol => Y chứa este đơn chức (0,045 mol) và este hai chức 0,1 mol (do các muối không phân nhanh nên tối đa hai chức)
Đốt cháy 0,055 mol X cần:
=> Đốt 0,055 mol Y cần nO2 = 0,275 + nH2/2 = 0,2975
Đốt Y => nCO2 (x mol), H2O (y mol)
Bảo toàn nguyên tố O => 2x + y = 0,065.2 + 0,2975.2
n Este 2 chức = x – y = 0,01 => x = 0,245; y = 0,235
nT = nKOH = 0,065 mol
T chứa C (a mol); H (b mol); O (0,065 mol)
mT = 12a + b + 0,065.16 = 3,14 gam
nT = b/2 - a = 0,065 => a = 0,16; b= 0,45 mol
Bảo toàn nguyên tố C => nC muối = x – a = 0,085
Bảo toàn H => nH muối = 2y + nKOH – b = 0,085
Do nC muối = nHmuối nên các muối có số C = số H
=> Muối gồm HCOOK (u mol) và C2H4(COOK)2 (v mol)
nKOH = u + 2v = 0,065 mol; nC muối = u + 4v = 0,085 mol => u = 0,045 mol, v = 0,01 mol
=> m 2 muối = 5,72 gam
Để xem chi tiết đề thi cũng như hướng dẫn giải chi tiết xin vui lòng ấn tải link phía dưới
VnDoc đã gửi Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Thái Bình tới bạn đọc. Để có kết quả cao hơn trong kì thi, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Thi thpt Quốc gia môn Toán, Thi THPT Quốc gia môn Hóa học, Thi THPT Quốc gia môn Vật Lý, mà VnDoc tổng hợp và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu ôn tập THPT Quốc gia miễn phí trên Facebook: Quyết tâm đỗ Đại Học Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu, đề thi mới nhất.