Tổng hợp toàn bộ kiến thức Hoá học lớp 12

VnDoc.com xin giới thiệu tới các bạn học sinh bộ tài liệu: Tổng hợp toàn bộ kiến thức Hoá học lớp 12. Với nội dung bộ tài liệu đã được VnDoc cập nhật một cách chi tiết sẽ giúp các bạn học sinh có kết quả cao hơn trong học tập. VnDoc mời thầy cô cùng các bạn học sinh tham khảo.
- Đề cương hóa 12 học kì 2 năm 2021 Chi tiết đầy đủ
- Đề thi học kì 2 hóa 12 năm học 2020 - 2021 Đề 2
- Đề thi học kì 2 hóa 12 năm học 2020 - 2021 Đề 1
Toàn bộ kiến thức Hoá học lớp 12
A. MỘT SỐ VẤN ĐỀ LÍ THUYẾT CẦN NẮM VỮNG
1. Khái niệm về dẫn xuất của axit cacboxylic
Dẫn xuất của axit cacboxylic là những sản phẩm tạo ra khi thay thế nhóm hiđroxyl - OH trong nhóm cacboxyl -COOH bằng nguyên tử hay nhóm nguyên tử khác: -COOH -COZ (với Z: OR', NH2, OCOR, halogen, …).
Este là dẫn xuất của axit cacboxylic. Khi thay thế nhóm OH ở nhóm cacboxyl của axit cacboxylic bằng nhóm OR' thì được este.
Halogenua axit (quan trọng nhất là clorua axit RCOCl). Để tạo ra halogenua axit có thể dùng các tác nhân như PCl5 (photpho pentaclorua), PCl3 (photpho triclorua), COCl2 (photgen), SOCl2 (thionyl clorua), …
RCOOH + PCl5 → RCOCl + POCl3 + HCl
3RCOOH + PCl3 → 3RCOCl + H3PO3
RCOOH + SOCl2 → RCOCl + SO2 + HCl
RCOOH + COCl2 → RCOCl + CO2 + HCl
Anhiđrit axit, có 2 loại: đối xứng (dạng (RCO)2O hoặc (ArCO)2O; gọi tên bằng cách thay từ axit bằng anhiđrit (CH3CO)2O là anhiđrit axetic), và không cân đối (sinh ra từ hai axit monocacboxylic khác nhau như CH3CO-O-OCC6H5; gọi tên bằng từ anhiđrit cộng với tên của hai axit - anhiđrit axetic benzoic).
Để tạo thành anhiđrit axit có thể sử dụng nhiều phương pháp khác nhau như dùng tác nhân hút nước P2O5 hay tác dụng của nhiệt, …
2. ESTE .
2.1. Khái niệm:
Khi thay nhóm OH ở nhóm cacboxyl của axit cacboxylic bằng nhóm OR thì được este
Công thức tổng quát của este
a/ Trường hợp đơn giản: là este không chứa nhóm chức nào khác, ta có các công thức như sau
Tạo bởi axit cacboxylic đơn chức RCOOH và ancol đơn chức R'OH: RCOOR'.
Tạo bởi axit cacboxylic đa chức R(COOH)a và ancol đơn chức R'OH: R(COOR')a
Tạo bởi axit cacboxylic đơn chức RCOOH và ancol đa chức R'(OH)b: (RCOO)bR'
Tạo bởi axit cacboxylic đa chức R(COOH)a và ancol đa chứcR'(OH)b: Rb(COO)abR'a.
Trong đó, R và R' là gốc hiđrocacbon (no, không no hoặc thơm); trường hợp đặc biệt, R có thể là H (đó là este của axit fomic H-COOH).
b/ Trường hợp phức tạp: là trường hợp este còn chứa nhóm OH (hiđroxi este) hoặc este còn chứa nhóm COOH (este - axit) hoặc các este vòng nội phân tử … Este trong trường hợp này sẽ phải xét cụ thể mà không thể có CTTQ chung được. Ví dụ với glixerol và axit axetic có thể có các hiđroxi este như HOC3H5(OOCCH3)2 hoặc (HO)2C3H5OOCCH3; hoặc với axit oxalic và metanol có thể có este - axit là HOOC-COOCH3.
c/ Công thức tổng quát dạng phân tử của este không chứa nhóm chức khác
Nên sử dụng CTTQ dạng CnH2n+2-2ΔO2n (trong đó n là số cacbon trong phân tử este n ≥ 2, nguyên; Δ là tổng số liên kết π và số vòng trong phân tử Δ ≥ 1, nguyên; a là số nhóm chức este a ≥ 1, nguyên), để viết phản ứng cháy hoặc thiết lập công thức theo phần trăm khối lượng của nguyên tố cụ thể.
Este đơn chức RCOOR,Trong đó R là gốc hidrocacbon hay H; R’ là gốc hidrocacbon
Este no đơn chức CnH2nO2 ( với n ≥ 2)
Tên của este:
Tên gốc R’ + tên gốc axit RCOO (đuôi at)
Vd: CH3COOC2H5
Etylaxetat
CH2=CH- COOCH3 metyl acrylat
2.2.Lí tính:
Nhiệt độ sôi ,độ tan trong nước thấp hơn axit và ancol có cùng số cacbon:
axit > ancol > este
Một số mùi đặc trưng: Isoamyl axetat : mùi chuối chín ; Etyl butiat ,etyl propionat có mùi dứa
2.3 TÍNH CHẤT HÓA HỌC:
Phản ứng thủy phân
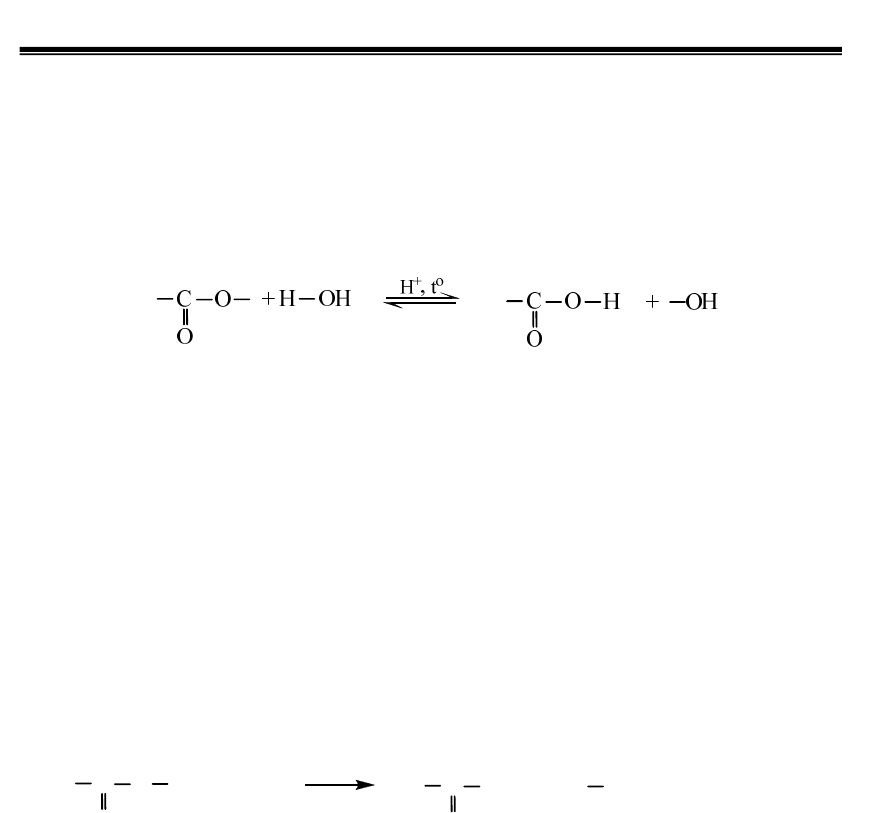
Tính chất hoá học quan trọng nhất của este là phản ứng thuỷ phân. Sơ đồ thuỷ phân
este (về cơ bản, chưa xét các trường hợp đặc biệt) là:
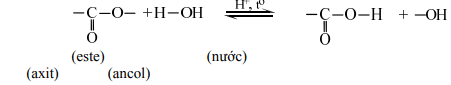
Thuỷ phân chính là quá trình nghịch của của phản ứng este hoá.
Phản ứng thuỷ phân có thể xảy ra trong môi trường axit hoặc môi trường bazơ.
Phản ứng thuỷ phân trong môi trường kiềm được gọi là phản ứng xà phòng hoá.
Đặc điểm của phản ứng thuỷ phân este:
Phản ứng thuỷ phân este trong môi trường axit là phản ứng thuận nghịch. Sản phẩm của phản ứng trong điều kiện này luôn có axit cacboxylic. Để chuyển dịch cân bằng về phía tạo axit và ancol, ta dùng lượng dư nước.
Phản ứng thuỷ phân este không những thuận nghịch mà còn rất chậm. Để tăng tốc độ phản ứng thuỷ phân ta đun nóng hỗn hợp phản ứng với với chất xúc tác axit (H2SO4, HCl…).
Phản ứng xà phòng hoá chỉ xảy ra một chiều, sản phẩm thu được luôn có muối của axit
cacboxylic.
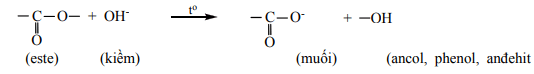
a. Thủy phân trong môi trường axit: tạo ra 2 lớp chất lỏng, là phản ứng thuận nghịch (2
chiều )
RCOOR' + H2O RCOOH + R'OH
b. Thủy phân trong môi trường bazơ ( Phản ứng xà phòng hóa ) : là phản ứng 1 chiều
RCOOR' + NaOH RCOONa + R'OH
ESTE đốt cháy tạo thành CO2 và H2O. nCO2 = nH2O ta suy ra este đó là este no đơn chức ,hở (CnH2nO2)
2/ Phản ứng của gốc hiđrocacbon
Este không no (este của axit không no hoặc ancol không no) có khả năng tham gia phản ứng cộng và phản ứng trùng hợp – đây là tính chất do liên kết π quy định (tương tự như hiđrocacbon tương ứng). Một số phản ứng thuộc loại này có ứng dụng quan trọng là: Phản ứng chuyển hoá dầu (chất béo lỏng) thành mỡ (chất béo rắn)
Để tham khảo toàn bộ tài liệu mời các bạn ấn link TẢI VỀ phía dưới
......................................
Mời các bạn tham khảo đề thi thử:
- 53 câu hỏi trắc nghiệm Hóa học: Luyện Tập NH3 - NH4+
- Đề thi thử THPT Quốc gia năm 2021 môn Hóa Sở GD&ĐT An Giang Lần 1
- Bộ đề thi thử THPT quốc gia năm 2020 môn Hóa Hay Chọn Lọc Có đáp án
- Đáp án Đề thi THPT Quốc Gia 2020 môn Hóa
- Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Trường Chuyên Đại học Sư phạm Hà Nội
------------------------------------
Trên đây VnDoc.com đã giới thiệu tới bạn đọc tài liệu: Tổng hợp toàn bộ kiến thức Hoá học lớp 12. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Hóa học lớp 10, Giải bài tập Hóa học lớp 11, Hóa học lớp 12, Thi thpt Quốc gia môn Văn, Thi thpt Quốc gia môn Lịch sử, Thi thpt Quốc gia môn Địa lý, Thi thpt Quốc gia môn Toán, đề thi học kì 1 lớp 11, đề thi học kì 2 lớp 11 mà VnDoc tổng hợp và đăng tải.
Để thuận tiện cho quá trình trao đổi xũng như cập nhật các tài liệu mới nhất của trang VnDoc. Mời bạn đọc cùng tham gia nhóm Tài liệu học tập lớp 12 để có thêm tài liệu học tập nhé
