Đề thi giải toán trên Máy tính cầm tay cấp Quốc gia năm 2013 môn Hóa lớp 12 THPT
Vndoc.com xin giới thiệu đến các bạn: Đề thi giải toán trên Máy tính cầm tay cấp Quốc gia năm 2013 môn Hóa lớp 12 THPT.
Đề thi môn Hóa học:
BỘ GIÁO DỤC VÀ ĐÀO TẠO
|
CUỘC THI GIẢI TOÁN TRÊN MÁY TÍNH CẦM TAY
|
Bài 1: (5 điểm)
Hỗn hợp giữa hai loại bột A và B có ứng dụng rộng rãi trong tàu lặn. Phân tử chất bột A được tạo thành từ các ion X+ và Z2-2. Tổng số hạt proton, notron, electron trong một phân tử A bằng 116, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 36 hạt. Số khối của X lớn hơn số khối của Z là 7 đơn vị. Tổng số hạt proton, notron, electron trong X+ ít hơn trong Z2-2 là 17 hạt. Phân tử chất bột B được tạo thành từ các ion Y+ và Z-2. Tổng số hạt proton, notron, electron trong Y+ nhiều hơn trong Z-2 là 8 hạt và số hạt mang điện trong Y+ lớn hơn số hạt mang điện trong Z-2 là 4 hạt (X, Y, Z là kí hiệu các nguyên tố chưa biết). Xác định công thức phân tử của A, B và viết phương trình hóa học biểu diễn ứng dụng nói trên của chúng.
Bài 2: (5 điểm)
Câu 1: Vanadi (V) có khối lượng riêng là 5,96g/cm3, kết tinh theo cấu trúc mạng lập phương với cạnh của ô mang cơ sở là 307pm. Biết khối lượng mol nguyên tử của Vanadi là 50,94.
a. Vanadi kết tinh theo kiểu mạng tinh thể nào?
b. Tính số phối trí của Vanadi trong cấu trúc mạng tinh thể đó? Giải thích?
c. Tính thể tích không gian trống trong ô mạng cơ sở của Vanadi?
Câu 2: Tính giá trị năng lượng mạng lưới tinh thể ion của hợp chất BaCl2. Cho biết entanpi chuẩn của các quá trình sau:
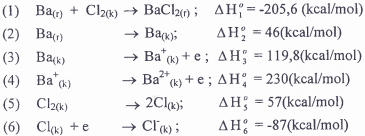
Bài 3: (5 điểm)
Câu 1: Cho một dung dịch FeCl3 có nồng độ C(mol/l). Ion Fe3+ hidrat hóa là một axit có pKa = 2,2. Tính nồng độ C và pH của dung dịch FeCl3 mà tại đó bắt đầu kết tủa của Fe(OH)3. Cho pTFe(OH) = 38
Câu 2: Dung dịch A gồm FeCl3 0,10M, MnCl2 0,10M, ZnCl2 0,01M, CdCl2 0,1M. Sục khí H2S vào dung dịch A đến bão hòa (nồng độ H2S bão hòa = 0,10M), thu được kết tủa B. Xác định thành phần hóa học của B?
Cho: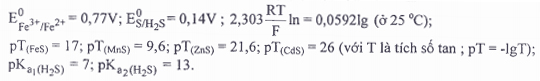
Bài 4: (5 điểm)
Trong công nghiệp người ta có thể điều chế hidro bằng cách cho hơi nước đi qua than nung đỏ, các phản ứng hóa học xảy ra như sau: Ở nhiệt độ nghiên cứu, phản ứng (2) có Kp = 5; trong phản ứng (2) người ta dùng n mol H2O cho 1 mol CO (Các phản ứng được thực hiện ở cùng nhiệt độ)
1. Hãy xác định mối quan hệ giữa x, n và Kp (với x là phần mol của CO trong hỗn hợp tại trạng thái cân bằng.
2. Tính x khi n = 3.
3. Tính giá trị của n để hỗn hợp cân bằng chứa không quá 1%CO
Bài 5: (5 điểm)
Hỗn hợp X có khối lượng 12,21 gam gồm CuO, Al2O3 và oxit của sắt. Cho H2 (dư) qua X nung nóng, sau khi phản ứng xong thu được 2,16 gam H2O. Hòa tan hoàn toàn X cần dùng 255ml dung dịch H2SO4 loãng 1M, thu được dung dịch Y. Cho dung dịch NaOH (dư) vào dung dịch Y, sau phản ứng lọc lấy kết tủa rồi đem nung trong không khí đến khối lượng không đổi, được 7,8 gam chất rắn. Xác định công thức của oxit sắt và tính khối lượng mỗi oxit trong hỗn hợp X ban đầu.
Bài 6: (5 điểm)
Cho hỗn hợp A gồm H2, một anken và một ankin có cùng số nguyên tử cacbon trong phân tử. Tỉ khối hơi của A so với H2 bằng 7,8. Sau khi cho A qua bột Ni nung nóng để các phản ứng xảy ra hoàn toàn, thu được hỗn hợp B có tỉ khối hơi so với hỗn hợp A là 20/9. Xác định công thức phân tử anken, ankin và tính thành phần phần trăm theo thể tích mỗi chất trong hỗn hợp A nói trên.
