Đề thi thử THPT Quốc gia năm 2017 môn Hóa học Sở GD&ĐT Phú Yên
Đề thi thử THPT Quốc gia 2017 môn Hóa học
Đề thi thử THPT Quốc gia năm 2017 môn Hóa học Sở GD&ĐT Phú Yên. Đề thi gồm có 40 câu hỏi trắc nghiệm nhằm kiểm tra, đánh giá năng lực học tập của học sinh để có kế hoạch tổ chức ôn thi THPT Quốc gia trong giai đoạn nước rút được tốt hơn. Mời các bạn cùng tham khảo.
Đề thi thử THPT Quốc gia năm 2017 môn Hóa học Sở GD&ĐT Hải Phòng
| SỞ GIÁO DỤC VÀ ĐÀO TẠO PHÚ YÊN |
KỲ KHẢO SÁT NĂNG LỰC HỌC SINH LỚP 12 THPT NĂM HỌC 2016 - 2017 Môn: HÓA HỌC Thời gian: 50 phút (không kể thời gian giao đề) Số câu trắc nghiệm: 40 |
Cho khối lượng mol nguyên tử (gam/mol) các nguyên tố: H = 1; C = 12; N = 14; O = 16; S = 32; Cl = 35,5; Na = 23; Mg = 24; Al = 27; K = 39; Ca = 40; Fe = 56; Cu = 64; Ag = 108; Ba = 137; điều kiện tiêu chuẩn được viết tắt là đktc
Câu 1: Nước cứng là nước có chứa nhiều các ion:
A. Na+, K+. B. Mg2+, Ca2+. C. Cl-, HCO3-. D. HCO3-, SO42-.
Câu 2: Chất nào trong số các chất sau đây, có nhiệt độ nóng chảy cao nhất?
A. CH3CH2OH. B. H2NCH2COOH. C. CH3CH2NH2. D. CH3COOCH3.
Câu 3: Trong các chất dưới đây, chất nào là đipeptit?
A. H2NCH2CONHCH(CH3)COOH.
B. H2NCH(CH3)CONHCH2CH2COOH.
C. H2NCH2CONHCH2CH(CH3)COOH.
D. H2NCH2CONHCH(CH3)CONHCH2COOH.
Câu 4: Chất nào dưới đây không có khả năng tan trong dung dịch NaOH?
A. Al. B. Cr. C. Al2O3. D. Cr(OH)3.
Câu 5: Cho các phản ứng sau:
(1) Kim loại (X) + Cl2 ![]() (Y)
(Y)
(2) (Y) + dd KOH dư → muối (Z) + muối (T) + H2O.
Kim loại X có thể là kim loại nào sau đây?
A. Al. B. Mg. C. Fe. D. Cu.
Câu 6: Cho hỗn hợp gồm 5,6 gam Fe và 6,4 gam Cu vào dung dịch H2SO4 loãng, dư. Phản ứng xong, thu được V lít (đktc) khí H2. Giá trị của V là
A. 4,48. B. 1,12. C. 3,36. D. 2,24.
Câu 7: Để rửa sạch lọ đã chứa anilin người ta dùng
A. dung dịch NaOH và nước. B. dung dịch HCl và nước.
C. dung dịch amoniac và nước. D. dung dịch NaCl và nước.
Câu 8: Chất X tan trong nước và tác dụng được với dung dịch HCl. Chất X là
A. Na2CO3. B. Al(OH)3. C. CaCO3. D. BaSO4.
Câu 9: Tiến hành thí nghiệm được mô tả theo hình vẽ sau:
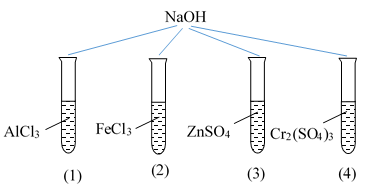
Khi cho dung dịch NaOH đến dư, phản ứng xong, ở ống nghiệm nào thu được kết tủa?
A. (2). B. (3). C. (4). D. (1).
Câu 10: Để xử lí chất thải có tính axit, người ta thường dùng
A. giấm ăn. B. nước vôi trong. C. lưu huỳnh. D. thạch cao.
Câu 11: Kim loại có khả năng dẫn điện tốt nhất là
A. Ag. B. Au. C. Al. D. Cu.
Câu 12: Kim loại phản ứng với nước ở nhiệt độ thường, tạo ra dung dịch có môi trường kiềm là
A. Na. B. Al. C. Be. D. Fe.
Câu 13: Cho các polime sau: bông, tơ tằm, thủy tinh hữu cơ và poli(vinyl clorua). Số polime thiên nhiên là
A. 1. B. 4. C. 3. D. 2.
Câu 14: Thủy phân hoàn toàn tinh bột trong dung dịch axit vô cơ loãng, thu được chất hữu cơ X có khả năng tham gia phản ứng tráng bạc. Tên gọi của X là
A. saccarozơ. B. fructozơ C. glucozơ. D. ancol etylic.
Câu 15: Trong công nghiệp, một lượng lớn chất béo dùng để sản xuất
A. ancol metylic và fructozơ. B. xà phòng và glucozơ.
C. glixerol và xà phòng. D. ancol metylic và xà phòng.
Câu 16: Công thức hóa học của metyl axetat là
A. C2H5COOCH3. B. CH3COOC2H5. C. CH3COOCH3. D. HCOOCH3.
Câu 17: Nhóm các kim loại đều có thể được điều chế bằng phương pháp thủy luyện là
A. Ba, Au. B. Al, Cr. C. Mg, Cu. D. Cu, Ag.
Câu 18: Quặng sắt pirit có thành phần chính là
A. Fe3O4. B. Fe2O3. C. FeS2. D. FeCO3.
Câu 19: Cho 16,1 gam hỗn hợp X gồm CaCO3 và MgCO3 (có tỉ lệ mol 1:1) tan hết trong dung dịch HCl dư, thu được V lít (đktc) khí CO2. Giá trị của V là
A. 2,94. B. 1,96. C. 3,92. D. 7,84.
Câu 20: Chất nào sau đây có nhiều trong thành phần của dầu thực vật?
A. glucozơ. B. axit axetic. C. triolein. D. etyl axetat.
Câu 21: Thủy tinh hữu cơ Plexiglas là một chất dẻo, cứng, trong suốt, bền với nhiệt, với nước, axit, bazơ nhưng bị hòa tan trong benzen, ete. Thủy tinh hữu cơ được dùng để làm kính máy bay, ô tô, kính bảo hiểm, đồ dùng gia đình... Thủy tinh hữu cơ có thành phần hóa học chính là polime nào sau đây?
A. Poli(phenol fomandehit). B. Poli(vinyl axetat).
C. Poli(vinyl clorua). D. Poli(metyl metacrylat).
Câu 22: Dung dịch chất nào sau đây đổi màu quỳ tím sang xanh?
A. Glyxin. B. Lysin. C. Alanin. D. Valin.
Câu 23: Phương trình hóa học nào sau đây được viết không đúng?
A. Fe(OH)2 + 2HCl → FeCl2 + 2H2O. B. 2Al + 6HCl → 2AlCl3 + 3H2.
C. Cu + 2FeCl3 → 2FeCl2 + CuCl2. D. 2Ag + 2HCl → 2AgCl + H2.
Câu 24: Khi phản ứng với dung dịch HCl, crom tạo thành sản phẩm muối có công thức hóa học là
A. CrCl6. B. CrCl4. C. CrCl3. D. CrCl2.
Câu 25: Cho 3,06 gam hỗn hợp bột X gồm Fe và Mg vào 100ml dung dịch Cu(NO3)2. Phản ứng xong, thu được 4,14 gam chất rắn và dung dịch Y. Thêm dung dịch NaOH dư vào dung dịch Y, lọc kết tủa, rửa sạch, sấy khô và nung trong không khí ở nhiệt độ cao đến khối lượng không đổi thì thu được 2,7 gam chất rắn. Nồng độ mol của dung dịch Cu(NO3)2 là
A. 0,25M. B. 0,45M. C. 0,35M. D. 0,3M.
Câu 26: Cho 7,5 gam glyxin phản ứng hết với dung dịch NaOH. Phản ứng xong, khối lượng muối thu được là
A. 9,8 gam. B. 9,9 gam. C. 11,5 gam. D. 9,7 gam.
Câu 27: Tiến hành các thí nghiệm sau:
(a) Cho crom vào cốc có chứa axit sunfuric đậm đặc, nguội.
(b) Cho dung dịch axit sunfuric loãng vào cốc chứa dung dịch kali cromat.
(c) Cho kẽm vào cốc có chứa dung dịch crom (III) clorua.
(d) Cho crom (III) oxit vào cốc có chứa dung dịch NaOH loãng ở nhiệt độ thường.
Số thí nghiệm có xảy ra phản ứng hóa học là
A. 4. B. 3. C. 1. D. 2.
Câu 28: Hỗn hợp X gồm Fe3O4 và CuO. Cho 25,4 gam X phản ứng với CO nung nóng, sau một thời gian thu được hỗn hợp rắn Y và hỗn hợp khí Z. Cho Z tác dụng với dung dịch Ba(OH)2 dư, thu được 9,85 gam kết tủa. Hòa tan hết Y trong 120 gam dung dịch HNO3 63% đun nóng thu được dung dịch T và 3,92 lít (đktc) khí NO2 (sản phẩm khử duy nhất). Cho V (lít) dung dịch NaOH 1M vào dung dịch T, phản ứng hoàn toàn tạo ra kết tủa với khối lượng lớn nhất. Phần trăm khối lượng Fe3O4 và giá trị V nhỏ nhất là
A. 68,5% và 1,025. B. 68,5% và 0,525. C. 20,54% và 1,025. zzzD. 20,54% và 0,525.
Câu 29: Hấp thụ hoàn toàn 7,84 lít (đktc) CO2 vào 200ml dung dịch hỗn hợp NaOH 1M và KOH xM. Sau khi phản ứng kết thúc, làm bay hơi dung dịch được 33,7 gam chất rắn. Cho rằng quá trình làm bay hơi dung dịch, các chất không có sự biến đổi về mặt hóa học. Giá trị của x là
A. 0,5. B. 1,0. C. 1,5. D. 1,8.
Câu 30: Cho hỗn hợp gồm 32,0 gam Fe2O3; 21,6 gam Ag và 32,0 gam Cu vào dung dịch HCl, thu được dung dịch X và 52,0 gam chất rắn không tan Y. Lọc bỏ Y, cho dung dịch AgNO3 dư vào dung dịch X thì thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 174,90. B. 129,15. C. 177,60. D. 161,55.
Câu 31: Trong cây xanh, phản ứng quang hợp xảy ra như sau:
6nCO2 + 5nH2O ![]() (C6H10O5)n + 6nO2
(C6H10O5)n + 6nO2
Cho rằng quá trình quang hợp đã tạo ra 729 gam tinh bột thì thể tích không khí (đktc) cần thiết ít nhất là (giả sử khí cacbonic chiếm tỉ lệ 0,05% thể tích không khí và quá trình quang hợp đạt hiệu suất 100%)
A. 201.600 lít. B. 1.209.600 lít. C. 604,8 lít. D. 1.290.600 lít.
Câu 32: Cho các phát biểu sau:
(a) Thủy phân hoàn toàn vinyl axetat bằng dung dịch NaOH, thu được natri axetat và andehit fomic.
(b) Polietilen được điều chế bằng phản ứng trùng hợp propilen.
(c) Ở điều kiện thường, trimetyl amin là chất khí.
(d) Xenlulozơ thuộc loại polisaccarit.
(e) Ở điều kiện thích hợp, triolein tham gia phản ứng cộng hợp H2.
Số phát biểu đúng là
A. 2. B. 5. C. 3. D. 4.
Câu 33: Thủy phân triglixerit X trong dung dịch NaOH, thu được hỗn hợp 3 muối gồm: natri oleat, natri stearat và natri linoleat. Khi đốt cháy hoàn toàn a mol X, thu được b mol CO2 và c mol H2O. Mối liên hệ giữa a, b, c là
A. b – c = 4a. B. b – c = 6a. C. b = c – a. D. b – c = 5a.
Câu 34: Điện phân (với điện cực trơ và màng ngăn) dung dịch chứa 0,05 mol CuSO4 và x mol KCl bằng dòng điện có cường độ 5A, sau một thời gian, thấy khối lượng dung dịch giảm 9,025 gam. Dung dịch thu được tác dụng với Al dư, phản ứng giải phóng 1,68 lít (đktc) khí H2. Biết các phản ứng xảy ra hoàn toàn. Thời gian đã điện phân là
A. 3860 giây. B. 5790 giây. C. 4825 giây. D. 2895 giây.
Câu 35: Hỗn hợp Q gồm 3 peptit X, Y và Z đều mạch hở và được tạo bởi alanin và glyxin; X và Y là đồng phân; MY < MZ; trong Q có tỉ lệ khối lượng mO : mN = 52 : 35. Đun nóng hết 0,3 mol Q trong dung dịch KOH, cô cạn dung dịch sau phản ứng thu được 120 gam chất rắn khan T. Đốt cháy hết T, thu được 71,76 gam K2CO3. Biết tổng số nguyên tử oxi trong 3 peptit bằng 17. Phần trăm khối lượng của Z trong Q gần nhất với giá trị nào sau đây?
A. 16,25%. B. 33,71%. C. 15,45%. D. 16,35%.
Câu 36: Cho 5,4 gam Mg tác dụng với dung dịch hỗn hợp Cu(NO3)2 và H2SO4 đun nóng, khuấy đều đến khi phản ứng xảy ra hoàn toàn, thu được dung dịch X và 1,344 lít (đktc) hỗn hợp khí Y gồm hai khí không màu, trong đó có một khí hóa nâu ngoài không khí và 2,64 gam hỗn hợp hai kim loại có cùng số mol. Biết tỉ khối của Y đối với H2 là 8. Khối lượng muối tạo thành trong dung dịch X gần nhất với giá trị nào sau đây?
A. 19,90 gam. B. 19,5 gam. C. 25,5 gam. D. 24,0 gam.
Câu 37: Từ m gam glucozơ (có chứa 5% tạp chất) cho lên men rượu với hiệu suất 90%. Toàn bộ lượng CO2 tạo ra cho hấp thụ vào dung dịch nước vôi trong thu được 11 gam kết tủa, khối lượng dung dịch sau phản ứng giảm 4,4 gam so với khối lượng dung dịch ban đầu. Giá trị của m gần nhất với giá trị nào sau đây?
A. 13,50. B. 15,80. C. 12,80. D. 12,15.
Câu 38: Hỗn hợp X gồm các chất Y (C5H14N2O4) và chất Z (C4H8N2O3). Trong đó, Y là muối của axit hai chức, Z là đipeptit mạch hở. Cho 21,5 gam X tác dụng với dung dịch NaOH dư, đun nóng, thu được 0,1 mol hỗn hợp khí đều làm xanh quỳ tím ẩm, tỉ khối của mỗi khí so với không khí đều lớn hơn 1. Mặt khác 21,5 gam X tác dụng với dung dịch HCl dư đun nóng thu được m gam chất hữu cơ. Giá trị của m là
A. 32,45. B. 37,90. C. 34,25. D. 28,80.
Câu 39: Este X mạch hở có công thức phân tử là CxHyO2. Trong phân tử X, cacbon chiếm 50% về khối lượng. Thủy phân hoàn toàn m gam X trong 200 ml dung dịch NaOH 2M, đun nóng, cô cạn dung dịch sau phản ứng thu được 24,4 gam chất rắn khan. Giá trị của m là
A. 21,6. B. 25,2. C. 23,4. D. 18,0.
Câu 40: Cho dung dịch X gồm Al2(SO4)3, H2SO4 và HCl. Cho dung dịch NaOH 0,1M vào dung dịch X, kết quả thí nghiệm được biểu diễn bằng đồ thị sau:
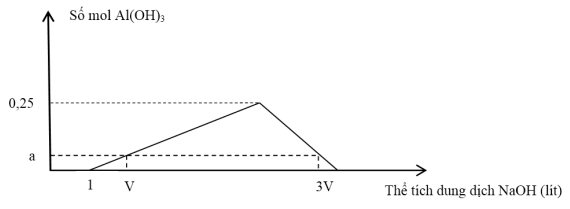
Giá trị của V và a lần lượt là:
A. 3,4 và 0,08. B. 2,5 và 0,07. C. 3,4 và 0,07. D. 2,5 và 0,08.
----------- HẾT ----------
Lưu ý: Học sinh được sử dụng Bảng tuần hoàn; Giám thị không giải thích gì thêm.
Giám thị 1: ...... ............................................. Chữ ký: ...................
Giám thị 2: ..................................................... Chữ ký. ...................