Lý thuyết Hóa học 10 bài 7 CTST
Chúng tôi xin giới thiệu bài Lý thuyết Hóa lớp 10 bài 7: Định luật tuần hoàn - Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học được VnDoc sưu tầm và tổng hợp các câu hỏi lí thuyết và trắc nghiệm có đáp án đi kèm nằm trong chương trình giảng dạy môn Hóa học lớp 10 sách CTST. Mời quý thầy cô cùng các bạn tham khảo tài liệu dưới đây.
Định luật tuần hoàn - Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
A. Lý thuyết Hóa học 10 bài 7
1. Định luật tuần hoàn
- Tìm hiểu sự biến đổi cấu hình electron nguyên tử của các nguyên tố nhóm A và định luật tuần hoàn
Bảng 7.1. Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm A
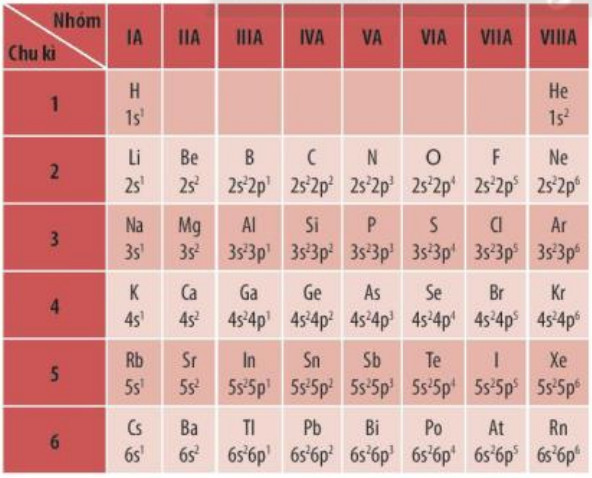
- Sự biến đổi tuần hoàn về cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố khi điện tích hạt nhân tăng dần chính là nguyên nhân của sự biến đổi tuần hoàn về tính chất của các nguyên tố, cũng như hợp chất của chúng.
| Định luật tuần hoàn: Tính chất của các nguyên tố và đơn chất, cũng như thành phần và tính chất của các hợp chất tạo nên từ các nguyên tố đó biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử. |
|---|
2. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
- Trình bày mối quan hệ giữa cấu hình electron, vị trí và tính chất của các nguyên tố trong bảng tuần hoàn
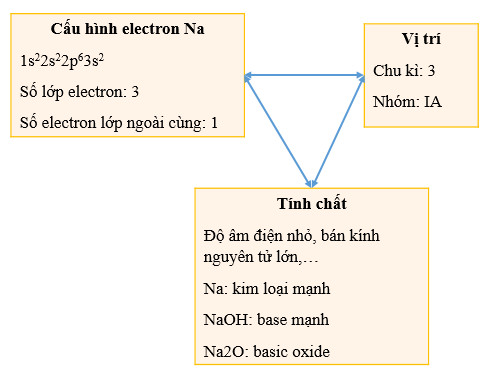
Hình 7.1. Mối quan hệ vị trí, cấu hình electron và tính chất của sodium
| Khi biết vị trí của một nguyên tố trong bảng tuần hoàn, có thể suy ra cấu tạo nguyên tử của nguyên tố đỏ và ngược lại. Từ đó, có thể suy ra những tính chất hoá học cơ bản của nó. |
|---|
B. Bài tập minh họa
Bài 1: Fluorine được sử dụng làm chất oxi hóa cho nhiên liệu lỏng dùng trong tên lửa. Fluorine (F) là một nguyên tố hóa học có số hiệu nguyên tử bằng 9, thuộc chu kì 2, nhóm VIIA. Từ vị trí của fluorine trong bảng tuần hoàn, có thể dự đoán được tính chất hóa học cơ bản của fluorine không? Khả năng phản ứng của fluorine như thế nào?

Hướng dẫn giải
- Fluorine thuộc chu kì 2, nhóm VIIA
→ Có 7 electron ở lớp ngoài cùng
→ Có xu hướng nhận thêm 1 electron tạo thành F- có cấu hình electron bền vững
→ Fluorine có tính phi kim, tính oxi hóa mạnh và có khả năng phản ứng mãnh liệt vì có độ âm điện lớn
Bài 2: Dựa vào vị trí của nguyên tố Mg (Z = 12) trong bảng tuần hoàn.
a) Hãy nêu các tính chất sau của nguyên tố:
- Tính kim loại hay tính phi kim.
- Hóa trị cao nhất trong hợp chất với oxi.
- Công thức của oxit cao nhất, của hiđroxit tương ứng và tính chất của nó.
b) So sánh tính chất hóa học của nguyên tố Mg (Z = 12) với Na (Z = 11) và Al (Z = 13).
Hướng dẫn giải
a) Cấu hình electron của nguyên tử Mg: 1s22s22p63s2.
Mg có 2e ở lớp ngoài cùng nên thể hiện tính kim loại, hóa trị cao nhất với oxi là II, chất MgO là oxit bazơ và Mg(OH)2 là bazơ.
b) Na:1s22s22p63s1.
Mg: 1s22s22p63s2
Al: 1s22s22p63s23p1
- Có 1, 2, 3 electron ở lớp ngoài cùng nên đều là kim loại.
- Tính kim loại giảm dần theo chiều Na, Mg, Al.
- Tính bazơ giảm dần theo chiều NaOH, Mg(OH)2, Al(OH)3.
Bài 3: Dựa vào quy luật biến đổi tính kim loại, tính phi kim của các nguyên tố trong bảng tuần hoàn, hãy trả lời các câu hỏi sau:
a) Nguyên tố nào là kim loại mạnh nhất? Nguyên tố nào là phi kim mạnh nhất?
b) Các nguyên tố kim loại được phân bố ở khu vực nào trong bảng tuần hoàn?
c) Các nguyên tố phi kim được phân bố ở khu vực nào trong bảng tuần hoàn?
d) Nhóm nào gồm những nguyên tố kim loại điển hình? Nhóm nào gồm hầu hết những nguyên tố phi kim điển hình?
e) Các nguyên tố khí hiếm nằm ở khu vực nào trong bảng tuần hoàn?
Hướng dẫn giải
a) Fr là kim loại mạnh nhất. F là phi kim mạnh nhất.
b) Các kim loại được phân bố ở khu vực bên trái trong bảng tuần hoàn.
c) Các phi kim được phân bố ở khu vực bên phải trong bảng tuần hoàn.
d) Nhóm IA gồm những kim loại mạnh nhất. Nhóm VIIA gồm những phi kim mạnh nhất.
e) Các khí hiếm nằm ở nhóm VIIIA ở khu vực bên phải trong bảng tuần hoàn.
C. Trắc nghiệm Hóa học 10 bài 7
------------------------------
Như vậy, VnDoc.com đã gửi tới các bạn Lý thuyết Hóa học 10 bài 7: Định luật tuần hoàn - Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học CTST. Ngoài ra, các em học sinh có thể tham khảo môn Hóa 10 Cánh Diều, Lý 10 Cánh Diều và Toán 10 Chân trời sáng tạo tập 1, Sinh 10 Chân trời sáng tạo đầy đủ khác.
