Đề thi học sinh giỏi lớp 10 THPT tỉnh Vĩnh Phúc năm 2012 môn Hóa học - Có đáp án
Vndoc.com xin giới thiệu đến các bạn: Đề thi học sinh giỏi lớp 10 THPT tỉnh Vĩnh Phúc năm 2012 môn Hóa học - Có đáp án.
Đề thi học sinh giỏi lớp 10 môn Hóa học:
SỞ GIÁO DỤC VÀ ĐÀO TẠO
|
KỲ THI CHỌN HSG LỚP 10 NĂM HỌC 2011-2012
|
Bài 1 (1,5 điểm).
Cho hợp chất X có dạng AB2, có tổng số proton trong X bằng 18 và có các tính chất sau:
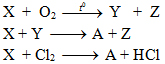
1) Xác định X và hoàn thành các phương trình phản ứng.
2) Viết các phương trình phản ứng xảy ra (nếu có) khi cho X lần lượt tác dụng với: dung dịch nước clo; dung dịch FeCl3; dung dịch Cu(NO3)2; dung dịch Fe(NO3)2
Bài 2 (1,0 điểm).
X và Y là các nguyên tố thuộc phân nhóm chính, đều tạo hợp chất với hiđro có dạng RH (R là kí hiệu của nguyên tố X hoặc Y). Gọi A và B lần lượt là hiđroxit ứng với hóa trị cao nhất của X và Y. Trong B, Y chiếm 35,323% khối lượng. Trung hòa hoàn toàn 50 gam dung dịch A 16,8% cần 150 ml dung dịch B 1M. Xác định các nguyên tố X và Y.
Bài 3 (1,0 điểm).
Hỗn hợp A gồm Cu và Fe trong đó Cu chiếm 70% về khối lượng. Cho m gam A phản ứng với 0,44 mol HNO3 trong dung dịch, thu được dung dịch B, phần rắn C có khối lượng 0,75m (gam) và 2,87 lít hỗn hợp khí NO2 và NO đo ở (1,2 atm, 270C).
Biết các phản ứng đều xảy ra hoàn toàn, trong B không có muối amoni.
Tính khối lượng muối trong dung dịch B và tính khối lượng m.
Bài 4 (1,5 điểm).
1) Cho 29,6 gam hỗn hợp gồm Cu và Fe tác dụng với oxi không khí, sau phản ứng thu được 39,2 gam hỗn hợp A gồm ( CuO, FeO, Fe2O3 và Fe3O4). Hòa tan hoàn toàn A trong dung dịch H2SO4 loãng, dư.
a) Tính số mol H2SO4 đã tham gia phản ứng
b) Tính khối lượng muối sunfat thu được.
2) Khử hoàn toàn 2,552 gam một oxit kim loại cần 985,6 ml H2 (đktc), lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 739,2 ml H2 (đktc). Xác định công thức của oxit kim loại đã dùng?
Bài 5 (1,0 điểm).
Hoàn thành các phương trình phản ứng sau theo phương pháp thăng bằng electron.
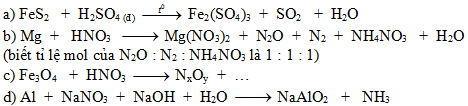
Bài 6 (1,5 điểm).
Sục Cl2 vào dung dịch KOH loãng thu được dung dịch A, hòa tan I2 vào dung dịch KOH loãng thu được dung dịch B (tiến hành ở nhiệt độ phòng).
1) Viết phương trình hóa học xảy ra.
2) Viết phương trình hóa học xảy ra khi cho lần lượt các dung dịch: hỗn hợp HCl và FeCl2, Br2, H2O2, CO2 vào dung dịch A (không có Cl2 dư, chỉ chứa các muối).
Bài 7 (1,5 điểm)
a) Cho 2,25 gam hỗn hợp A gồm Al, Fe, Cu tác dụng với dung dịch HCl dư, sau khi phản ứng kết thúc thu được 1344 ml (đktc) khí và còn lại 0,6 gam chất rắn không tan. Tính % khối lượng mỗi kim loại trong A.
b) Hấp thụ hoàn toàn 1,344 lít SO2 ( đktc) vào 13,95 ml dung dịch KOH 28%, có khối lượng riêng là 1,147g/ml. Hãy tính nồng độ phần trăm các chất có trong dung dịch sau phản ứng
Bài 8 (1 điểm).
Khi thêm 1 gam MgSO4 khan vào 100 gam dung dịch MgSO4 bão hoà ở 200C, thấy tách ra một tinh thể muối kết tinh trong đó có 1,58 gam MgSO4. Hãy xác định công thức của tinh thể muối ngậm nước kết tinh. Biết độ tan cuả MgSO4 ở 200C là 35,1 gam trong 100 gam nước.
