Hóa học 11 Bài 21: Công thức phân tử hợp chất hữu cơ
Lý thuyết Hóa học 11 Bài 21: Công thức phân tử hợp chất hữu cơ
VnDoc.com xin gửi tới bạn đọc bài viết Hóa học 11 Bài 21: Công thức phân tử hợp chất hữu cơ. Mời các bạn cùng tham khảo chi tiết bài viết dưới đây nhé.
I. Công thức đơn giản nhất
1. Định nghĩa
Công thức đơn giản nhất là công thức biểu thị tỉ lệ tối giản về số nguyên tử của các nguyên tố trong phân tử.
2. Cách thiết lập công thức đơn giản nhất
Thiết lập công thức đơn giản nhất của hợp chất hữu cơ CxHyOz là tìm tỉ lệ:
![]() \(x:y:z = n_{C} : n_{H} : n_{O} = \frac{m_{C} }{12,0} : \frac{m_{H} }{1,0} : \frac{m_{O} }{16,0}\)
\(x:y:z = n_{C} : n_{H} : n_{O} = \frac{m_{C} }{12,0} : \frac{m_{H} }{1,0} : \frac{m_{O} }{16,0}\)
dưới dạng tỉ lệ giữa các số nguyên tối giản.
Trong thực tế, ta thường xác định công thức đơn giản nhất dựa vào phần trăm khối lượng các nguyên tố như sau:
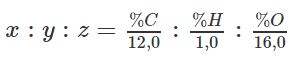
Sau đó biến đổi về tỉ lệ giữa các số nguyên tối giản.
Thí dụ: Kết quả phân tích nguyên tố hợp chất X cho biết %C = 40,00%; %H = 6,67%, còn lại là oxi. Lập công thức đơn giản nhất của X.
Giải:
Gọi công thức phân tử của X là CxHyOz (với x, y, z nguyên dương).
Từ kết quả phân tích định lượng, lập được hệ thức:
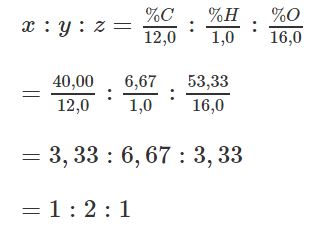
Vậy công thức đơn giản nhất của X là CH2O.
II. Công thức phân tử
1. Định nghĩa
Công thức phân tử là công thức biểu thị số lượng nguyên tử của mỗi nguyên tố trong phân tử.
2. Quan hệ giữa công thức phân tử và công thức đơn giản nhất
- Số nguyên tử của mỗi nguyên tố trong công thức phân tử là số nguyên lần số nguyên tử của nó trong công thức đơn giản nhất.
- Trong nhiều trường hợp, công thức phân tử cũng chính là công thức đơn giản nhất.
Thí dụ: Ancol etylic C2H6O, metan CH4,...
- Một số chất có công thức phân tử khác nhau nhưng có cùng một công thức đơn giản nhất.
Thí dụ: Axetilen C2H2 và benzen C6H6; axit axetic C2H4O2 và glucozơ C6H12O6, …
3. Cách thiết lập công thức phân tử hợp chất hữu cơ
a, Dựa vào thành phần phần trăm khối lượng các nguyên tố
Xét sơ đồ:
CxHyOz ![]() \(\rightarrow\) xC + yH + xO
\(\rightarrow\) xC + yH + xO
Khối lượng: M (g) 12,0.x (g) 1,0.y (g) 16,0.z (g)
Thành phần phần trăm khối lượng: 100% % C % H % O
Suy ra:
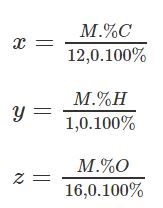
Thí dụ: Phenolphtalein - chất chỉ thị màu dùng nhận biết dung dịch bazơ - có phần trăm khối lượng C, H và O lần lượt bằng 75,47%, 4,35% và 20,18%. Khối lượng mol phân tử của phenolphtalein bằng 318,0 g/mol. Hãy lập công thức phân tử của phenolphtalein.
Giải:
Ta thấy %C + %H + %O = 100%
⇒ Thành phần phân tử phenolphtalein gồm ba nguyên tố C, H, O nên ta đặt công thức phân tử là CxHyOz (với x, y, z nguyên dương).
Ta có:
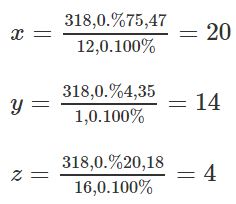
Công thức phân tử của phenolphtalein là C20H14O4.
b, Thông qua công thức đơn giản nhất
Thí dụ: Chất hữu cơ X có công thức đơn giản nhất CH2O và có khối lượng mol phân tử bằng 60,0 g/mol. Xác định công thức phân tử của X.
Giải:
Công thức phân tử của X là (CH2O)n hay CnH2nOn.
Từ MX = (12,0+2.1,0+16,0).n = 60,0
⇒ n=2
Vậy X có công thức phân tử C2H4O2.
c, Tính trực tiếp theo khối lượng sản phẩm đốt cháy
Thí dụ: Hợp chất Y chứa các nguyên tố C, H, O. Đốt cháy hoàn toàn 0,88 gam Y thu được 1,76 gam CO2 và 0,72 gam H2O. Tỉ khối hơi của Y so với không khí xấp xỉ 3,04. Xác định công thức phân tử của Y.
Giải:
Mϒ= 29,0. 3,04 ≈ 88,0 (g/mol);
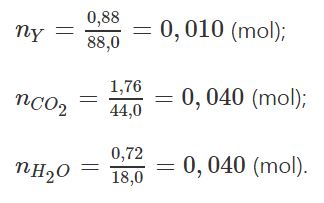
Đặt công thức phân tử của Y là CxHyOz (với x, y, z nguyên dương).
Phương trình hóa học của phản ứng cháy:

VnDoc.com vừa gửi tới bạn đọc bài viết Hóa học 11 Bài 21: Công thức phân tử hợp chất hữu cơ. Hi vọng qua bài viết này bạn đọc có thêm tài liệu để học tập tốt hơn môn Hóa học lớp 11. Mời các bạn cùng tham khảo thêm nội dung Lý thuyết Hóa học 11...
