Bài 12 mối quan hệ giữa các loại hợp chất vô cơ
Bài 12 mối quan hệ giữa các loại hợp chất vô cơ được VnDoc biên soạn, hệ thống lại toàn bộ kiến thức hóa 9 bài 12. Bên cạnh đó là ôn tập tổng hợp lại các tính chất hóa học của hợp chất vô cơ đã được học. Giúp các bạn học sinh nắm được mối quan hệ giữa các hợp chất vô cơ. Mời các bạn tham khảo
A. Mối quan hệ giữa các loại hợp chất vô cơ
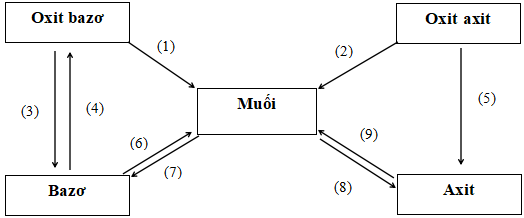
B. Giải Hóa 9 bài 12 Mối quan hệ giữa các loại hợp chất vô cơ
Bài 1 trang 41 sgk Hóa 9
Chất nào trong những thuốc thử sau đây có thể dùng để phân biệt dung dịch natri sunfat và dung dịch natri cacbonat?
a) Dung dịch bari clorua.
b) Dung dịch axit clohiđric.
c) Dung dịch chì nitrat.
d) Dung dịch bạc nitrat.
e) Dung dịch natri hiđroxit.
Hướng dẫn giải bài 1
Thuốc thử phải chọn sao cho khi cho vào Na2SO4 và Na2CO3 phải gây ra hiện tượng khác biệt, dễ nhận thấy.
Không dùng BaCl2 và Pb(NO3)2 vì đều xảy ra phản ứng và tạo kết tủa có màu giống nhau.
Không dùng AgNO3, vì đều xảy ra phản ứng, hiện tượng không khác nhau rõ rệt; Ag2CO3 không tan, Ag2SO4 ít tan và có màu giống nhau.
Không dùng NaOH, vì đều không phản ứng, không có hiện tượng gì. Thuốc thử dùng được là dung dịch HCl ví HCl tác dụng với Na2CO3 có xuất hiện bọt khí và không tác dụng với Na2SO4.
2HCl + Na2CO3 → 2NaCl + CO2↑ H2O.
Bài 2 trang 41 sgk hóa 9
a) Cho các dung dịch sau đây lần lượt phản ứng với nhau từng đôi một, hãy ghi dấu (x) nếu có phản ứng xảy ra, số 0 nếu không có phản ứng.
|
NaOH |
HCl |
H2SO4 |
|
|
CuSO4 |
|
|
|
|
HCl |
|
|
|
|
Ba(OH)2 |
|
|
b) Viết các phương trình hóa học (nếu có).
Hướng dẫn giải bài 2
a) Phản ứng giữa các dung dịch trên đều thuộc loại phản ứng trao đổi, muốn xảy ra được sản phẩm phải có chất không tan, chất khí hoặc H2O.
|
|
NaOH |
HCl |
H2SO4 |
|
CuSO4 |
x |
0 |
0 |
|
HCl |
x |
0 |
0 |
|
Ba(OH)2 |
0 |
x |
x |
b) Các phương trình hóa học:
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2↓
HCl + NaOH → NaCl + H2O
Ba(OH)2 + 2HCl → BaCl2 + 2H2O
Ba(OH)2 + H2SO4 → BaSO4↓ + 2H2O
Bài 3 trang 41 sgk hóa 9
Viết phương trình hóa học cho những chuyển đổi hóa học sau:

Hướng dẫn giải bài 3
a) (1) Fe2(SO4)3 + 3BaCl2 → 2FeCl3 + 3BaSO4↓
(2) FeCl3 + 3NaOH → 3NaCl + Fe(OH)3↓
(3) Fe2(SO4)3 + 6NaOH → 3Na2SO4 + 2Fe(OH)3↓
(4) 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O
(5) 2Fe(OH)3 → Fe2O3 + 3H2O
(6) Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
b) (1) 2Cu + O2 → 2CuO
(2) CuO + H2 → Cu+ H2O
(3) CuO + 2HCl → CuCl2 + H2O
(4) CuCl2 + 2NaOH → Cu(OH)2 ↓ + 2NaCl
(5) Cu(OH)2 + 2HCl → CuCl2 + 2H2O
(6) Cu(OH)2 → CuO + H2O
Bài 4 trang 41 sgk hóa 9
Có những chất: Na2O, Na, NaOH, Na2SO4, Na2CO3, NaCl.
a) Dựa vào mối quan hệ giữa các chất, hãy sắp xếp các chất trên thành một dãy chuyển đổi hóa học.
b) Viết các phương trình hóa học cho dãy chuyển đổi hóa học ở câu a.
Hướng dẫn giải bài 4
a) Dãy chuyển hóa trên có thể là:
Na ![]() \(\overset{+O_{2} }{\rightarrow}\) Na2O
\(\overset{+O_{2} }{\rightarrow}\) Na2O ![]() \(\overset{+H_{2}O }{\rightarrow}\)NaOH
\(\overset{+H_{2}O }{\rightarrow}\)NaOH ![]() \(\overset{+CO_{2}}{\rightarrow}\)Na2CO3
\(\overset{+CO_{2}}{\rightarrow}\)Na2CO3 ![]() \(\overset{+H_{2}SO_{4} }{\rightarrow}\) Na2SO4
\(\overset{+H_{2}SO_{4} }{\rightarrow}\) Na2SO4 ![]() \(\overset{+BaCl_{2} }{\rightarrow}\)NaCl
\(\overset{+BaCl_{2} }{\rightarrow}\)NaCl
b) Các phương trình hóa học:
4Na + O2 → 2Na2O
Na2O + H2O → 2NaOH
2NaOH + CO2 → Na2CO3 + H2O
Na2CO3 + H2SO4 → Na2SO4 + CO2↑ + H2O
Na2CO3 + BaCl2 → 2NaCl + BaSO4
.............................................
Mời các bạn tham khảo một số tài liệu liên quan:
- Hóa học 9 Bài 12: Mối quan hệ giữa các hợp chất vô cơ
- Bảng hệ thống hóa các loại hợp chất vô cơ
- Trắc nghiệm hóa học 9 bài 12
Trên đây VnDoc đã giải thiệu Bài 12 mối quan hệ giữa các loại hợp chất vô cơ tới bạn đọc. Mời các bạn học sinh còn có thể tham khảo các Trắc nghiệm Hóa học 9, Giải sách bài tập Hóa 9, Giải bài tập Hóa học 9 các môn Toán, Văn, Anh, Lý, Địa, Sinh mà chúng tôi đã sưu tầm và chọn lọc. Với tài liệu lớp 9 này giúp các bạn rèn luyện thêm kỹ năng giải đề và làm bài tốt hơn. Chúc các bạn học tốt.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THCS miễn phí trên Facebook: Luyện thi lớp 9 lên lớp 10. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.
