Cho sơ đồ pin Galvani Zn-Cu ở điều kiện chuẩn như hình vẽ sau:
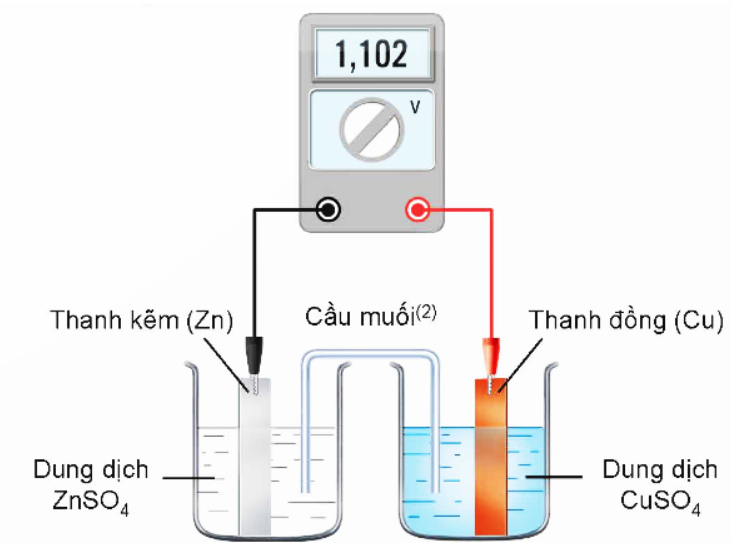
Mỗi phát biểu sau đây là đúng hay sai?
a. Tại cathode của pin xảy ra quá trình Cu → Cu2+ + 2e . Sai||Đúng
b. Thế điện cực chuẩn của cặp Cu2+/Cu có giá trị bằng 1,102 V. Sai||Đúng
c. Dòng điện trong pin có chiều từ điện cực Cu sang điện cực Zn. Sai||Đúng
d. Phản ứng xảy ra trong pin là Zn + Cu2+ → Zn2+ + Cu. Đúng||Sai
Cho sơ đồ pin Galvani Zn-Cu ở điều kiện chuẩn như hình vẽ sau:

Mỗi phát biểu sau đây là đúng hay sai?
a. Tại cathode của pin xảy ra quá trình Cu → Cu2+ + 2e . Sai||Đúng
b. Thế điện cực chuẩn của cặp Cu2+/Cu có giá trị bằng 1,102 V. Sai||Đúng
c. Dòng điện trong pin có chiều từ điện cực Cu sang điện cực Zn. Sai||Đúng
d. Phản ứng xảy ra trong pin là Zn + Cu2+ → Zn2+ + Cu. Đúng||Sai
Phản ứng xảy ra trong pin là Zn + Cu2+ → Zn2+ + Cu.
a. Sai. Ở cathode xảy ra quá trình: Cu2+ + 2e → Cu .
b. Sai. E pin Zn − Cu = 1,102 V .
c. Sai. Các electron trong pin đi từ cực âm (anode, Zn) sang cực dương (cathode, Cu) tức là chúng di chuyển ngược chiều dòng điện.
d. Đúng.