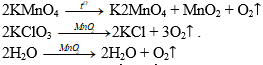Giải bài tập Hóa 10 nâng cao bài 41
Hóa học 10: Oxi
VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa 10 nâng cao bài 41, tài liệu gồm 5 bài tập trang 162 SGK kèm theo lời giải chi tiết sẽ giúp các bạn học sinh giải bài tập Hóa học một cách hiệu quả hơn. Mời các bạn học sinh và thầy cô cùng tham khảo.
Giải bài tập Hóa 10 nâng cao bài 35
Giải bài tập Hóa 10 nâng cao bài 36
Giải bài tập Hóa 10 nâng cao
Bài 1 (trang 162 sgk Hóa 10 nâng cao): Hãy giải thích:
a) Cấu tạo của phân tử oxi.
b) Oxi là phi kim có tính oxi hóa mạnh. Lấy ví dụ minh họa.
Lời giải:
a) Cấu tạo phân tử oxi: Nguyên tử oxi có cấu hình electron ls22s22p4, lớp ngoài cùng có 2 electron độc thân. Hai electron độc thân (ở phân lớp 2p) của mỗi nguyên tử xen phủ vào nhau tạo 2 liên kết cộng hóa trị.
b) Oxi là phi kim có tính oxi hóa mạnh.
- Tác dụng với kim loại: Oxi tác dụng với hầu hết các kim loại (trừ Ag, Au, Pt,...)
3Fe + 2O2 -> Fe3O4;
2Cu + O2 -> 2CuO
- Tác dụng với phi kim: oxi tác dụng với hầu hết các phi kim (trừ halogen)
4P + 5O2 -> 2P2O5
S + O2 -> SO2
- Tác dụng với hợp chất: oxi tác dụng với nhiều chất hữu cơ và vô cơ.
C2H2OH + 3O2 -> 2CO2 + 3H2O;
2H2S + 3O2 -> 2SO2+ 2H2O
Bài 2 (trang 162 sgk Hóa 10 nâng cao): Trình bày những phương pháp điều chế oxi:
a) Trong phòng thí nghiệm.
b) Trong công nghiệp.
Lời giải:
a) Phương pháp điều chế oxi trong phòng thí nghiệm:
b) Phương pháp điều chế oxi trong công nghiệp:
- Từ không khí: Không khí sau khi đã loại bỏ CO2 và hơi nước, được hóa lỏng áp suất 200 atm.
Chưng cất phân đoạn không khí lỏng thu được khí oxi ở -183oC.
Khí oxi được vận chuyển trong những bình thép có thể tích 100 lít (p = 150 atm).
![]()
Bài 3 (trang 162 sgk Hóa học 10 nâng cao): Thêm 3 gam MnO2 vào 197gam hỗn hợp muối KCl và KClO3. Trộn kĩ và đun nóng hỗn hợp đến phản ứng hoàn toàn, thu được chất rắn cân nặng 152gam. Hãy xác định thành phần phần trăm khối lượng của hỗn hợp muối đã dùng.
Lời giải:
![]()
Áp dụng định luật BTKL ta có:
Khối lượng oxi thoát ra: 197 + 3 - 152 = 48 (gam) => nO2=48/32=1,5 (mol)
Từ (1) =>![]() \(n_{KClO_2}\) = 2/3.1,5=1(mol)
\(n_{KClO_2}\) = 2/3.1,5=1(mol)
Khối lượng KClO3 trong hỗn hợp đầu: 1.122,5 = 122,5 (gam)
Khối lượng KCl trong hỗn hợp đầu: 197 - 122,5 = 74,5 (gam)
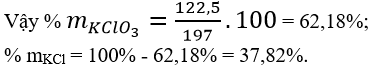
Bài 4 (trang 162 sgk Hóa 10 nâng cao): So sánh thể tích khí oxi thu được (trong cùng điều kiện nhiệt độ và áp suất) khi phân hủy hoàn toàn KMnO4. KClO3, H2O2 trong các trường hợp sau:
a) Lấy cùng khối lượng các chất đem phân hủy.
b) Lấy cùng lượng chất đem phân hủy.
Lời giải:
a) Nếu lấy cùng khối lượng a gam.
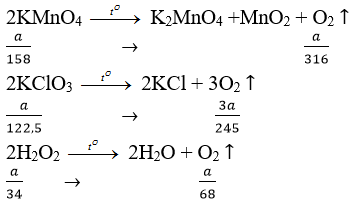
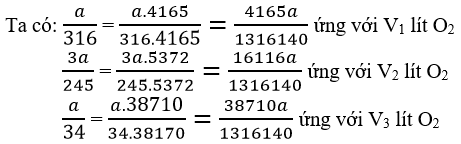
Vậy V3 > V2 > V1
b) Nếu lấy cùng số mol là b: mol
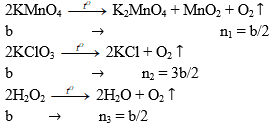
Ta có: n1 = n3 < n2. Vậy V2 = V3 < V2.
Bài 5 (trang 162 sgk Hóa 10 nâng cao): Đốt cháy hoàn toàn m gam cacbon trong V lít oxi (điều kiện tiêu chuẩn), thu được hỗn hợp khí A có tỉ khối đối với oxi là 1,25.
a) Hãy xác định thành phần phần trăm theo thể tích các khí có trong hỗn hợp A.
b) Tính m và V. Biết rằng khi dẫn hỗn hợp khí A vào đựng dung dịch Ca(OH)2 dư tạo thành 6 gam kết tủa trắng.
Lời giải:
a) Ta có:
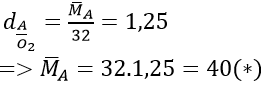
Phương trình phản ứng:
C + O2 -> CO2 (1)
C + CO2 -> 2CO (2)
Bài toán này có thể xảy ra hai trường hợp sau:
Trường hợp 1: Oxi dư (không có phản ứng 2): Hỗn hợp A gồm CO2 và O2 dư.
Thành phần phần trăm các chất trong hỗn hợp về mặt toán học không ảnh hưởng đến số mol hỗn hợp.
Xét 1 mol hỗn hợp A, trong đó X là số mol của CO2 và (1 - x) là số mol của O2 dư.
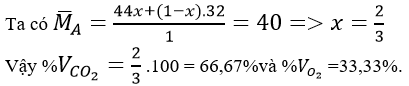
Trường hợp 2: O2 thiếu (có phản ứng 2), hỗn hợp A có CO2 và CO.
Tương tự trên, xét 1 mol hỗn hợp A, trong đó a là số mol của CO2 và (1 - a) là số moi của CO
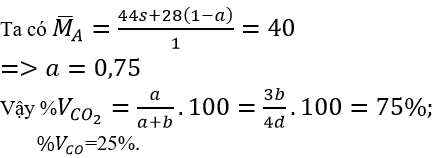
b) Tính m, V:
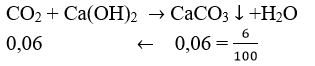
Trường hợp 1: ![]() \(n_{CO_2}\) = 0,06 mol =>
\(n_{CO_2}\) = 0,06 mol => ![]() \(n_{O_2}\) (dư) = 0,03 (mol)
\(n_{O_2}\) (dư) = 0,03 (mol)
Vậy: mC = 0,06.12 = 0,72 gam; ![]() \(V_{O_2}\) = (0,06 + 0,03).22,4 = 2,016 (lít).
\(V_{O_2}\) = (0,06 + 0,03).22,4 = 2,016 (lít).
Trường hợp 2: ![]() \(n_{CO_2}\) = 0,06mol; nCO =
\(n_{CO_2}\) = 0,06mol; nCO = ![]() \(n_{CO_2}\)/3 = 0,02(mol)
\(n_{CO_2}\)/3 = 0,02(mol)
=> nC = ![]() \(n_{CO_2}\) +nCO = 0,06 + 0,02 = 0,08 mol => mC = 0,08.12 = 0,96(g)
\(n_{CO_2}\) +nCO = 0,06 + 0,02 = 0,08 mol => mC = 0,08.12 = 0,96(g)
![]() \(n_{O_2}\)=
\(n_{O_2}\)= ![]() \(n_{CO_2}\) + nCO/2 = 0,06 + 0,01 = 0,07 mol =>
\(n_{CO_2}\) + nCO/2 = 0,06 + 0,01 = 0,07 mol => ![]() \(V_{O_2}\) = 0,07.22,4 = 1,568 (lít).
\(V_{O_2}\) = 0,07.22,4 = 1,568 (lít).
-----------------------------------
Trên đây VnDoc.com đã giới thiệu tới bạn đọc tài liệu: Giải bài tập Hóa 10 nâng cao bài 41. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán 10, Giải bài tập Vật Lí 10, Giải bài tập Sinh học 10, Giải bài tập Hóa học 10 mà VnDoc tổng hợp và đăng tải.