Giải bài tập trang 76 SGK Hóa học lớp 10: Luyện tập - Liên kết hóa học
Giải bài tập Hóa học lớp 10: Liên kết hóa học
VnDoc xin giới thiệu tới bạn đọc tài liệu Giải bài tập trang 76 SGK Hóa học lớp 10: Luyện tập - Liên kết hóa học, với nội dung tài liệu được cập nhật chi tiết và đầy đủ sẽ giúp các bạn học sinh có kết quả cao hơn trong học tập. Mời thầy cô cùng các bạn học sinh cùng tham khảo.
Giải bài tập trang 64 SGK Hóa học lớp 10: Liên kết cộng hóa trị
Giải bài tập trang 70, 71 SGK Hóa học lớp 10: Tinh thể nguyên tử và tinh thể phân tử
Giải bài 1, 2, 3, 4, 5, 6, 7, 8, 9 trang 76 SGK Hóa 10: Liên kết hóa học
Bài 1: a) Viết phương tình biểu diễn sự hình thành các ion sau đây từ các nguyên tử tương ứng:
Na → Na+ ; Cl → Cl-
Mg → Mg2+; S → S2-
Al → Al3+; O → O2-
b) Viết cấu hình electron của các nguyên tử và các ion. Nhận xét về cấu hình electron lớp ngoài cùng của các ion được tạo thành.
Lời giải:
a) Na → Na+ + 1e; Cl + 1e → Cl-
Mg → Mg2+ + 2e; S + 2e → S2-
Al → Al3+ + 3e; O +2e → O2-
b) Cấu hình electron của các nguyên tử và các ion:
11Na : 1s22s22p63s1; Na+: 1s22s22p6
Cấu hình electron lớp ngoài cùng giống Ne.
17Cl : 1s22s22p63s23p5; Cl-: 1s22s22p63s23p6
Cấu hình electron lớp ngoài cùng giống Ar.
12Mg: 1s22s22p63s2; Mg2+: 1s22s22p6
Cấu hình electron lớp ngoài cùng giống Ne.
16S: 1s22s22p63s23p4; S2-: 1s22s22p63s23p6
Cấu hình electron lớp ngoài cùng giống Ar.
13Al: 1s22s22p63s23p1; Al3+: 1s22s22p6
Cấu hình electron lớp ngoài cùng giống Ne.
8O: 1s22s22p4; O2-: 1s22s22p6
Cấu hình electron lớp ngoài cùng giống Ne.
Bài 2: Trình bày sự giống nhau và khác nhau của 3 loại liên kết : Liên kết ion, liên kết cộng hóa trị không có cực và liên kết cộng hóa trị có cực.
Lời giải:
| So sánh | Liên kết ion | Liên kết cộng hóa trị không có cực | Liên kết cộng hóa trị có cực |
| Giống nhau | Các nguyên tử kết hợp với nhau để tạo ra cho mỗi nguyên tử lớp electron ngoài cùng bền vững giống cấu trúc khí hiếm (2e hoặc 8e) | ||
| Khác nhau về cách hình thành liên kết | Cho và nhận electron | Dùng chung e, cặp e không bị lệch | Dùng chung e, cặp e bị lệch về phía nguyên tử có độ âm điện mạnh hơn |
| Khác nhau về nguyên tố tạo nên liên kết | Giữa kim loại và phi kim | Giữa các nguyên tử của cùng một nguyên tố phi kim | Giữa phi kim mạnh và yếu khác |
| Nhận xét | Liên kết cộng hóa trị có cực là dạng trung gian giữa liên kết cộng hóa trị không cực và liên kết ion | ||
Bài 3: Cho dãy oxit sau đây: Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7.
Dựa vào giá trị hiệu độ âm điện của 2 nguyên tử trong phân tử hãy xác định loại liên kết trong từng phân tử oxit (tra giá trị độ âm điện ở bảng 6, trang 45).
Lời giải:
Hiệu độ âm điện của các chất:
Na2O: 2,51 liên kết ion.
MgO: 2,13 liên kết ion.
Al2O3: 1,83 liên kết ion.
SiO2: 1,54 liên kết cộng hóa trị có cực
P2O5: 1,25 liên kết cộng hóa trị có cực
SO3: 0,86 liên kết cộng hóa trị có cực
Cl2O7: 0,28 liên kết cộng hóa trị không cực
Bài 4: a) Dựa vào giá trị độ âm điện (F: 3,98; O: 3,44; Cl: 3,16; N: 3,04) hãy xét xem tính phi kim thay đổi như thế nào của dãy nguyên tố sau : F, O, N, Cl.
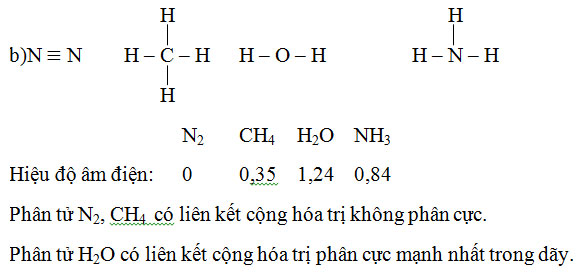
b) Viết công thức cấu tạo của các phân tử sau đây: N2, CH4, H2O, NH3.
Xét xem phân tử nào có liên kết không phân cực, liên kết phân cực mạnh nhất.
Lời giải:
a)
| F | O | Cl | N | |
| Độ âm điện | 3,98 | 3,44 | 3,16 | 3,04 |
Nhận xét: Tính phi kim tăng dần
Bài 5: Một nguyên tử có cấu hình electron 1s22s22p3.
a) Xác định vị trí của nguyên tố đó trong bảng tuần hoàn, suy ra công thức phân tử của hợp chất khí với hiđro.
b) Viết công thức electron và công thức cấu tạo của phân tử đó.
Lời giải:
a) Tổng số electron là 7, suy ra số thứ tự của nguyên tố là 7. Có 2 lớp electron suy ra nguyên tố ở chu kì 2. Nguyên tố p có 5 electron ở lớp ngoài cùng nên thuộc nhóm VA. Đó là nitơ. Công thức phân tử hợp chất với hidro là NH3.
b) Công thức electron và công thức cấu tạo:

Bài 6: a) Lấy ví dụ về tinh thể ion, tinh thể nguyên tử, tinh thể phân tử.
b) So sánh nhiệt độ nóng chảy của các loại tinh thể đó. Giải thích.
c) Tinh thể nào dẫn điện được ở trạng thái rắn? Tinh thể nào dẫn điện được khi nóng chảy và khi hòa tan trong nước?
Lời giải:
a) Tinh thể ion: NaCl; MgO; CsBr; CsCl.
Tinh thể nguyên tử: Kim cương.
Tinh thể phân tử: Băng phiến, iot, nước đá, cacbon đioxit.
b) So sánh nhiệt độ nóng chảy: Lực hút tĩnh điện giữa các ion ngược dấu lớn nên tinh thể ion rất bền vững. Các hợp chất ion đều khá rắn,khó bay hơi,khó nóng chảy.
Lực liên kết cộng hóa trị trong tinh thể nguyên tử rất lớn, vì vậy tinh thể nguyen tử đều bền vững, khá cững, khó nóng chảy, khó bay hơi.
Trong tinh thể phân tử các phân tử hút nhau bằng lực tương tác yếu giữa các phân tử. Vì vây tinh thể phân tử dễ nóng chảy, dễ bay hơi.
c) Không có tinh thể nào có thể dẫn điện ở trạng thái rắn. Tinh thể dẫn điện được nóng chảy và khi hòa tan trong nước là: tinh thể ion.
Bài 7: Xác định điện hóa trị của các nguyên tố nhóm VIA, VIIA trong các hợp chất với các nguyên tố nhóm IA.
Điện hóa trị của các nguyên tố nhóm VIA, VIIA, trong các hợp chất vời nguyên tố nhóm IA là:
Lời giải
Các nguyên tố kim loại thuộc nhóm IA có số electron ở lớp ngoài cùng là 1, có thể nhường 1 electron này nên có điện hóa trị 1+.
Các nguyên tố phi kim thuộc nhóm VIA, VIIA có 6,7 electron ở lớp ngoài cùng, có thể nhận thêm 2 hay 1 electron vào lớp ngoài cùng nên có điện hóa trị 2- hay 1-.
Bài 8: a) Dựa vào vị trí của các nguyên tố trong bảng tuần hoàn, hãy nêu rõ trong các nguyên tố sau đây những nguyên tố nào có cùng cộng hóa trị trong các oxit cao nhất:
Si, P, Cl, S, C, N, Se, Br.
b) Những nguyên tố nào sau đây có cùng cộng hóa trị trong các hợp chất khí với hiđro.
P, S, F, Si, Cl, N, As, Te.
Lời giải:
a) Những nguyên tố có cùng cộng hóa trị trong các oxit cao nhất:
RO2 R2O5 RO3 R2O7.
Si, C, P, N, S, Se, Cl, Br.
b) Những nguyên tố có cùng cộng hóa trị trong hợp chất khí với hiđro:
RH4 RH3 RH2 RH.
Si, N, P, As, S, Te, F, Cl.
Bài 9: Xác định số oxi hóa của Mn, Cr, Cl, P, N, S, C, Br:
a) Trong phân tử: KMnO4, Na2Cr2O7, KClO3, H3PO4.
b) Trong ion: NO3-, SO42-, CO32-, Br-, NH4+.
Lời giải:
a) Trong phân tử
Mn: +7.
Cr: +6.
Cl: +5.
P: +5.
b) Trong ion:
NO3-: N có số oxi hóa là 5+.
SO42-: S có số oxi hóa là 6+.
CO32-: C có số oxi hóa là 4+.
Br-: Br có số oxi hóa là -1.
NH4+: N có số oxi hóa là -3.
---------------------------------------------
Trên đây VnDoc.com đã giới thiệu tới bạn đọc tài liệu: Giải bài tập trang 76 SGK Hóa học lớp 10: Luyện tập - Liên kết hóa học. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Hóa học lớp 10, Thi thpt Quốc gia môn Văn, Thi thpt Quốc gia môn Lịch sử, Thi thpt Quốc gia môn Địa lý, Thi thpt Quốc gia môn Toán, đề thi học kì 1 lớp 11, đề thi học kì 2 lớp 11 mà VnDoc tổng hợp và đăng tải.