Đề thi thử tốt nghiệp THPT 2025 môn Hóa bám sát đề minh họa - Đề 35
Thi THPT Quốc gia 2025
Lớp:
THPT Quốc gia
Môn:
Hóa Học
Dạng tài liệu:
Đề thi
Loại:
Tài liệu Lẻ
Loại File:
Word + PDF
Phân loại:
Tài liệu Tính phí
PHÁT TRIỂN TỪ ĐỀ MINH HỌA
ĐỀ 35
ĐỀ ÔN THI TỐT NGHIỆP THPT 2025
MÔN: HÓA
Thời gian: 50 phút
Phần I. Câu trắc nghiệm nhiều phương án lựa chọn.
Thí sinh trả lời từ câu 1 đến câu 18. Với mỗi câu hỏi, thí sinh chỉ chọn một phương án.
Câu 1: Kim cương là một dạng thù hình được biết đến nhiều nhất của nguyên tố carbon. Kim cương có
độ cứng rất cao, độ khúc xạ cực tốt nên được ứng dụng trong các ngành công nghiệp và đặc biệt
làm đồ trang sức có giá trị kinh tế rất cao. Nguyên tử của nguyên tố carbon có số hiệu nguyên tử
là 6 và số khối là 12. Tổng số hạt proton, electron và neutron trong nguyên tử carbon là
A. 38. B. 28. C. 18. D. 49.
Câu 2: Cho các phát biểu sau:
(a) Thực phẩm bảo quản trong tủ lạnh sẽ giữ được lâu hơn.
(b) Hầm xương bằng nồi áp suất sẽ nhanh nhừ hơn.
(c) Bệnh nhân dễ hô hấp hơn khi dùng oxygen từ bình chứa khí oxygen so với từ không khí.
Các yếu tố chính ảnh hưởng đến tốc độ phản ứng trong các quá trình trên lần lượt là
A. nhiệt độ, áp suất, nồng độ. B. nhiệt độ, nhiệt độ, nồng độ.
C. áp suất, nhiệt độ, nồng độ. D. nhiệt độ, nồng độ, áp suất.
Câu 3: Alkene CH
3
CH=CHCH
3
có tên là
A. 2–methylprop–2–ene. B. but–2–ene. C. but–1–ene. D. but–3–ene.
Câu 4: Sulfuric acid là một hóa chất quan trọng trong công nghiệp, được dùng để sản suất phân bón, khai
khoáng, chế biến dầu mỏ. Trong công nghiệp sulfuric acid được sản xuất với nồng độ từ 70% đến
98% từ sulfur, bằng quá trình tiếp xúc và thiết bị phản ứng dòng liên tục qua 3 giai đoạn sau đây:
– Giai đoạn 1: Đốt sulfur với không khí khô và sạch tạo ta chất X.
– Giai đoạn 2: Nung X với oxygen dư trong lò tầng ở 450°C–500°C, có V
2
O
5
xúc tác thu được
chất Y.
– Giai đoạn 3: Dùng chất Z để hấp thụ Y, tạo ra chất T rồi cho T kết hợp với lượng nước vứa đủ
tạo ra H
2
SO
4
có nồng độ như yêu cầu sản xuất.
Chất Z và chất T nêu trên lần lượt là:
A. H
2
O và oleum. B. H
2
SO
4
loãng và oleum.
C. H
2
SO
4
đặc và oleum. D. H
2
O và H
2
SO
4
> 98%.
Câu 5: Chất béo là triester của acid béo với
A. methyl alcohol. B. ethylene glycol. C. ethyl alcohol. D. glycerol.
Câu 6: Mỗi đơn vị glucose trong cellulose liên kết với nhau bởi liên kết
A. α–1,6–glycoside. B. α–1,4–glycoside. C. β–1,2–glycoside. D. β–1,4–glycoside.
Câu 7: Cặp chất nào sau đây có thể phân biệt bằng thuốc thử Tollens?
A. Glucose và maltose. B. Tinh bột và cellulose.
C. Saccharose và glucose. D. Glucose và fructose.
Câu 8: Dung dịch methyl amine trong nước làm
A. quì tím không đổi màu. B. quì tím hoá xanh.
C. phenolphtalein hoá xanh. D. phenolphtalein không đổi màu.
Câu 9: Phát biểu nào sau đây không đúng?
A. Thuỷ phân hoàn toàn protein thu được các phân tử α–amino acid.
B. Protein tác dụng với Cu(OH)
2
trong môi trường kiềm tạo dung dịch màu xanh lam.
C. Protein bị đông tụ khi đun nóng ở nhiệt độ cao.
D. Protein tác dụng với nitric acid đặc tạo kết tủa vàng.
Câu 10: Vật liệu nào sau đây được chế tạo từ polymer trùng ngưng?
A. Cao su isoprene. B. Polyethylene. C. Tơ nitron. D. Nylon–6,6.
Câu 11: Trong quá trình mạ vàng (mạ vàng) một vật bằng đồng, người ta dùng cathode là vật bằng đồng,
anode làm bằng vàng, dung dịch điện li là dung dịch muối vàng (AuCl
3
chẳng hạn). Phương trình
hóa học của phản ứng xảy ra ở điện cực âm là:
A. Au
3+
+ 3e → Au. B. Au → Au
3+
+ 3e. C. Cu
2+
+ 2e → Cu. D. Cu → Cu
2+
+ 2e.
Câu 12: Cho E
o
pin(Zn–Cu)
= 1,10V;
2
0
Zn /Zn
E
= –0,76V và
0
Ag /Ag
E
= +0,80V. Suất điện động chuẩn của
pin điện hóa Cu–Ag là
A. 0,46V. B. 0,56V. C. 1,14V. D. 0,34V.
Câu 13: Kim loại nào sau đây có nhiệt độ nóng chảy cao nhất?
A. Au. B. Pt. C. Cr. D. W.
Câu 14: Xét các cặp oxi hóa – khử sau:
Cặp oxi hóa – khử
Al
3+
/Al
Ag
+
/Ag
Mg
2+
/Mg
Fe
2+
/Fe
Thế điện cực chuẩn (V)
–1,676
+0,799
–2,356
–0,44
Kim loại có tính khử mạnh nhất, yếu nhất lần lượt là
A. Mg, Ag. B. Al, Ag. C. Al, Fe. D. Mg, Fe.
Câu 15: Kim loại nào sau đây là kim loại kiềm?
A. K. B. Ba. C. Al. D. Ca.
Câu 16: Dãy gồm các chất đều có thể làm mất tính cứng tạm thời của nước là
A. NaOH, Na
3
PO
4
, Na
2
CO
3
. B. HCl, Ca(OH)
2
, Na
2
CO
3
.
C. KCl, Ca(OH)
2
, Na
2
CO
3
. D. HCl, NaOH, Na
2
CO
3
.
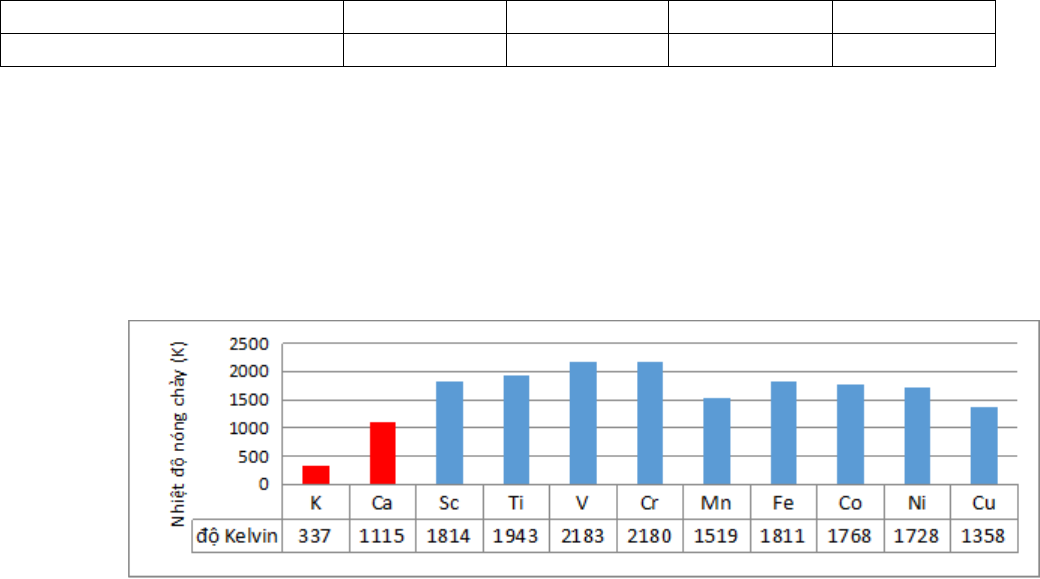
Câu 17: Đồ thị nhiệt độ nóng chảy của các nguyên tố kim loại chu kì 4 (từ nhóm IA đến IB)
Dựa vào đồ thị, nhận định nào đúng trong các nhận định sau:
A. Nhiệt độ nóng chảy của nguyên tố họ s gần bằng kim kim loại chuyển tiếp.
B. Nhiệt độ nóng chảy của nguyên tố họ s cao hơn kim kim loại chuyển tiếp.
C. Nhiệt độ nóng chảy của nguyên tố họ s thấp hơn kim kim loại chuyển tiếp.
D. Nhiệt độ nóng chảy tăng dần theo chiều tăng của điện tích hạt nhân.
Câu 18: Phát biểu nào sau đây đúng?
A. Phức chất aqua là phức chất chứa phối tử NH
3
.
B. Phức chất của kim loại chuyển tiếp đều tan trong dung dịch.
C. Muối CuSO
4
khan màu trắng khi tan vào nước tạo thành dung dịch có màu xanh do tạo thành
phức chất aqua [Cu(H
2
O)
6
1
2+
.
D. Phức chất của kim loại chuyển tiếp đều có màu.
Phần II. Câu trắc nghiệm đúng sai.
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a, b, c, d ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1: Từ xa xưa con người đã biết lên men các loại ngũ cốc hoa quả để tạo ra các đồ uống có cồn (có
chứa ethanol – một alcohol quen thuộc). Ngày nay, alcohol được sử dụng phổ biến trong nhiều
lĩnh vực khác nhau như làm dung môi, nguyên liệu hoá học, nhiên liệu, xăng sinh học.
a) Trong đời sống rượu ethylic (ethanol) được điều chế từ phản ứng lên men cơm gạo, cơm nếp,
hoặc một số loại trái cây.
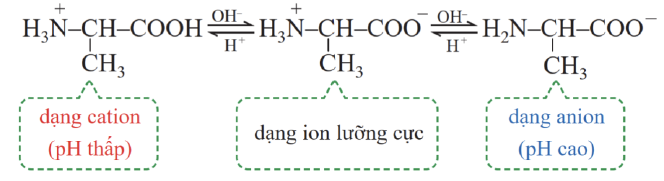
b) Các alcohol thường có nhiệt độ sôi cao hơn so với hydrocarbon và dẫn xuất halogen có phân tử
khối tương đương và dễ tan trong nước.
c) Nhiều vụ ngộ độc do uống phải rượu pha chế từ cồn công nghiệp do có chứa methanol gây độc.
d) Đun nóng isoamylic alcohol và acetic acid với xúc tác sulfuric acid đặc thu được ester có mùi
chuối chín dùng trong công nghiệp thực phẩm.
Câu 2: Trong dụng dịch, tồn tại cân bằng hóa học giữa ion lưỡng cực và các dạng ion tồn tại của amino
acid. Các dạng tồn tại của alanine ở các dạng pH khác nhau.
a) Ở điều kiện thường alanine tồn tại ở thể rắn, có nhiệt độ nóng chảy cao.
b) Alanine phản ứng được với dung dịch NaOH.
c) Trong môi trường acid mạnh alanine tồn tại chủ yếu ở dạng anion di chuyển về phía cực dương
dưới tác dụng của điện trường.
d) Alanine là amino acid không thiết yếu (tự cơ thể tổng hợp được) và rất quan trọng trong việc
hình thành nên protein cho cơ thể.
Câu 3: Ăn mòn hóa học thường xảy ra ở các chi tiết bằng kim loại của máy móc dung trong các nhà máy
sản xuất hóa chất, những bộ phận của thiết bị lò đốt, nồi hơi, các chi tiết của động cơ đốt trong
hoặc những thiết bị thường xuyên phải tiếp xúc với hơi nước, khí oxygen, …
Ví dụ phản ứng xảy ra trong sự ăn mòn hóa học của kim loại iron:
3Fe + 2O
2
0
t
Fe
3
O
4
(1)
3Fe + 4H
2
O
0
t
Fe
3
O
4
+ 4H
2
(2)
Hãy cho biết trong các nhận định sau, nhận định nào đúng, nhận định nào sai?
a) Trong phản ứng (1) và (2), Fe đều đóng vai trò chất khử.
b) Phản ứng (1) và (2) đều thuộc loại phản ứng oxi hóa – khử.
c) Các vật dụng bằng sắt thường dễ bị gỉ, để bảo vệ sắt không bị gỉ người ta thường ngâm sắt
trong giấm ăn hoặc chanh sau khi sử dụng.
d) Để bảo vệ các tàu thép không bị ăn mòn khi giao thông dưới biển, người ta thường áp các tấm
kẽm bên ngoài để tránh hiện tượng ăn mòn.
Câu 4: Kim loại nhóm IA còn gọi là kim loại kiềm, bao gồm các nguyên tố Li, Na, K, Rb và Cs. Kim loại
kiềm và hợp chất của chúng có nhiều ứng dụng trong cuộc sống.
a) Có thể nhận biết hợp chất của kim loại nhóm IA bằng màu ngọn lửa.
b) Quá trình điện phân dung dịch NaCl bão hòa có màng ngăn điện cực được ứng dụng để sản
xuất nước Javel.
c) Trộn một số muối hoặc oxide của các kim loại nhóm IA để tạo màu sắc cho pháo hoa.
d) Sodium carbonate (Na
2
CO
3
) có thể tách loại ion Fe
3+
ra khỏi nước ở dạng kết tủa Fe(OH)
3
trong quá trình xử lí nước nhiễm phèn.
Phần III. Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1: Xét phản ứng 2CO
(g)
CO
2 (g)
+ C
(s)
trong bình kín, nhiệt độ không đổi. Nếu áp suất của hệ tăng
3 lần thì tốc độ phản ứng sẽ tăng bao nhiêu lần?.
Câu 2: Xà phòng và chất giặt rửa tổng hợp đều có tác dụng giặt rửa. Dưới đây là ví dụ về cấu tạo của xà
phòng và chất giặt rửa.
Đề thi thử bám sát đề minh họa 2025 môn Hóa - Đề 35
Đề thi thử tốt nghiệp THPT Quốc gia 2025 môn Hóa bám sát đề minh họa - Đề 35 có đáp án là tài liệu hữu ích giúp bạn đọc có thể trau dồi, luyện tập kiến thức chuẩn bị thật tốt cho kì thi THPT Quốc gia sắp tới. Đề thi được tổng hợp gồm có 18 câu hỏi trắc nghiệm nhiều phương án lựa chọn, 4 câu hỏi trắc nghiệm đúng sai và 6 câu hỏi trắc nghiệm trả lời ngắn. Thí sinh làm bài trong thời gian 50 phút, đề có đáp án và lời giải chi tiết kèm theo. Mời các bạn cùng theo dõi đề thi dưới đây nhé.