Đề thi thử tốt nghiệp THPT 2025 môn Hóa bám sát đề minh họa - Đề 36
Thi THPT Quốc gia 2025
Lớp:
THPT Quốc gia
Môn:
Hóa Học
Dạng tài liệu:
Đề thi
Loại:
Tài liệu Lẻ
Loại File:
Word + PDF
Phân loại:
Tài liệu Tính phí
PHÁT TRIỂN TỪ ĐỀ MINH HỌA
ĐỀ 36
ĐỀ ÔN THI TỐT NGHIỆP THPT 2025
MÔN: HÓA
Thời gian: 50 phút
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn 1 phương án
Câu 1. Ester ethyl formate có mùi thơm của đào và có thành phần trong hương vị của quả mâm xôi, đôi khi
nó còn được tìm thấy trong táo, ester này công thức là
A. CH
3
COOCH
3
. B. HCOOC
2
H
5
. C. HCOOCH=CH
2
. D. HCOOCH
3
.
Câu 2. Phản ứng giữa C
2
H
5
OH với CH
3
COOH (xúc tác H
2
SO
4
đặc, đun nóng) là phản ứng
A. Xà phòng hóa. B. ester hóa. C. Trùng hợp. D. Trùng ngưng
Câu 3. Chất thuộc loại disaccharide là
A. glucose. B. saccharose. C. cellulose. D. fructose.
Câu 4. Tên gọi và bậc của amine có công thức cấu tạo CH
3
-CH
2
-NH
2
A. methylamine, bậc I. B. ethylamine, bậc I. C. ethylamine, bậc II. D. ethaneamine, bậc
II.
Câu 5. Amino acid là hợp chất hữu cơ trong phân tử
A. chứa nhóm carboxyl và nhóm amino. B. chỉ chứa nhóm amino.
C. chỉ chứa nhóm carboxyl. D. chỉ chứa nitrogen hoặc carbon.
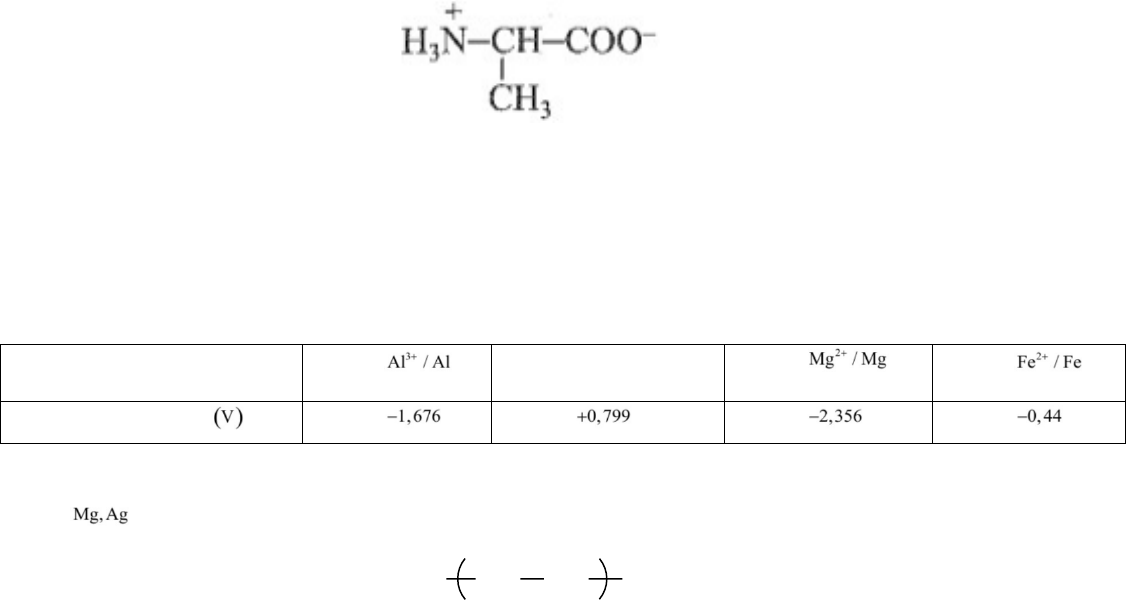
Câu 6. Cho dung dịch chứa amino acid X tồn tại ở dạng ion lưỡng cực:
Đặt dung dịch này trong một điện trường. Khi đó:
A. Chất X sẽ di chuyển về phía cực âm của điện trường.
B. Chất X sẽ di chuyển về phía cực dương của điện trường.
C. Chất X không di chuyển dưới tác dụng của điện trường.
D. Chất X chuyển hoàn toàn về dạng H
2
NCH(R)COOH.
Câu 7. So sánh, phân loại, lựa chọn được các đối tượng, khái niệm hoặc quá trình hoá học theo các tiêu chí
khác nhau.
Xét các cặp oxi hoá - khử sau:
Cặp oxi hoá - khử
Ag / Ag
Thế điện cực chuẩn
Kim loại có tính khử mạnh nhất, yếu nhất lần lượt là
A. . B. Al, Ag. C.Al, Fe D. Mg, Fe
Câu 8. Tên gọi của polymer có công thức cho dưới đây là
CH
2
CH
2
n
A. Cao su buna. B. Cao su buna-S. C. Polyethylene. D. Cao su isoprene .
Câu 9. Cho các chất sau:
CH
2
=CHCl; CH
2
= CH – CH
3
, CH
2
=CH-CH=CH
2
; H
2
N[CH
2
]
5
COOH.
Số chất có khả năng tham gia phản ứng trùng hợp là
A. 3. B. 1. C. 4. D. 2
Câu 10. Một học sinh tiến hành thí nghiệm: Nhúng một thanh đồng vào dung dịch AgNO
3
, sau một lúc
nhúng tiếp một thanh sắt vào dung dịch này đến phản ứng hoàn toàn. Sau khi thí nghiệm kết thúc, học sinh
đó rút ra các kết luận sau :
(1) Dung dịch thu được sau phản ứng có màu xanh nhạt.
(2) Khối lượng thanh đồng bị giảm sau phản ứng.
(3) Khối lượng thanh sắt tăng lên sau phản ứng.
Số kết luận không đúng là
A. 0. B. 1. C. 2. D. 3.
Câu 11. Ở trạng thái cơ bản, cấu hình electron của nguyên tử Mg (Z = 12) là
A. 1s
2
2s
2
2p
6
3s
1
. B. 1s
2
2s
2
2p
6
3s
2
. C. 1s
2
2s
3
2p
6
3s
2
. D. 1s
2
2s
2
2p
7
3s
1
.
Câu 12. Liên kết kim loại là liên kết được hình thành do:
A. Các electron tự do chuyển động quanh vị trí cân bằng giữa nguyên tử kim loại và ion dương kim loại.
B. Sự cho và nhận electron giữa các nguyên tử kim loại.
C. Sự góp chung electron giữa các nguyên tử kim loại.
D. Lực hút tĩnh điện của ion dương kim loại này với nguyên tử kim loại.
Câu 13. Nhiệt tạo thành của một số chất được cho trong bảng sau:
Chất
Na
2
CO
3
(s)
NaHCO
3
(s)
Na
2
O(s)
CO
2
(g)
H
2
O(l)
0
298f
H
(kJ.mol
– 1
)
-1130,70
-950,81
-414,20
-393,51
-285,83
Phát biểu sau đây là sai?
A. Quá trình hình thành muối NaHCO
3
từ các đơn chất thuận lợi về năng lượng hơn so với quá trình hình
thành muối Na
2
CO
3
từ các đơn chất.
B. Giá trị biến thiên enthalpy chuẩn bị của phản ứng
2NaHCO
3
(s)
Na
2
CO
3
(s) + H
2
O(l) + CO
2
(g) là -91,28kJ.
C. Phản ứng Na
2
CO
3
(s)
Na
2
O(s) + CO
2
(g) không diễn ra ở điều kiện thường, phù hợp với giá trị
biến thiên enthalpy chuẩn của phản ứng khá dương.
D. Na
2
CO
3
bền với nhiệt hơn NaHCO
3
.
Câu 14. Trong dãy kim loại chuyển tiếp thứ nhất, kim loại có độ cứng cao nhất là
A. Ti B. Fe C. Cr D. Cu
Câu 15. Dãy nào sau đây sắp xếp các kim loại nhóm IA theo mức độ phản ứng với nước tăng dần?
A. K, Na, Li. B. Na, K, Li. C. Li, Na, K. D. K, Li, Na.
Câu 16. Cho pin điện hoá Al-Pb. Biết
3+
o
Al /Al
E
= -1,66 V và
2+
o
Pb /Pb
E
= - 0,13 V.
Sức điện động chuẩn của pin điện hoá Al - Pb là
A. 1,79 V. B. -1,79V. C. -1,53V. D. 1,53 V.
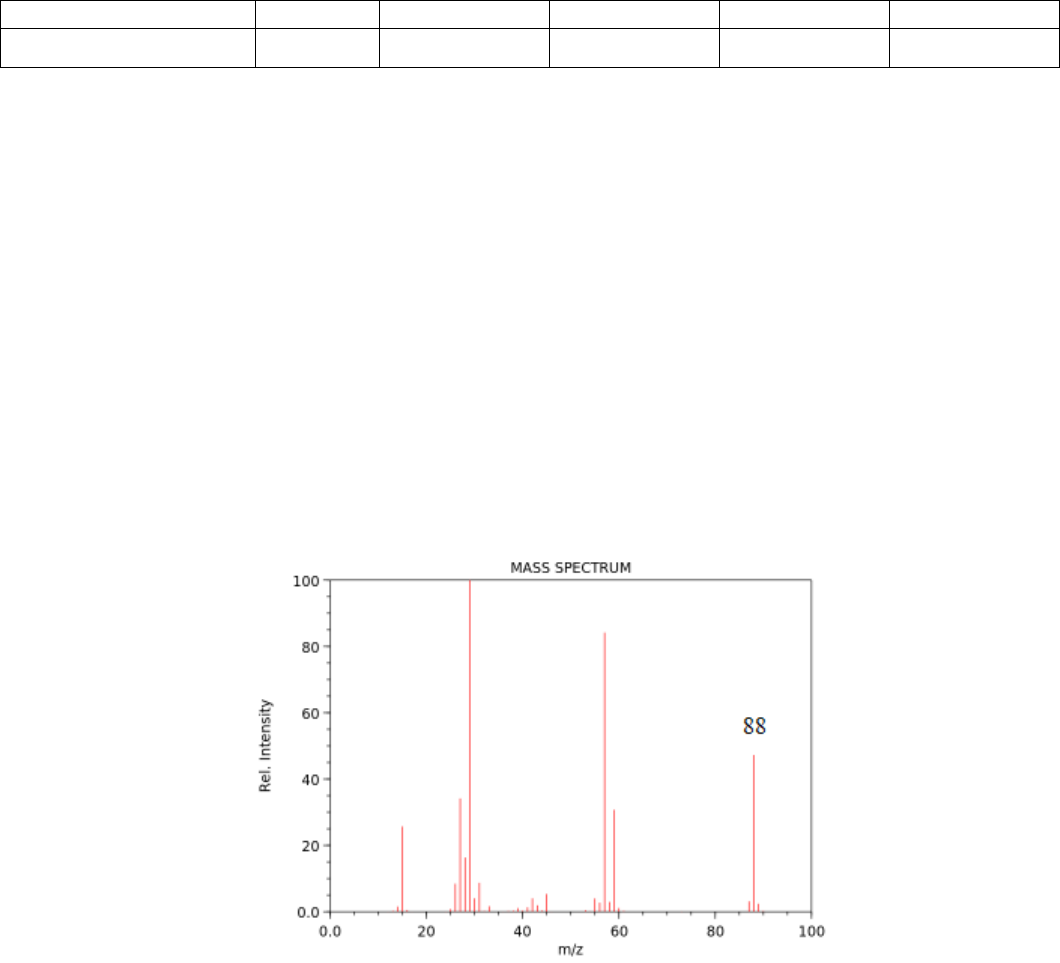
Câu 17. Phổ khối lượng của hợp chất hữu cơ X được cho như hình vẽ:
Công thức phân tử của X có thể là:
A. C
4
H
10
O. B. C
5
H
10
O. C. C
4
H
10
O
2
. D. C
4
H
8
O
2
.
Câu 18. Cho các chất sau: H
2
O, Cl
2
, K
2
O, NaF, N
2
, HCl, MgO. Số chất chứa liên kết ion trong phân tử là
A. 2. B. 3. C. 4. D. 5.
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc
sai.
Câu 1. Ở điều kiện chuẩn, cho bột Cu dư vào dung dịch Fe
2
(SO
4
)
3
tới khi phản ứng hoàn toàn, thu được chất
rắn X và dung dịch Y. Biết E°Fe
2+
/Fe = -0,44V; E°Cu
2+
/Cu = +0,34V; E°Fe
3+
/Fe
2+
= +0,771V. Phát
biểu dưới đây là đúng hay sai?
a. Cu có tính khử mạnh hơn Fe
2+
ở điều kiện chuẩn.
b. Trong điều kiện Fe
2
(SO
4
)
3
dư thì Y gồm ba muối.
c. Y gồm hai chất tan là CuSO
4
và FeSO
4
.
d. X gồm hai kim loại.
Câu 2. X là một peptide mạch hở có công thức phân tử C
13
H
24
N
4
O
6
. Thực hiện các phản ứng sau (theo
đúng tỉ lệ mol các chất):
(1) X + 4NaOH → X
1
+ H
2
NCH
2
COONa + X
2
+ 2H
2
O.
(2) X
1
+ 3HCl → C
5
H
10
NO
4
Cl + 2NaCl.
a. X là một tetrapeptide.
b. X
1
được ứng dụng làm mì chính (bột ngọt).
c. Trong dung dịch, X
1
làm quỳ tím hóa đỏ.
d. X
2
tác dụng với dung dịch HCl theo tỉ lệ mol tương ứng 1 : 3.
Câu 3. Hoà tan 0,422g mẫu khoáng vật của sắt trong dung dịch sulfuric acid dư, sao cho tất cả lượng sắt có
trong quặng đều chuyển thành Fe
2+
, thu được dung dịch A. Chuẩn độ Fe
2+
trong dung dịch A bằng chất
chuẩn là dung dịch thuốc tím KMnO
4
0,040M. Khi đã sử dụng 23,50mL thì phản ứng vừa qua điểm tương
đương.
5Fe
2+
(aq) + MnO
4
−
(aq) +8H
+
(aq) → 5Fe
3+
(aq) + Mn
2+
(aq) + 4H
2
O(l)
Mỗi phát biểu dưới đây là đúng hay sai?
a. Nếu chỉ có Fe
2+
trong dung dịch A tác dụng được với thuốc tím thì việc chuẩn độ dung dịch A sẽ giúp
xác định được lượng nguyên tố sắt trong mẫu khoáng vật. Từ đó tính được % (theo khối lượng) của nguyên
tố sắt có trong mẫu khoáng vật là 60,26 %.
b. Trong quá trình chuẩn độ trên, cần nhỏ từ từ dung dịch thuốc tím từ burette vào bình tam giác chứa
dung dịch A.
c. Cần thêm chất chỉ thị phù hợp vào bình tam giác chứa dung dịch A để xác định được thời điểm kết
thúc quá trình chuẩn độ.
d. Cần lặp lại thí nghiệm chuẩn độ 2 lần để bảo đảm tính chính xác của kết quả.
Câu 4. Một nhóm học sinh đã thực hiện phản ứng điều chế ethyl acetate từ nguyên liệu ban đầu là acetic
acid và ethanol trong phòng thí nghiệm. Khi phản ứng kết thúc, nhóm đã thu được hỗn hợp sản phẩm gồm
ethyl acetate và acetic acid, ethanol còn dư theo phương trình hoá học:
CH
3
COOH + C
2
H
5
OH
o
H ,t
CH
3
COOC
2
H
5
+ H
2
O
Vì ethyl acetate không phân cực, còn acetic acid và ethanol đều phân cực nên nhóm đã dùng dung môi hữu
cơ không phân cực diethyl ether (C
2
H
5
OC
2
H
5
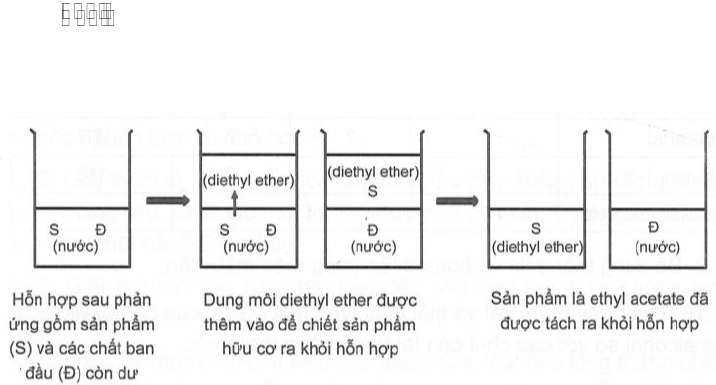
) đề chiết ethyl acetate ra khỏi hỗn hợp sau phản ứng theo sơ
đồ sau:
Chọn tính đúng sai cho các phát biểu sau về thí nghiệm của nhóm:
a) Diethyl ether là dung môi chiết lí tưởng trong thí nghiệm trên vì ethyl acetate tan tốt trong dung môi
này, còn acetic acid và ethanol lại tan tốt trong nước.
b) Bằng phương pháp chưng cất đơn giản, ta có thể tách ethyl acetate ra khỏi dung môi diethyl ether sau
khi chiết.
c) Do diethyl ether có nhiệt độ sôi thấp hơn nhiều so với ethyl acetate (34,6°C so với 77,1°C) nên có thể
thu được ethyl acetate sau khi chiết bằng cách dùng đèn cồn đun nhẹ cho dung môi diethyl ether bay hơi.
d) Để an toàn, ta có thể dùng nước nóng liên tục tưới lên bình cầu trong phương pháp chưng cất đơn giản
để tách ethyl acetate ra khỏi dung môi diethyl ether sau khi chiết.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6
Câu 1. Cho dãy các dung dịch: glucose, saccharose, ethanol, glycerol. Số dung dịch trong dãy phản ứng
được với Cu(OH)
2
ở nhiệt độ thường tạo thành dung dịch có màu xanh lam là
Đề thi thử bám sát đề minh họa 2025 môn Hóa - Đề 36
VnDoc.com xin gửi tới bạn đọc bài viết Đề thi thử tốt nghiệp THPT Quốc gia 2025 môn Hóa bám sát đề minh họa - Đề 36 để bạn đọc cùng tham khảo. Đề thi được tổng hợp gồm có 18 câu hỏi trắc nghiệm nhiều phương án lựa chọn, 4 câu hỏi trắc nghiệm đúng sai và 6 câu hỏi trả lời ngắn. Thí sinh làm bài trong thời gian 50 phút, đề có đáp án và lời giải chi tiết kèm theo. Mời các bạn cùng theo dõi đề thi dưới đây để có thêm tài liệu ôn thi kì thi THPT Quốc gia sắp tới nhé.