Hóa 11 Kết nối tri thức bài 3
Hóa 11 Kết nối tri thức bài 3: Ôn tập chương 1
Hóa 11 Kết nối tri thức bài 3: Ôn tập chương 1 được VnDoc.com tổng hợp và xin gửi tới bạn đọc cùng tham khảo. Mong rằng qua đây bạn đọc có thêm tài liệu để giải bài tập Hóa học 11 Kết nối tri thức nhé. Mời các bạn cùng theo dõi bài viết dưới đây.
Câu 1 trang 28 SGK Hóa 11 Kết nối
Hằng số KC của một phản ứng phụ thuộc vào yếu tố nào sau đây?
A. Nồng độ.
B. Nhiệt độ.
C. Áp suất.
D. Chất xúc tác.
Lời giải
Đáp án: B
Hằng số KC của một phản ứng phụ thuộc vào nhiệt độ.
Câu 2 trang 28 SGK Hóa 11 Kết nối
Thêm nước vào 10 mL dung dịch HCl 1,0 mol/L để được 1000 mL dung dịch A. Dung dịch mới thu được có pH thay đổi như thế nào so với dung dịch ban đầu?
A. pH giảm đi 2 đơn vị.
B. pH giảm đi 0,5 đơn vị.
C. pH tăng gấp đôi.
D. pH tăng 2 đơn vị.
Lời giải
Đáp án: D
Pha loãng dung dịch 100 lần thì nồng độ giảm 100 lần ⇒ pH tăng 2 đơn vị.
Câu 3 trang 28 SGK Hóa 11 Kết nối
Tính pH của các dung dịch sau:
a) Dung dịch NaOH 0,1 M;
b) Dung dịch HCl 0,1 M;
c) Dung dịch Ca(OH)2 0,01 M.
Lời giải
a) NaOH → Na+ + OH-
0,1 → 0,1 M
Ta có: [H+] . [OH]- = 10-14
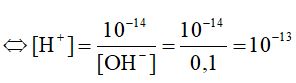
Ta có: pH = -log[H+] = 13.
b) HCl → H+ + Cl-
0,1 → 0,1 M
Ta có: pH = -log[H+] = 1 M.
c) Ca(OH)2 → Ca2+ + 2OH-
0,01 → 0,02 M
Ta có: [H+] . [OH]- = 10-14
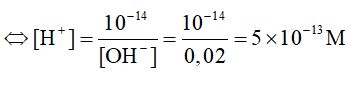
Ta có: pH = -log[H+] = 12,3.
Câu 4 trang 28 SGK Hóa 11 Kết nối
Viết biểu thức hằng số cân bằng KC cho các phản ứng sau:
a) 2SO2(g) + O2(g) ⇌ 2SO3 (g)
b) 2C(s) + O2(g) ⇌ 2CO(g)
c) AgCl(s) ⇌ Ag+(aq) + Cl-(aq)
Lời giải
a) 2SO2(g) + O2(g) ⇌ 2SO3 (g)
b) 2C(s) + O2(g) ⇌ 2CO(g)
c) AgCl(s) ⇌ Ag+(aq) + Cl-(aq)
KC = [Ag+].[Cl-]
Câu 5 trang 28 SGK Hóa 11 Kết nối
Cho cân bằng hoá học sau:
H2(g) + I2(g) ⇌ 2HI(g) ![]() \(\triangle _{r} H_{298}^{0}\) = -9,6 kJ
\(\triangle _{r} H_{298}^{0}\) = -9,6 kJ
Nhận xét nào sau đây không đúng?
A. Khi tăng nhiệt độ, cân bằng trên chuyển dịch theo chiều nghịch.
B. Ở nhiệt độ không đổi, khi tăng áp suất thì cân bằng không bị chuyển dịch.
C. Ở nhiệt độ không đổi, khi tăng nồng độ H2 hoặc I2 thì giá trị hằng số cân bằng tăng.
D. Ở trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
Lời giải
Đáp án: C
Hằng số cân bằng chỉ phụ thuộc vào nhiệt độ và bản chất của phản ứng, không phụ thuộc vào nồng độ.
Câu 6 trang 28 SGK Hóa 11 Kết nối
Xét phản ứng xảy ra trong lò luyện gang:
Fe2O3 (s) + 3CO(g) ⇌ 2Fe(s) + 3CO2(g) ∆rHo < 0
Nêu các yếu tố (nồng độ, nhiệt độ, áp suất) cần tác động vào cân bằng trên để cân bằng chuyển dịch về bên phải (làm tăng hiệu suất của phản ứng).
Lời giải
- Tăng nồng độ CO, cân bằng sẽ chuyển dịch theo chiều làm giảm nồng độ CO, tức chiều thuận, chiều tăng hiệu suất phản ứng.
- ∆rHo < 0 ⇒ Chiều thuận toả nhiệt ⇒ Giảm nhiệt độ, cân bằng sẽ chuyển dịch theo chiều làm tăng nhiệt độ tức chiều thuận, chiều tăng hiệu suất phản ứng.
- Do phản ứng thuận nghịch có tổng hệ số tỉ lượng của các chất khí ở hai vế bằng nhau, việc thay đổi áp suất không làm ảnh hưởng đến cân bằng.
Câu 7 trang 28 SGK Hóa 11 Kết nối
Cho cân bằng hoá học sau:
CO(g) + H2O(g) ⇌ CO2(g) + H2(g)
Ở 700oC, hằng số cân bằng KC = 8,3. Cho 1 mol khí CO và 1 mol hơi nước vào bình kín, dung tích 10 lít và giữ ở 700oC. Tính nồng độ các chất ở trạng thái cân bằng.
Lời giải
Nồng độ ban đầu của khí CO là:
Nồng độ ban đầu của hơi nước H2O là:
CO(g) + H2O(g) ⇌ CO2(g) + H2(g)
Ban đầu: 0,1 0,1 0 0 M
Phản ứng: x x x x M
Cân bằng: (0,1 – x) (0,1 – x) x x M
Áp dụng công thức:
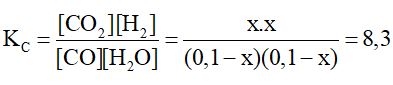
⇒ x2 = 8,3(x2 – 0,2x + 0,01)
⇔ 7,3x2 – 1,66x + 0,083 = 0
⇒ x = 0,074 (thoả mãn); x = 0,153 (loại do > 0,1).
Vậy ở trạng thái cân bằng:
[CO2] = [H2] = 0,074 M.
[CO] = [H2O] = 0,026 M.
Trắc nghiệm Hóa 11 Kết nối tri thức bài 3
-------------------------
Bài tiếp theo: Hóa 11 Kết nối tri thức bài 4
Trên đây VnDoc.com vừa gửi tới bạn đọc bài viết Hóa 11 Kết nối tri thức bài 3: Ôn tập chương 1. Hi vọng qua bài viết này bạn đọc có thể học tập tốt hơn môn Hóa học 11 Kết nối tri thức nhé. Mời các bạn cùng tham khảo thêm tại mục Toán 11 Kết nối tri thức.
