Giải bài tập Hóa 11 nâng cao bài 4
Hóa học 11 - Sự điện li của nước - pH - Chất chỉ thị axit-bazơ
- Bài 1 (trang 20 sgk Hóa học 11 nâng cao)
- Bài 2 (trang 20 sgk Hóa 11 nâng cao)
- Bài 3 (trang 20 sgk Hóa 11 nâng cao)
- Bài 4 (trang 20 sgk Hóa 11 nâng cao)
- Bài 5 (trang 20 sgk Hóa 11 nâng cao)
- Bài 6 (trang 20 sgk Hóa 11 nâng cao)
- Bài 7 (trang 20 sgk Hóa 11 nâng cao)
- Bài 8 (trang 20 sgk Hóa 11 nâng cao)
- Bài 9 (trang 20 sgk Hóa 11 nâng cao)
- Bài 10 (trang 20 sgk Hóa 11 nâng cao)
VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa 11 nâng cao bài 4, nội dung tài liệu gồm 10 bài tập trang 20 SGK kèm theo đáp án sẽ là nguồn thông tin hữu ích để phục vụ công việc học tập của các bạn học sinh được tốt hơn. Mời các bạn học sinh tham khảo chi tiết bài viết dưới đây nhé.
- Giải bài tập Hóa 11 nâng cao bài 1
- Giải bài tập Hóa 11 nâng cao bài 2
- Giải bài tập Hóa 11 nâng cao bài 3
Giải bài tập Hóa 11 nâng cao bài 4 Sự điện li của nước - pH - Chất chỉ thị axit-bazơ vừa được VnDoc.com sưu tập và xin gửi tới bạn đọc cùng tham khảo. Bài viết được tổng hợp gồm có lời giải của 10 bài tập trong sách giáo khoa môn Hóa học lớp 11 nâng cao. Qua bài viết bạn đọc có thể thấy được định nghĩa môi trường axit, trung tính và kiềm theo nồng độ H+ và pH, cách phân biệt các dung dịch bằng màu quỳ tím... Mời các bạn cùng tham khảo chi tiết và tải về tại đây nhé.
Giải bài tập Hóa 11 nâng cao
Bài 1 (trang 20 sgk Hóa học 11 nâng cao)
Phát biểu các định nghĩa môi trường axit, trung tính và kiềm theo nồng độ H+ và pH.
Lời giải:
- Môi trường axit [H+] > 10-7 ⇒ pH < 7
- Môi trường bazơ [H+] < 10-7 ⇒ pH > 7
- Môi trường trung tính [H+] = 10-7 ⇒ pH = 7
Bài 2 (trang 20 sgk Hóa 11 nâng cao)
Một dung dịch có [OH-] = 2,5.10-10M. Môi trường của dung dịch là:
A. Axit
B. Kiềm
C. Trung tính
D. Không xác định được.
Lời giải:
Chọn A.
Ta có: pOH = -lg[OH-] = -lg2,5.10-10 = 9,6
⇒ pH = 14 – 9,6 = 4,4 < 7
⇒ Môi trường của dung dịch là axit.
Bài 3 (trang 20 sgk Hóa 11 nâng cao)
Trong dung dịch HNO3 0,010M, tích số ion của nước là:
A. [H+][OH-] = 1,0.10-14
B. [H+][OH-] > 1,0.10-14
C. [H+][OH-] < 1,0.10-14
D. không xác định được.
Lời giải:
Chọn A. [H+][OH-] = 1,0.10-14
Bài 4 (trang 20 sgk Hóa 11 nâng cao)
Một dung dịch có [H+] = 4,2.10-3M, đánh giá nào dưới đây là đúng?
A. pH = 3,00;
B. pH = 4,00;
C. pH < 3,00;
D. pH > 4,00.
Lời giải:
Chọn D.
Ta có: pOH = -lg[OH-] = -lg4,2.10-3 = 2,3767
⇒ pH = 14 – 2,3767 = 11,6233 > 4
Bài 5 (trang 20 sgk Hóa 11 nâng cao)
Một dung dịch có pH = 5,00, đánh giá nào dưới đây là đúng?
A. [H+] = 2,0.10-5M ;
B. [H+] = 5,0.10-4M ;
C. [H+] = 1,0.10-5M ;
D. [H+] = 1,0.10-4M ;
Lời giải:
Chọn C. Ta có pH = -lg[H+] = 5 ⇒ [H+] = 1,0.10-5M ;
Bài 6 (trang 20 sgk Hóa 11 nâng cao)
Ka(CH3COOH) = 1,75.10-5 ; Ka(HNO2) = 4,0.10-4. Nếu hai axit có nồng độ mol bằng nhau và ở cùng nhiệt đô, khi quá trình điện li ở trạng thái cân bằng, đánh giá nào dưới đây là đúng?
A. [H+]CH3COOH > [H+]HNO2 ;
B. [H+]CH3COOH < [H+]HNO2 ;
C. pH(CH3COOH) < pH(HNO2) ;
D. [CH3COO-] > [NO2-].
Lời giải:
Chọn B.
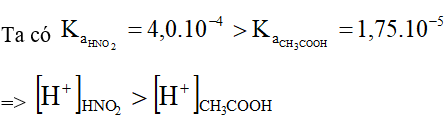
Bài 7 (trang 20 sgk Hóa 11 nâng cao)
Hai dung dịch axit đưa ra ở câu 6 có cùng nồng độ mol và ở cùng nhiệt độ, axit nào có độ điện li α lớn hơn?
Lời giải:
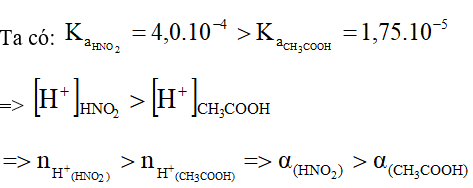
Bài 8 (trang 20 sgk Hóa 11 nâng cao)
Chất chỉ thị axit – bazơ là gì? Hãy cho biết màu của quỳ và phenolphtalein trong dung dịch ở các khoảng pH khác nhau.
Lời giải:
Chất chỉ thị axit – bazơ: Là chất có màu biến đổi phụ thuộc vào giá trị pH của dung dịch.
Màu của quỳ và phenolphtanein trong dung dịch ở các khoảng pH khác nhau.
- pH ≤ 6: Quỳ hóa đỏ, phenolphtanein không màu.
- pH = 7: Quỳ không đổi màu, phenolphtanein không màu.
- pH ≥ 8: Quỳ hóa xanh, phenophtanein không màu.
- pH ≥ 8,3: Quỳ hóa xanh, phenolphtanein hóa hồng.
Bài 9 (trang 20 sgk Hóa 11 nâng cao)
Cần bao nhiêu gam NaOH để pha chế 300,0 ml dung dịch có pH = 10,0?
Lời giải:
Ta có: pH = 10 ⇒ pOH = 14 – 10 = 4 ⇒ [OH-] = 10-4M
⇒ nOH- = [OH-].V = 10-4. 0,3 = 3.10-5
NaOH + Na+ + OH-
3.10-5 ← 3.10-5
Khối lượng NaOH cần dùng: m = 40.0,3.10-4 = 12.10-4 = 0,0012 (g).
Bài 10 (trang 20 sgk Hóa 11 nâng cao)
a) Tính pH của dung dịch chứa 1,46g HCl trong 400,0 ml.
b) Tính pH của dung dịch tạo thành sau khi trộn 100,0 ml dung dịch HCl 1,00M và 400,0 ml dung dịch NaOH 0,375M.
Lời giải:
a) nHCl = 1,46/35,5 = 0,04 mol
HCl → H+ + cl-
0,04 → 0,04
⇒ [H+] = 0,04/0,4 = 10-1M ⇒ pH = -lg10-1
b) nHCl = 0,1 mol; nNaOH = 0,4.0,375 = 0,15 (mol)
HCl → H+ + cl-
0,1 → 0,1
NaOH + Na+ + OH-
0,15 → 0,15
H+ + OH- → H2O
Trước phản ứng 0,1 → 0,15
Phản ứng 0,1 → 0,1
Sau phản ứng 0 0,05
⇒ nOH- dư = 0,05 mol
⇒ [OH-]dư = (nOH-dư)/V = 0,05/0,5 = 10-1M
⇒ pOH = -lg[OH-] = -lg10-1= 1 ⇒ pH = 13.
-----------------------------------
Trên đây VnDoc.com đã giới thiệu tới bạn đọc tài liệu: Giải bài tập Hóa 11 nâng cao bài 4. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Sinh học lớp 11, Vật lý lớp 11, Giải bài tập Hóa học lớp 11, Giải bài tập Toán 11 mà VnDoc tổng hợp và đăng tải.
Mời bạn đọc cùng tham gia nhóm Tài liệu học tập lớp 11 để có thêm tài liệu học tập nhé
