Giải bài tập Hóa 11 nâng cao bài 5
Hóa học 11 - Luyện tập: Axit, bazơ và muối
- Bài 1 (trang 23 sgk Hóa 11 nâng cao)
- Bài 2 (trang 23 sgk Hóa học 11 nâng cao)
- Bài 3 (trang 23 sgk Hóa 11 nâng cao)
- Bài 4 (trang 23 sgk Hóa 11 nâng cao)
- Bài 5 (trang 23 sgk Hóa 11 nâng cao)
- Bài 6 (trang 23 sgk Hóa 11 nâng cao)
- Bài 7 (trang 23 sgk Hóa 11 nâng cao)
- Bài 8 (trang 23 sgk Hóa 11 nâng cao)
- Bài 9 (trang 23 sgk Hóa 11 nâng cao)
- Bài 10 (trang 23 sgk Hóa 11 nâng cao)
VnDoc xin giới thiệu tới bạn đọc tài liệu Giải bài tập Hóa 11 nâng cao bài 5, nội dung tài liệu gồm 10 bài tập trang 23 SGK kèm theo đáp án sẽ là nguồn thông tin hữu ích để phục vụ công việc học tập của các bạn học sinh được tốt hơn. Mời thầy cô và các bạn học sinh tham khảo chi tiết bài viết dưới đây nhé.
- Giải bài tập Hóa 11 nâng cao bài 2
- Giải bài tập Hóa 11 nâng cao bài 3
- Giải bài tập Hóa 11 nâng cao bài 4
Giải bài tập Hóa 11 nâng cao bài 5 Luyện tập: Axit, bazơ và muối vừa được VnDoc.com sưu tập và xin gửi tới bạn đọc cùng tham khảo. Bài viết được tổng hợp gồm có lời giải của 10 bài tập trong sách giáo khoa môn Hóa học lớp 11 nâng cao bài Luyện tập: Axit, bazơ và muối. Qua bài viết bạn đọc có thể luyện tập được cách viết các biểu thức tính hằng số, cách tính giá trị của hằng số phân li... Mời các bạn cùng tham khảo chi tiết và tải về tại đây nhé.
Giải bài tập Hóa 11 nâng cao
Bài 1 (trang 23 sgk Hóa 11 nâng cao)
Viết các biểu thức tính hằng số phân li axit Ka hoặc hằng số phân li bazơ Kb của các axit và bazơ sau: HClO, BrO-, HNO2, NO2-.
Lời giải:
HClO ↔ H+ + ClO
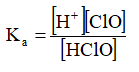
BrO- + H2O ↔ HbrO + OH-
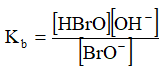
HNO2 ↔ H+ + NO2-
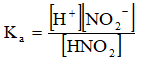
NO2- + H2O ↔ HNO2 + OH-
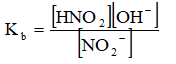
Bài 2 (trang 23 sgk Hóa học 11 nâng cao)
Đối với dung dịch axit yếu HNO2 0,10M, nếu bỏ qua sự điện li của nước thì đánh giá nào sau đây là đúng?
A. p> 1,00;
B. pH = 1,00;
C. [H+] > [NO2-];
D. [H+] < [NO2-];
Lời giải:
Chọn A.
HNO2 ↔ H+ + NO2-
Trước điện li 0,1 0 0
Điện li x x x
Ta có: [H+] = x = 10pH
Và x < 0,1 ≈ 10-1⇒ [H+] < 10-1⇒ 10-pH < 10-1⇒ pH > 1
Bài 3 (trang 23 sgk Hóa 11 nâng cao)
Đối với dung dịch axit mạnh HNO3 0,10M, nếu bỏ qua sự điện li của nước thì đánh giá nào sau đây là đúng?
A. pH < 1,00;
B. pH > 1,00;
C. [H+] = [NO3-];
D. [H+] > [NO3-];
Lời giải:
Chọn C.
HNO3 → H+ + NO3-
[H+] = [NO3-] = 0,1M
Bài 4 (trang 23 sgk Hóa 11 nâng cao)
Độ điện li α của axit yếu tăng theo độ pha loãng dung dịch. Khi đó giá trị của hằng số phân li axit Ka
A. tăng.
B. giảm.
C. không đổi.
D. có thể tăng, có thể giảm.
Lời giải:
Chọn A. Khi pha loãng, độ điện li α tăng ⇒ Ka tăng (K = α2.C)
Bài 5 (trang 23 sgk Hóa 11 nâng cao)
a) Hòa tan hoàn toàn 2,4g Mg trong 100,0 ml dung dịch HCl 2,1M. Tính pH của dung dịch thu được.
b) Tính pH của dung dịch thu được sau khi trộn 40,0 ml dung dịch HCl 0,50M với 60,0 ml dung dịch NaOH 0,50M
Lời giải:
a) nMg = 2,4/24 = 0,1 mol; nHCl = 0,1.3 = 0,3 mol
Mg + 2HCl + MgCl2 + H2↑
Trước phản ứng 0,1 0,3
Phản ứng 0,1→ 0,2
Sau phản ứng 0 0,1
Số mol HCl dư: (0,3 – 0,2) = 0,1 mol
HCldư → H+ + Cl-
0,1 → 0,1
⇒ [H+]dư = 0,1/0,1 = 1 mol/lít ⇒ pH = -lg[H+] =0.
b) nHCl= 0,04.0,5 = 0,02 (mol); nNaOH = 0,06.0,5 = 0,03 (mol)
HCl → H+ + Cl-
0,02 → 0,02
NaOH → Na+ + OH-
0,03 → 0,03
H+ + OH- →H2O
Trước phản ứng 0,02 0,03
Phản ứng 0,02 → 0,02
Sau phản ứng 0 0,01
⇒ nOH-dư = 0,01 mol
⇒ [OH-]dư = (nOH-)/V = 0,01/0,1 = 10-1M
⇒ pOH = -lg[OH-] = -lg10-1= 1 ⇒ pH = 13.
Bài 6 (trang 23 sgk Hóa 11 nâng cao)
Viết phương trình điện li của các chất sau trong nước: MgSO4, HClO3, H2S, Pb(OH)2, LiOH
Lời giải:
Phương trình điện li:
MgSO4 → Mg2+ + SO42-
Pb(OH)2 ↔ Pb(OH)+ + OH-
Pb(OH)+ ↔ Pb2+ + OH-
H2S ↔ H+ + HS-
HS- ↔ H+ + S2-
HClO3 → H+ + ClO3-
H2PbO2 ↔ H+ + HpbO2-
HpbO2- ↔ H+ + PbO22-
LiOH → Li+ + OH-
Bài 7 (trang 23 sgk Hóa 11 nâng cao)
Ion nào dưới đây là axit theo thuyết Bron – stêt?
A. SO42-;
B. NH4+;
C. NO3-;
D. SO32-.
Lời giải:
Chọn B. NH4+: NH4+ + H2O ↔ NH3 + H3O+
Bài 8 (trang 23 sgk Hóa 11 nâng cao)
Theo thuyết Bron – stêt, ion nào dưới đây là bazơ?
A. Cu2+;
B. Fe3+;
C. BrO-;
D. Ag+.
Lời giải:
Chọn C. BrO- : BrO- + H2O ↔ HBrO + OH-
Bài 9 (trang 23 sgk Hóa 11 nâng cao)
Ion nào sau đây là lưỡng tính theo thuyết Bron – Stêt?
A. Fe2+ ;
B. Al3+ ;
C. HS- ;
D. Cl-.
Lời giải:
Chọn C. HS- là ion lưỡng tính.
HS- + H2O ↔ H2S + OH-
HS- + H2O ↔ S2- + H3O+
Bài 10 (trang 23 sgk Hóa 11 nâng cao)
Tính nồng độ mol của ion H+ trong dung dịch HNO2 0,10M, biết rằng hằng số phân li axit của HNO2 là Ka = 4,0.10-4.
Lời giải:
Xét 1 lít dung dịch HNO2
HNO2 ↔ H+ + NO2-
Trước điện li 0,1 0 0
Điện li x → x → x
Sau điện li (0,01-x) x x
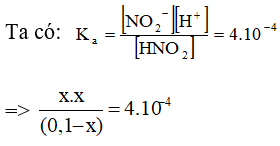
Vì x << 0,1 ⇒ (0,1 – x) ≈ 0,1 ⇒ x.x = 0,1.4.10-4 = 40.10-6 ⇒ x = 6,32.10-3.
⇒ [H+] = 6,32.10-3 mol/ lít
-----------------------------------
Trên đây VnDoc.com đã giới thiệu tới bạn đọc tài liệu: Giải bài tập Hóa 11 nâng cao bài 5. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Sinh học lớp 11, Vật lý lớp 11, Giải bài tập Hóa học lớp 11, Giải bài tập Toán 11 mà VnDoc tổng hợp và đăng tải.
Mời bạn đọc cùng tham gia nhóm Tài liệu học tập lớp 11 để có thêm tài liệu học tập nhé
