Các yếu tố ảnh hưởng đến tốc độ phản ứng
Phương án nào dưới đây mô tả đầy đủ nhất các yếu tố ảnh hưởng đến tốc độ phản ứng?
Các yếu tố ảnh hưởng đến tốc độ phản ứng:
- Nồng độ;
- Nhiệt độ;
- Áp suất;
- Chất xúc tác;
- Diện tích bề mặt tiếp xúc.
Cùng nhau thử sức với bài kiểm tra 15 phút Hóa 10 Chủ đề 6 Tốc độ phản ứng
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Các yếu tố ảnh hưởng đến tốc độ phản ứng
Phương án nào dưới đây mô tả đầy đủ nhất các yếu tố ảnh hưởng đến tốc độ phản ứng?
Các yếu tố ảnh hưởng đến tốc độ phản ứng:
Xác định các phương pháp hiệu quả để tăng tốc độ phản ứng
Phản ứng tạo NO từ NH3 là một giai đoạn trung gian trong quá trình sản xuất nitric acid:
4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g)
4NO(g) + 6H2O(g)
Một học sinh đề xuất một số phương pháp sau để tăng tốc độ phản ứng trên:
(1) Tăng nồng độ của chất tham gia phản ứng.
(2) Sử dụng chất xúc tác: Platinim (Pt) (hoặc Fe2O3, Cr2O3)
(3) Tăng nhiệt độ.
(4) Giảm áp suất.
Các phương pháp hiệu quả để tăng tốc độ phản ứng là:
Các phương pháp hiệu quả để tăng tốc độ phản ứng là: (1), (2) và (3).
Phản ứng có chất khí tham gia Khi giảm áp suất thì tốc độ phản ứng giảm.
Hằng số k của phản ứng
Hằng số tốc độ phản ứng k
Đại lượng hằng số tốc độ phản ứng k đặc trưng cho mỗi phản ứng và chỉ phụ thuộc vào nhiệt độ, không phụ thuộc vào nồng độ chất phản ứng.
Khái niệm tốc độ phản ứng
Tốc độ phản ứng của phản ứng hóa học là
Tốc độ phản ứng của một phản ứng hóa học là đại lượng đặc trưng cho sự biến thiên nồng độ của một trong các chất phản ứng hoặc sản phẩm trong một đơn vị thời gian.
Yếu tố đã ảnh hưởng đến tốc độ phản ứng
Cho 2 quá trình:
(1) Zinc dạng bột phản ứng với dung dịch hydrochloric acid nhanh hơn so với Zinc dạng lá.
(2) Để thực phẩm trong tủ lạnh giúp cho thực phẩm dược tươi lâu hơn.
Yếu tố nào đã ảnh hưởng đến tốc độ phản ứng của 2 quá trình trên?
(1) Zinc dạng bột phản ứng với dung dịch hydrochloric acid nhanh hơn so với Zinc dạng lá ⇒ Diện tích tiếp xúc
(2) Để thực phẩm trong tủ lạnh giúp cho thực phẩm dược tươi lâu hơn ⇒ Nhiệt độ
Tính tốc độ phản ứng tại thời điểm t khi nồng độ A giảm
Cho phản ứng A + 2B → C
Nồng độ ban đầu của [A] = 0,3M, [B] = 0,5M, hằng số tốc độ k = 0,4. Tính tốc độ phản ứng tại thời điểm t khi nồng độ A giảm 0,1 mol/l:
A + 2B → C
Tốc độ tại thời điểm t
Khi nồng độ A giảm 0,1 mol/lít thì B giảm 0,2 mol/l theo phản ứng tỉ lệ 1 : 2
Nồng độ tại thời điểm t:
[A’] = 0,3 – 0,1 = 0,2 (mol/l)
[B’] = 0,5 -0,2 = 0,3 (mol/l)
v = k.[A’].[B’] 2= 0,4.[0,2].[0,3] 2 = 0,0072 mol/ls
Phản ứng thuận nghịch
Phản ứng nào sau đây không phải là phản ứng thuận nghịch.
Phản ứng không phải là phản ứng thuận nghịch.
Fe (s) + H2SO4 (aq) → FeSO4 (aq) + H2(g).
Nước trong bình có nhiệt độ
Cho sơ đồ hòa tan NH4NO3 sau:
NH4NO3(s) + H2O(l) → NH4NO3 (aq) ∆H = +26 kJ
Hòa tan 80 g NH4NO3 khan vào bình chứa 1 L nước ở 25oC. Sau khi muối tan hết, nước trong bình có nhiệt độ là
80g NH4NO3 ~ 1 mol ⇒ Q = 26 (kJ)
∆H > 0, quá trình hòa tan thu nhiệt, nhiệt độ giảm đi một lượng là:
(Với 4,2 (J/g.K) là nhiệt dung riêng của nước)
⇒ Nhiệt độ cuối cùng là 25 – 6,2 = 18,8oC
Yếu tố được sử dụng để tăng tốc độ phản ứng
Yếu tố nào được sử dụng để tăng tốc độ phản ứng trong trường hợp sau: “Sự cháy diễn ra mạnh và nhanh hơn khi đưa lưu huỳnh (sulfur) đang cháy ngoài không khí vào lọ đựng khí oxygen”?
Khi đưa lưu huỳnh (sulfur) đang cháy ngoài không khí vào lọ đựng khí oxygen, phản ứng diễn ra nhanh hơn ⇒ tăng nồng độ khí oxygen ⇒ yếu tố nồng độ được sử dụng để tăng tốc độ phản ứng.
Các yếu tố làm tăng hiệu suất
Phản ứng N2 + 3H2 ![]() 2NH3; ΔrH0298 < 0. Cho một số yếu tố: (1) tăng áp suất, (2) tăng nhiệt độ, (3) tăng nồng độ N2 và H2, (4) tăng nồng độ NH3, (5) tăng lượng xúc tác.
2NH3; ΔrH0298 < 0. Cho một số yếu tố: (1) tăng áp suất, (2) tăng nhiệt độ, (3) tăng nồng độ N2 và H2, (4) tăng nồng độ NH3, (5) tăng lượng xúc tác.
Các yếu tố làm tăng hiệu suất của phản ứng nói trên là:
Tăng áp suất và tăng nồng độ H2, N2 làm cân bằng chuyển dịch theo chiều thuận, làm tăng hiệu suất của phản ứng.
Tốc độ phản ứng thay đổi
Với phản ứng có γ = 2. Nếu nhiệt độ tăng từ 35°C lên 75°C thì tốc độ phản ứng
=
⇒
=
= 16
Vậy tốc độ phản ứng tăng gấp 16 lần.
Khí được bơm vào các túi đựng thực phẩm trước khi đóng gói
Để hạn chế sự ôi thiu thực phẩm do các phản ứng của oxygen cũng như sự hoạt động của vi khuẩn, người ta thường bơm khí nào sau đây vào các túi đựng thực phẩm trước khi đóng gói?
Thực phẩm bị ôi thiu do các phản ứng oxi hóa của oxygen cũng như hoạt động của vi khuẩn. Để hạn chế sự ôi thiu, người ta bơm khí N2 hoặc CO2 vào túi đựng thực phẩm trước khi đóng gói. Khi đó nồng độ khí oxygen sau khi bơm N2 hoặc CO2 chỉ còn 2 – 5%.
Tác động nào làm cân bằng chuyển dịch theo chiều thuận
Cho cân bằng sau: 2SO2 (g) + O2 (g) ![]() 2SO3 (g) ΔrHo 298 < 0. Tác động nào sau đây làm cân bằng chuyển dịch theo chiều thuận.
2SO3 (g) ΔrHo 298 < 0. Tác động nào sau đây làm cân bằng chuyển dịch theo chiều thuận.
ΔrHo 298 < 0 (phản ứng tỏa nhiệt)
Giảm thể tích bình phản ứng thì áp suất tăng, chuyển dịch chiều giảm áp suất (hay chiều làm giảm số mol khí) ⇒ theo chiều thuận
Tìm các phát biểu đúng về đồ thị
Có hai miếng iron có kích thước giống hệt nhau, một miếng là khối iron đặc (A), một miếng có nhiều lỗ nhỏ li ti bên trong và trên bề mặt (B). Thả hai miếng iron vào hai cốc đựng dung dịch HCl cùng thể tích và nồng độ, theo dõi thể tích khi hydrogen thoát ra theo thời gian. Vẽ đồ thị thể tích khi theo thời gian, thu được hai đồ thị sau:
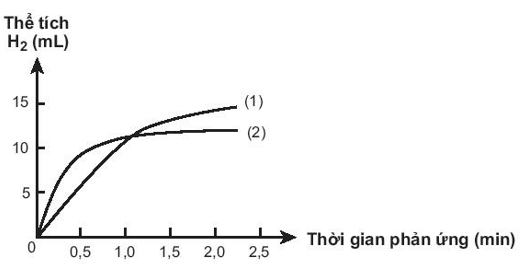
Cho các phát biểu sau, các phát biểu đúng là:
(1) Miếng iron có nhiều lỗ có diện tích bề mặt lớn hơn nên lúc đầu có tốc độ phản ứng với HCl cao hơn.
(2) Đồ thị (2) mô tả tốc độ thoát khí từ miếng iron (A).
(3) Đồ thị (1) mô tả tốc độ thoát khí từ miếng iron (B).
(4) Khi 2 miếng iron chưa phản ứng hết, thể tích khí H2 thoát ra của miếng iron (B) nhiều hơn miếng iron (A).
Các phát biểu đúng là: (1) và (4).
Miếng iron có nhiều lỗ có diện tích bề mặt lớn hơn nên lúc đầu tốc độ phản ứng với HCl cao hơn. Đồ thị (2) mô tả tốc độ thoát khí từ miếng iron B. Đồ thị (1) mô tả tốc độ thoát khí từ miếng iron A.
Tốc độ trung bình của phản ứng theo N2O4
Xét phản ứng phân hủy N2O5 ở 45oC
![]()
Sau 184 giây đầu tiên, nồng độ của N2O4 là 0,25M. Tốc độ trung bình của phản ứng theo N2O4 trong khoảng thời gian trên là
Phương trình tổng quát
aA + bB → cC + dD
Đồ thị biểu diễn sự phụ thuộc của tốc độ phản ứng vào nồng độ
Đồ thị dưới đây biểu diễn sự phụ thuộc của tốc độ phản ứng vào nồng độ chất phản ứng:
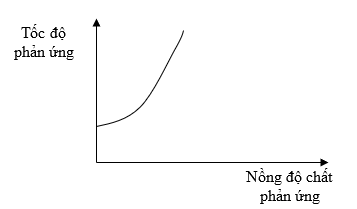
Từ đồ thị trên, ta thấy tốc độ phản ứng
Theo đồ thị ta thấy khi nồng độ chất phản ứng tăng, tốc độ phản ứng tăng.
Khái niệm tốc độ trung bình của phản ứng
Tốc độ trung bình của phản ứng là
Tốc độ trung bình của phản ứng là tốc độ được tính trong một khoảng thời gian phản ứng.
Tốc độ phản ứng thay đổi
Cho 5 gam kẽm (Zn) hạt vào một cốc đựng dung dịch H2SO4 3 M (dư) ở nhiệt độ thường. Nếu giữ nguyên các điều kiện khác, chỉ biến đổi một trong các điều kiện sau thì tốc độ phản ứng sẽ biến đổi như thế nào (tăng lên, giảm xuống hay không đổi)? Vì sao?
a. Thay 5 gam kẽm hạt bằng 5 gam kẽm bột.
b. Thay dung dịch H2SO4 3 M bằng dung dịch H2SO4 4 M.
c. Thực hiện phản ứng ở nhiệt độ phản ứng là 50oC.
Cho 5 gam kẽm (Zn) hạt vào một cốc đựng dung dịch H2SO4 3 M (dư) ở nhiệt độ thường. Nếu giữ nguyên các điều kiện khác, chỉ biến đổi một trong các điều kiện sau thì tốc độ phản ứng sẽ biến đổi như thế nào (tăng lên, giảm xuống hay không đổi)? Vì sao?
a. Thay 5 gam kẽm hạt bằng 5 gam kẽm bột.
b. Thay dung dịch H2SO4 3 M bằng dung dịch H2SO4 4 M.
c. Thực hiện phản ứng ở nhiệt độ phản ứng là 50oC.
a. Thay 5 gam kẽm hạt bằng 5 gam kẽm thì diện tích tiếp xúc của chất phản ứng tăng lên ⇒ tốc độ phản ứng tăng.
b. Thay dung dịch H2SO4 3 M bằng dung dịch H2SO4 4 M thì nồng độ chất phản ứng tăng ⇒ tốc độ phản ứng tăng.
c. Thực hiện phản ứng ở nhiệt độ phản ứng là 50oC tức là tăng nhiệt độ ⇒ tốc độ phản ứng tăng.
Yếu tố ảnh hưởng của xúc tác đến tốc độ phản ứng
Yếu tố nào liên quan đến sự ảnh hưởng của xúc tác với tốc độ phản ứng?
Ảnh hưởng của chất xúc tác đến tốc độ phản ứng được giải thích dựa vào năng lượng hoạt hóa. Đây là năng lượng tối thiểu cần cung cấp cho các hạt (nguyên tử, phân tử hoặc ion) để va chạm giữa chúng gây ra phản ứng hóa học.
Khi có xúc tác, phản ứng sẽ xảy ra qua nhiều giai đoạn. Mỗi giai đoạn đều có năng lượng hoạt hóa thấp hơn so với phản ứng không xúc tác. Do đó số hạt có đủ năng lượng hoạt hóa sẽ nhiều hơn, dẫn đến tốc độ phản ứng tăng lên.
Tính thời gian để kết thúc phản ứng
Nếu ở 150°C, một phản ứng hoá học kết thúc sau 16 phút. Nếu hạ nhiệt độ xuống 80°C thì thời gian để kết thúc là bao nhiêu phút? Biết trong khoảng nhiệt độ đó thì cứ nhiệt độ tăng 10oC thì tốc độ phản ứng tăng 2,5 lần.
Ta có
v150 = v80.610
Tốc độ của phản ứng ở 150°C lớn hơn tốc độ của phản ứng ở 80°C là 610 lần thì thời gian phản ứng tăng ở 80°C là:
610.16 = 9760 phút.
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: