Cấu tạo hóa học hợp chất hữu cơ
1. Tìm hiểu thuyết cấu tạo hóa học trong hóa học hữu cơ
Thuyết cấu tạo hóa học gồm những luận điểm chính sau:
- Trong phân tử hợp chất hữu cơ, các nguyên tử liên kết với nhau theo đúng hóa trị và theo một trật tự nhất định.
Ví dụ: Ethanol và dimethyl ether đều có công thức phân tử là C2H6O nhưng có tính chất vật lí và tính chất hóa học rất khác nhau do chúng có cấu tạo hóa học khác nhau.
| Ethanol | Dimethyl ether |
| Nhiệt độ sôi: 78,3oC | Nhiệt độ sôi: -24,9oC |
| Tan vô hạn trong nước | Ít tan trong nước |
| Tác dụng với sodium tạo khí hydrogen | Không tác dụng với sodium |
- Trong phân tử hợp chất hữu cơ, carbon có hóa trị 4. Nguyên tử carbon không những có thể liên kết với nguyên tử của nguyên tố khác mà còn liên kết với nhau tạo thành mạch carbon (mạch vòng, mạch hở, mạch nhánh, mạch không nhánh).
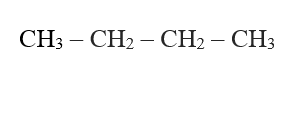
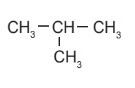
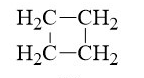
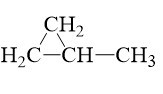
Một số chất hữu cơ tương ứng với các dạng mạch carbon khác nhau
- Tính chất của hợp chất hữu cơ phụ thuộc vào thành phần phân tử (bản chất, số lượng các nguyên tử) và cấu tạo hóa học (thứ tự liên kết giữa các nguyên tử).
Ví dụ:
| Chất | Nhiệt độ sôi (oC) | Nhiệt độ nóng chảy (oC) | Một số tính chất khác |
| CH4 | -161,5 | -182,46 | Chất khí, dễ cháy, không tan trong nước. |
| CCl4 | 76,7 | -22,8 | Chất lỏng, không cháy, không tan trong nước. |
| CH3OH | 64,5 | -97,5 | Chất lỏng, tan nhiều trong nước, tác dụng với sodium. |
| CH3-O-CH3 | -24,8 | -141,49 | Chất khí, tan ít tronh nước, không tác dụng với sodium. |
2. Biểu diễn cấu tạo phân tử của hợp chất hữu cơ
- Công thức cấu tạo biểu diễn thứ tự và cách thức liên kết (liên kết đơn, liên kết bội) của các nguyên tử trong phân tử.
- Công thức cấu tạo của hợp chất hữu cơ có thể được biểu diễn dưới các dạng:
- Công thức cấu tạo đầy đủ: Biểu diễn đầy đủ tất cả các liên kết trên một mặt phẳng.
- Công thức cấu tạo thu gọn: Các nguyên tử, nhóm nguyên tử cùng liên kết với một nguyên tử carbon được viết thành một nhóm.
- Công thức khung phân tử: Dùng nét gạch để biểu diễn liên kết giữa các nguyên tử carbon với nhau và giữa carbon với nguyên tử khác mà không phải là hydrogen.
Ví dụ:
- Butane có các công thức cấu tạo đầy đủ, công thức cấu tạo thu gọn và công thức khung phân tử như sau:
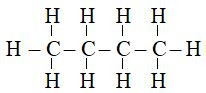 |
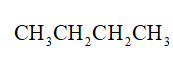 |
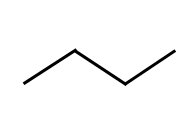 |
| Công thức cấu tạo đầy đủ | Công thức cấu tạo thu gọn | Công thức khung phân tử |
- 2-methylbut-1-ene có các công thức cấu tạo đầy đủ, công thức cấu tạo thu gọn và công thức khung phân tử như sau:
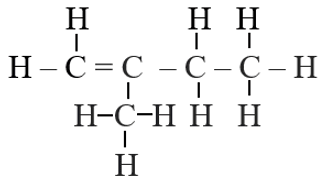 |
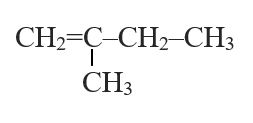 |
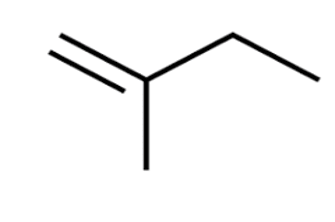 |
| Công thức cấu tạo đầy đủ | Công thức cấu tạo thu gọn | Công thức khung phân tử |
II. Đồng đẳng, đồng phân
1. Tìm hiểu khái niệm chất đồng đẳng và dãy đồng đẳng
Những hợp chất hữu cơ được gọi là đồng đẳng khi chúng có thành phần phân tử hơn kém nhau một hoặc nhiều nhóm CH2 và có tính chất hóa học tương tự nhau.
Ví dụ:
- Một số hợp chất hữu cơ trong dãy đồng đẳng của alkane (CnH2n+2).
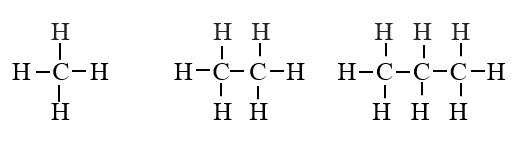 |
||
| (A) CH4 | (B) CH3-CH3 | (C) CH3-CH2-CH3 |
| methane | ethane | propane |
- Một số hợp chất hữu cơ trong dãy đồng đẳng của alcohol no, đơn chức, mạch hở (CnH2n+2O).
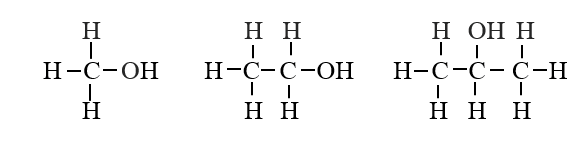 |
||
| (X) CH3OH | (Y) CH3CH2OH | (Z) CH3-CHOH-CH3 |
| methanol | ethanol | propan-2-ol |
2. Tìm hiểu hiện tượng đồng phân trong hóa học hữu cơ
Chất đồng phân là những chất khác nhau nhưng có cùng công thức phân tử.
Ví dụ:
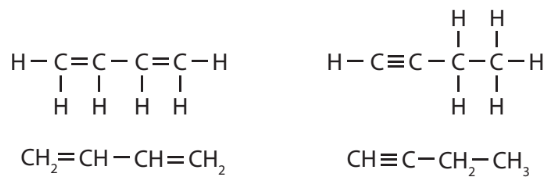 |
|
| buta-1,3-dien | but-1-yne |
Có nhiều loại đồng phân: đồng phân cấu tạo (gồm đồng phân mạch carbon, đồng phân loại nhóm chức, đồng phân vị trí nhóm chức) và đồng phân lập thể (đồng phân khác nhau về vị trí không gian của các nguyên tử, nhóm nguyên tử).
Ví dụ:
| Đồng phân mạch carbon | CH3 – CH2 – CH3 | 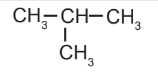 |
| Đồng phân loại nhóm chức | CH3 – CH2 – OH | CH3 – O – CH3 |
| Đồng phân vị trí nhóm chức | CH3 – CH2 – CH2 – OH | 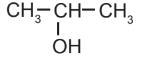 |
