Điều chế khí oxi - Phản ứng phân hủy
Chuyên đề Hóa học lớp 8: Điều chế khí oxi - Phản ứng phân hủy được VnDoc sưu tầm và giới thiệu tới các bạn học sinh cùng quý thầy cô tham khảo. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 8 hiệu quả hơn. Mời các bạn tham khảo.
Chuyên đề: Điều chế khí oxi - Phản ứng phân hủy
A/ Lý thuyết bài: Điều chế khí oxi - Phản ứng phân hủy
1. Điều chế oxi
a. Trong phòng thí nghiệm
Đun nóng hợp chất giâu oxi và dễ bị phân hủy ở nhiệt độ cao như kali pemanganat KMnO4 hoặc kali clorat KClO3 trong ống nghiệm, oxi thoát ra theo PT:
2KMnO4 −to→ K2MnO4 + MnO2 + O2
2KClO3 −to→ 2KCl + 3O2
b. Trong công nghiệp
- Sản xuất từ không khí: hóa lỏng không khí ở nhiệt độ thấp và áp suất cao. Trước hết thu được Nitơ (-196°C) sau đó là Oxi (- 183°C)
- Sản xuất từ nước: điện phân nước
2. Phản ứng phân hủy
Là phản ứng hóa học trong đó từ môtj chất sinh ra nhiều chất mới.
VD: 2KMnO4 −to→ K2MnO4 + MnO2 + O2
2KClO3 −to→ 2KCl + 3O2
B/ Trắc nghiệm bài: Điều chế khí oxi - Phản ứng phân hủy
Câu 1: Các chất dung để điều chế Oxi trong phòng thí nghiệm là
A. KClO3 B. KMnO4 C. CaCO3 D. Cả A & B
Câu 2: Tổng hệ số của chất tham gia và sản phẩm là
2KClO3 −to→ 2KCl + 3O2
A. 2&5 B. 5&2 C. 2&2 D. 2&3
Câu 3: Có những cách nào điều chế oxi trong công nghiệp
A. Dùng nghiên liệu là không khí
B. Dùng nước làm nguyên liệu
C. Cách nào cũng được
D. A&B
Câu 4: Nhiệt phân 12,25 g KClO3 thấy có khí bay lên. Tính thể tích của khí ở đktc
A. 4,8 l B. 3,36 l C. 2,24 l D. 3,2 l
Câu 5: Số sản phẩm tạo thành của phản ứng phân hủy là
A. 2
B. 3
C. 2 hay nhiều sản phẩm
D. 1
Câu 6: Chọn nhận xét đúng
A. Phản ứng phân hủy là một dạng của phản ứng hóa học
B. Phản ứng hóa hợp là phản ứng oxi hóa khử
C. Phản ứng phân hủy là phản ứng sinh ra duy nhất 2 chất mới
D. Cả A và C đều đúng
Câu 7: Phản ứng phân hủy là
A. Ba + 2HCl → BaCl2 + H2
B. Cu + H2S → CuS+H2
C. MgCO3 → MgO + CO2
D. KMnO4 → MnO + O2 + K2O
Câu 8: Cho phản ứng 2KMnO4 −to→ K2MnO4 + MnO2 + O2
Tổng hệ số sản phẩm là
A. 3 B. 2 C. 1 D. 5
Câu 9: Tính khối lượng KMnO4 biết nhiệt phân thấy 2,7552 l khí bay lên
A. 38,678 g B. 38,868 g C. 37,689 g D. 38,886 g
Câu 10: Phương trình không điều chế oxi trong phòng thí nghiệm
A. 2KMnO4 −to→ K2MnO4 + MnO2 + O2 ↑
B. 2H2O2 −to→ 2H2O + O2
C. 2KClO3 −MnO2→ 2KCl + 3O2
D. 2H2O −to→ 2H2 + O2
Đáp án:
| 1.D | 2.A | 3.D | 4.B | 5.C |
| 6.A | 7.C | 8.A | 9.B | 10.D |
Hướng dẫn:
Câu 4:
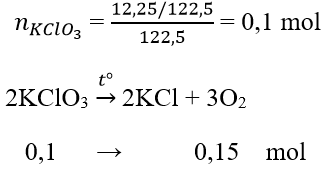
VO2= 0,15.22,4 = 3,36 l
Câu 9:
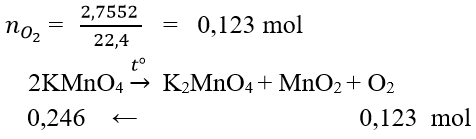
nKMnO4= 0,246.158 = 38,868 g
Với chuyên đề: Điều chế khí oxi - Phản ứng phân hủy trên đây chúng ta có thể hiểu rõ về cách điều chế khí oxi trong phòng thí nghiệm và thực tế, các khái niệm, phương trình hóa học của phản ứng phân hủy.
Trên đây VnDoc đã giới thiệu tới các bạn lý thuyết Hóa học 8: Điều chế khí oxi - Phản ứng phân hủy. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Chuyên đề Hóa học 8, Giải bài tập Hóa học lớp 8, Giải bài tập Vật Lí 8, Tài liệu học tập lớp 8 mà VnDoc tổng hợp và giới thiệu tới các bạn đọc.
