Lý thuyết Hóa 9 bài 4: Một số axit quan trọng
Lý thuyết Hóa học lớp 9 bài 4: Một số axit quan trọng hệ thống kiến thức cơ bản trong chương trình Hóa 9 bài 4, giúp các em nắm vững lý thuyết được học trong bài, từ đó vận dụng làm bài tập liên quan hiệu quả.
Lý thuyết Hóa học 9 bài 4: Một số axit quan trọng
A. Lý thuyết Hóa 9 bài 4
A. AXIT CLOHIĐRIC (HCl)
I. Tính chất
- Khí hiđro clorua (khí HCl) tan trong nước tạo thành dung dịch axit clohiđric.
- Axit clohiđric có đầy đủ tính chất của một axit mạnh
1. Làm đổi màu quỳ tím thành đỏ
2. Tác dụng với nhiều kim loại (Mg, Zn, Al, Fe,…) tạo thành muối và giải phóng khí H2 (không tác dụng với Cu, Ag, …)
Ví dụ: Al + HCl → AlCl3 + H2↑
3. Tác dụng với bazơ tạo thành muối clorua và nước (phản ứng trung hòa)
Cu(OH)2 + 2HCl → CuCl2 (dd xanh lam) + 2H2O
Fe(OH)3 + 3HCl → FeCl3 (dd vàng nâu) + 3H2O
4. Tác dụng với oxit bazơ tạo thành muối clorua và nước
VD: CaO + 2HCl → CaCl2 + H2O
5. Tác dụng với một số muối
* Điều kiện xảy ra phản ứng: thỏa mãn 1 trong 3 điều kiện sau
+ Tạo ra chất khí
+ Tạo ra kết tủa
+ Tạo ra nước (hoặc axit yếu)
Ví dụ: BaCO3 + 2HCl → BaCl2 + CO2 ↑ + H2O
II. Ứng dụng
- Điều chế các muối clorua
- Làm sạch bề mặt kim loại trước khi hàn (VD nhựa thông)
- Tẩy gỉ kim loại trước khi sơn, tráng, mạ kim loại
- Chế biến thực phẩm, dược phẩm
B. AXIT SUNFURIC (H2SO4)
I. Tính chất vật lí
- Chất lỏng sánh, không màu, nặng gấp đôi nước, không bay hơi, dễ tan trong nước, tỏa rất nhiều nhiệt.
* Cách pha loãng dung dịch H2SO4
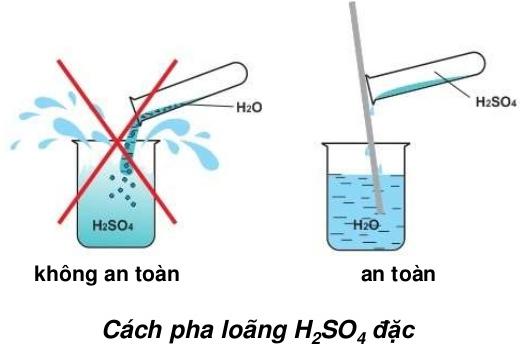
H2SO4 tan vô hạn trong nước và tỏa rất nhiều nhiệt. Nếu ta rót nước vào H2SO4, nước sôi đột ngột và kép theo những giọt axit bắn ra xung quanh gây nguy hiểm. Vì vậy, muốn pha loãng axit H2SO4 đặc, người ta phải rót từ từ axit vào nước và khuấy nhẹ bằng đũa thủy tinh mà không được làm ngược lại.
II. Tính chất hóa học
1. Axit sunfuric loãng có tính chất hóa học của axit (5 tính chất, tương tự HCl)
2. Axit sunfuric đặc có những tính chất hóa học riêng
a) Tác dụng với hầu hết kim loại (trừ Ag, Pt)
Cu không phản ứng với H2SO4 loãng nhưng phản ứng với H2SO4 đặc tạo dung dịch màu xanh lam và khí mùi hắc:
Cu + 2H2SO4 đặc ![]() CuSO4 + SO2 + 2H2O
CuSO4 + SO2 + 2H2O
- H2SO4 đặc tác dụng với nhiều kim loại khác tạo muối sunfat và giải phóng sản phẩm khử (S, SO2, H2S), không giải phóng khí H2.
b) Tính háo nước

- Đổ dung dịch H2SO4 vào cốc đựng đường. Màu trắng của đường chuyển sang nâu rồi thành màu đen, xốp và bị bọt khí đẩy trào ra khỏi miệng cốc, tỏa nhiều nhiệt.
Giải thích: Chất rắn màu đen là Cacbon, do axit sunfuric đặc có tính háo nước, hút nước của phân tử đường
C12H22O11 ![]() + 11H2O
+ 11H2O
III. Ứng dụng
H2SO4 có rất nhiều ứng dụng quan trọng như: phẩm nhuộm, phân bón, chất tẩy rửa tổng hợp, chất dẻo, ắc quy…
IV. Sản xuất axit sunfuric
Sơ đồ phản ứng: S → SO2 → SO3 → H2SO4
V. Nhận biết axit sunfuric và muối sunfat
- Dùng dung dịch muối BaCl2, Ba(NO3)2 hoặc Ba(OH)2 => hiện tượng: có kết tủa trắng
B. Trắc nghiệm Hóa 9 bài 4
C. Giải bài tập Hóa 9 bài 4
Mời các bạn tham khảo lời giải Hóa 9 bài 4 tại đây: Giải Hóa 9 Bài 4: Một số axit quan trọng
............................................
Ngoài Lý thuyết Hóa học lớp 9 bài 4, các bạn có thể tham khảo thêm tài liệu: Hóa học lớp 9, Giải bài tập Hóa học 9, Giải sách bài tập Hóa 9, Tài liệu học tập lớp 9, được cập nhật trên VnDoc để học tốt môn Hóa hơn.












