Giải Hóa 9 bài 4: Một số axit quan trọng
Giải bài tập Hóa 9 bài 4: Một số axit quan trọng hướng dẫn giải chi tiết cho từng bài tập trong SGK Hóa học 9 Bài 4 trang 19: Một số axit quan trọng. Tài liệu giúp cho các bạn học sinh ôn tập và củng cố các dạng bài tập, rèn luyện kỹ năng giải môn Hóa 9. Mời các bạn tham khảo.
Giải Hóa 9 bài 4: Một số axit quan trọng
I. Giải bài tập Hóa 9 bài 4: Một số axit quan trọng
Bài 1 Trang 19 SGK hóa 9
Có những chất: CuO, BaCl2 Zn, ZnO. Chất nào nói trên tác dụng với dung dịch HCl, dung dịch H2SO4 loãng sinh ra:
a) Chất khí cháy được trong không khí?
b) Dung dịch có màu xanh lam
c) Chất kết tủa màu trắng không tan trong nước và axit?
d) Dung dịch không màu và nước?
Viết tất cả các phương trình hóa học.
Đáp án và hướng dẫn giải
a) Khí cháy được trong không khí là hiđro
Zn + 2HCl → ZnCl2 + H2
Zn + H2SO4 → ZnSO4 + H2
b) Dung dịch có màu xanh lam là dung dịch muối đồng (II)
CuO + 2HCl → CuCl2 + H2O
CuO + H2SO4 → CuSO4 + H2O
c) Chất kết tủa trắng không tan trong nước và axit là BaSO4
BaCl2 + H2SO4 → 2HCl + BaSO4
d) Dung dịch không màu là muối kẽm.
ZnO + 2HCl → ZnCl2 + H2O
ZnO + H2SO4 → ZnSO4 + H2O
Bài 2 Trang 19 SGK hóa 9
Sản xuất axit sunfuric trong công nghiệp cần phải có những nguyên liệu chủ yếu nào? Hãy cho biết mục đích của mỗi công đoạn sản xuất axit sunfuric và dẫn ra những phản ứng hóa học.
Đáp án và hướng dẫn giải
* Trong công nghiệp axít sufuric được sản xuất từ nguyên liệu: lưu huỳnh (hoặc quặng pirit), không khí và nước.
* Mục đích của mỗi công đoạn và phương trình phản ứng:
Sản xuất SO2 bằng cách đốt S trong không khí:
S + O2 → SO2 (nhiệt độ)
Sản xuất SO3 bằng cách oxi hóa SO2:
2SO2 + O2 → SO3 (điều kiện: to, V2O5)
Sản xuất H2SO4 bằng cách cho SO3 tác dụng với nước:
SO3(k) + H2O(l) → H2SO4(dd)
Bài 3 Trang 19 SGK hóa 9
Bằng cách nào có thể nhận biết được từng chất trong mỗi cặp chất sau theo phương pháp hóa học?
a) Dung dịch HCl và dung dịch H2SO4
b) Dung dịch NaCl và dung dịch Na2SO4
c) Dung dịch Na2SO4 và H2SO4
Viết phương trình hóa học
Đáp án và hướng dẫn giải
a) Cho dung dịch muối bari hoặc Ba(OH)2, thí dụ BaCl2 vào hai ống nghiệm, mỗi ống chứa sẵn dung dịch HCl và H2SO4
Ở ống nghiệm nào xuất hiện kết tủa thì dung dịch chứa ban đầu là dung dịch H2SO4; ở ống nghiệm không thấy hiện tượng gì thì dung dịch chứa ban đầu là dung dịch HCl
BaCl2 + H2SO4 → 2HCl + BaSO4
b) Dùng thuốc thử như câu a thấy kết tủa là dung dịch Na2SO4 không có kết tủa là dung dịch NaCl
BaCl2 + Na2SO4 → 2NaCl + BaSO4
c) Có nhiều cách để nhận biết 2 dung dịch Na2SO4 và H2SO4 đơn giản nhất là dùng quỳ tím.
Cho quỳ tím vào từng dung dịch: dung dịch làm quỳ tím đối sang màu đỏ là dung dịch H2SO4, dung dịch không làm đổi màu quỳ tím là dung dịch muối Na2SO4.
Bài 4 Trang 19 SGK hóa 9
Bảng dưới đây cho biết kết quả của 6 thí nghiệm xảy ra giữa Fe và dung dịch H2SO4 loãng. Trong mỗi thí nghiệm người ta dùng 0,2 gam Fe tác dụng với thể tích bằng nhau của axit, nhưng có nồng độ khác nhau:
|
Thí nghiệm |
Nồng độ axit |
Nhiệt độ (oC) |
Sắt ở dạng |
Thời gian phản ứng xong (s) |
|
1 |
1M |
25 |
Lá |
190 |
|
2 |
2M |
25 |
Bột |
85 |
|
3 |
2M |
35 |
Lá |
62 |
|
4 |
2M |
50 |
Bột |
15 |
|
5 |
2M |
35 |
Bột |
45 |
|
6 |
3M |
50 |
Bột |
11 |
Những thí nghiệm nào chứng tỏ rằng:
a) Phản ứng xảy ra nhanh hơn khi tăng nhiệt độ?
b) Phản ứng xảy ra nhanh hơn khi tăng diện tích tiếp xúc?
c) Phản ứng xảy ra nhanh hơn khi tăng nồng độ axit?
Đáp án và hướng dẫn giải
So sánh các điều kiện: nồng độ axit, nhiệt độ của dung dịch H2SO4 loãng và trạng thái của sắt với thời gian phản ứng để rút ra:
a) Thí nghiệm 4 và thí nghiệm 5 chứng tỏ phản ứng xảy ra nhanh hơn khi tăng nhiệt độ của dung dịch H2SO4.
b) Thí nghiệm 3 và thí nghiệm 5 chứng tỏ phản ứng xảy ra nhanh hơn khi tăng diện tích tiếp xúc.
c) Thí nghiệm 4 và thí nghiệm 6 chứng tỏ phản ứng xảy ra nhanh hơn khi tăng nồng độ của dung dịch H2SO4.
Bài 5 Trang 19 SGK hóa 9
Hãy sử dụng những chất có sẵn: Cu, Fe, KOH, C6H12O6 (glucozơ), dung dịch H2SO4 loãng, H2SO4 đặc và những dụng cụ thí nghiệm cần thiết để làm những thí nghiệm chứng minh rằng:
a) Dung dịch H2SO4 loãng có những tính chất hóa học của axit
b) H2SO4 đặc có những tính chất hóa học riêng
Viết phương trình hóa học cho mỗi thí nghiệm.
Đáp án và hướng dẫn giải
a) Để chứng minh dung dịch H2SO4 loãng có những tính chất hóa học của axit, ta thực hiện các thí nghiệm:
Cho axit H2SO4 loãng lần lượt phản ứng với Fe, CuO, KOH:
Fe + H2SO4 → FeSO4 + H2 (có khí thoát ra)
(kim loại Cu không tác dụng với dd H2SO4 loãng)
CuO + H2SO4 → H2O + CuSO4 (dung dịch có màu xanh lam)
2KOH + H2SO4 → K2SO4 + 2H2O
(Cho quỳ tím vào dung dịch KOH, dung dịch có màu xanh. Rót từ từ dung dịch H2SO4 thấy màu xanh dần biến mất đến khi dung dịch không màu)
b) Để chứng minh dung dịch H2SO4 đặc có những tính chất hóa học riêng ta thực hiện các thí nghiệm:
Cho axit H2SO4 đặc tác dụng với Cu đun nóng và với glucozơ:
Cu + H2SO4 đ,nóng → CuSO4 + SO2 + H2O
(Đồng bị hòa tan dần, dung dịch chuyển sang màu xanh và có khí mùi hắc thoát ra)
C12H22O11 → 12C + 11H2O
(Đường bị hóa thành than và đẩy lên khỏi cốc)
Bài 6 Trang 19 SGK hóa 9
Cho một khối lượng mạt sắt dư vào 50 ml dung dịch HCl. Phản ứng xong, thu được 3,36 lít khí (đktc).
a) Viết phương trình hóa học;
b) Tính khối lượng mạt sắt đã tham gia phản ứng
c) Tìm nồng độ mol của dung dịch HCl đã dùng.
Đáp án và hướng dẫn giải
a) Số mol khí H2 = 3,36 : 22,4 = 0,15 mol
a) Phương trình phản ứng:
Fe + 2HCl → FeCl2 + H2
0,15 0,3 0,15 ← 0,15 (mol)
b) Khối lượng sắt đã phản ứng:
mFe = 0,15 . 56 = 8,4 g
c) Số mol HCl phản ứng:
nHCl = 0,3 mol; 50 ml = 0,05 lít
Nồng độ mol của dung dịch HCl: CM,HCl = 0,3/0,05 = 6M
Bài 7 Trang 19 SGK hóa 9
Hòa tan hoàn toàn 12,1 gam hỗn hợp bột CuO và ZnO cần 100 ml dung dịch HCl 3M.
a) Viết các phương trình hóa học.
b) Tính phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu.
c) Hãy tính khối lượng dung dịch H2SO4 nồng độ 20% để hòa tan hoàn toàn hỗn hợp các oxit trên.
Đáp án và hướng dẫn giải
Số mol HCl = 3 . 100/1000 = 0,3 mol
Gọi x, y là số mol của CuO và ZnO
a) Các phương trinh hóa học:
CuO + 2HCl → CuCl2 + H2O
Phản ứng: x → 2x x (mol)
ZnO + 2HCl → ZnCl2 + H2O
Pư: y → 2y y (mol)
b) Từ khối lượng của hỗn hợp và số mol HCl, ta lập hệ phương trình.
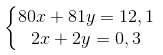
Giải (1) (2) ta được x = 0,05 mol = số mol CuO; y = 0,1 mol = số mol ZnO
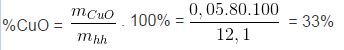
c) Vì CuO và ZnO phản ứng với H2SO4 theo cùng tỉ lệ mol, nên có thể coi hai oxit như một oxit có công thức chung là MO với số mol = x + y = 0,15 mol
MO + H2SO4 → MSO4 + H2O
Pư: 0,15 → 0,15 0,15 (mol)
mH2SO4 = 0,15 . 98 = 14,7 g
mdd H2SO4 20% = 14,7.100/ 20 = 73,5 g
>> Bài tiếp theo: Giải bài tập Hóa 9 bài 5: Luyện tập tính chất hóa học của oxit và axit
II. Nhắc lại lý thuyết hóa 9 bài 4
1. Axit clohidric
a. Tính chất hóa học (HCl có đầy đủ tính chất hóa học của axit)
Làm quỳ tím chuyển màu đỏ
Tác dụng với nhiều kim loại như: Mg, Al, Zn, Fe… tạo thành muối clorua và khí hidro.
Mg + 2HCl → MgCl2 + H2
Tác dụng với bazơ tạo thành muối clorua và nước.
HCl + NaOH → NaCl + H2O
Tác dụng với oxit bazơ tạo thành muối clorua và nước.
2HCl + CuO → CuCl2 + H2O
Tác dụng với muối → Muối clorua + axit
HCl + AgNO3 → AgCl + HNO3
b. Ứng dụng
- Điều chế các muối
- Làm sạch bề mặt kim loại trước khi hàn
- Tẩy gỉ kim loại trước khi tráng, sơn, mạ kim loại
- Chế biến thực phẩm, dược phẩm
2. Axit sunfuric
a. Tính chất vật lí
- Chất lỏng sánh, không màu.
- Nặng gấp gần 2 lần nước
- Không bay hơi
- Dễ tan trong nước, tỏa nhiều nhiệt.
Chú ý: Khi pha loãng axit sunfuric đặc: Rót từ từ axit đặc vào nước, khuấy đều. Tuyệt đối không làm ngược lại.
b. Tính chất hóa học
- Tính chất hóa học Axit H2SO4 loãng (H2SO4)
+ Làm đổi màu quỳ tím thành đỏ
+ Tác dụng với kim loại (Al, Fe, Zn, Mg,…) → muối sunfat + khí hidro
+ Tác dụng với bazơ → muối sunfat + nước
+ Tác dụng với oxit bazơ → muối sunfat + nước
+ Tác dụng với muối → muối (mới) + axit (mới)
- Tính chất hóa học Axit H2SO4 đặc
Có những tính chất hóa học riêng
+ Tác dụng với hầu hết các kim lọai trừ (Au, Pt) → muối sunfat, không giải phóng khí hidro
+ Tính háo nước trong phản ứng với đường
c. Ứng dụng
H2SO4 có rất nhiều ứng dụng quan trọng như: phẩm nhuộm, phân bón, chất tẩy rửa tổng hợp, chất dẻo, ắc quy.
d. Sản xuất axit sunfuric
Sơ đồ phản ứng: S → SO2 → SO3 → H2SO4
S ra SO2: Đốt lưu huỳnh trong không khí
S + O2 → SO2.
SO2 ra SO3: Oxi hóa SO2
2SO2 + O2 → 2SO3.
SO3 ra H2SO4: cho SO3 tác dụng với nước
SO3 + H2O → H2SO4
3. Nhận biết axit sunfuric và muối sunfat
a. Phân biệt H2SO4 và muối sunfat
- Dùng một số kim loại như: Mg, Zn, Al, Fe,…
- Axit phản ứng, có khí hidro thoát ra
- Muối không có khí thoát ra.
b. Nhận biết gốc sunfat
Dùng dung dịch muối BaCl2, Ba(NO3)2 hoặc Ba(OH)2 => hiện tượng: có kết tủa trắng
III. Giải sách bài tập hóa 9 bài 4: Một số axit quan trọng
Ngoài các dạng câu hỏi bài tập sách giáo khoa hóa 9 bài 4, để nâng cao củng cố cũng như vận dụng tốt kiến thức lý thuyết hóa 9 bài 4. Các bạn học sinh cần làm thêm các dạng câu hỏi bài tập sách bài tập hóa 9 bài 4. Để giúp bạn đọc nắm được các phương pháp giải bài tập. VnDoc đã biên soạn hướng dẫn bạn đọc giải bài tập
- SBT hóa 9 bài 4 tại: Giải Sách bài tập Hóa học 9 bài 4: Một số axit quan trọng
IV. Trắc nghiệm Hóa 9 bài 4: Một số axit quan trọng
.............................................
Ngoài Giải bài tập Hóa 9 bài 4: Một số axit quan trọng, các bạn học sinh còn có thể tham khảo các Trắc nghiệm Hóa học 9, Giải sách bài tập Hóa 9, Giải bài tập Hóa học 9 được cập nhật liên tục trên VnDoc để học tốt Hóa 9 hơn.
