Giải Hóa 9 Bài 19: Sắt
Giải Hóa 9 Bài 19: Sắt tổng hợp đáp án cho các câu hỏi trong SGK Hoá 9 bài 19 giúp các em nắm vững kiến thức được học trong bài, luyện giải Hoá 9 hiệu quả. Sau đây mời các bạn tham khảo chi tiết.
Giải bài tập Hóa 9 trang 60
A. Giải bài tập SGK Hóa 9 trang 60
Bài 1 trang 60 SGK Hóa 9
Sắt có những tính chất hoá học nào? Viết các phương trình hoá học minh hoạ.
Đáp án hướng dẫn giải chi tiết
1. Tác dụng với phi kim
a) Tác dụng với oxi.
3Fe + 2O2 ![]() \(\overset{t^{o} }{\rightarrow}\)Fe3O4 (oxit sắt từ, sắt có hóa trị II và III)
\(\overset{t^{o} }{\rightarrow}\)Fe3O4 (oxit sắt từ, sắt có hóa trị II và III)
b) Tác dụng với phi kim khác.
2Fe + 3Cl2 ![]() \(\overset{t^{o} }{\rightarrow}\) 2FeCl3
\(\overset{t^{o} }{\rightarrow}\) 2FeCl3
Lưu ý: Fe tác dụng với clo chỉ cho Fe(III) clorua (không cho Fe(II) clorua)
2. Tác dụng với dung dịch axit:
Sắt tác dụng với HCl, H2SO4 loãng tạo thành muối sắt (II) và giải phóng H2.
Fe + 2HCl → FeCl2 + H2 ↑
Bài 2 trang 60 SGK Hóa 9
Từ sắt và các hoá chất cần thiết, hãy viết các phương trình hoá học để thu được các oxit riêng biệt: Fe3O4, Fe2O3 và ghi rõ điều kiện phản ứng, nếu có.
Đáp án hướng dẫn giải chi tiết
a) 3Fe + 2O2 → Fe3O4
b) 2Fe + 3Cl2 → 2FeCl3
FeCl3 + 3NaOH → 3NaCl + Fe(OH)3
2Fe(OH)3 → Fe2O3 + 3H2O
Bài 3 trang 60 SGK Hóa 9
Có bột kim loại sắt lẫn tạp chất nhôm. Hãy nêu phương pháp làm sạch sắt.
Đáp án hướng dẫn giải chi tiết
Cho hỗn hợp vào dung dịch NaOH dư, nhôm bị hòa tan hết, còn sắt không phản ứng:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
Lọc bỏ dung dịch, chất rắn thu được là Fe.
Bài 4 trang 60 SGK Hóa 9
Sắt tác dụng được với chất nào sau đây?
a) Dung dịch muối Cu(NO3)2
b) H2SO4 đặc, nguội;
c) Khí Cl2
d) Dung dịch ZnSO4
Viết các phương trình hoá học và ghi điều kiện, nếu có.
Đáp án hướng dẫn giải chi tiết
Sắt tác dụng được với dung dịch Cu(NO3)2 và khí Cl2
Fe + Cu(NO3)2 —> Fe(NO3)2 + Cu
2Fe + 3Cl2 —> 2FeCl3
Bài 5 trang 60 SGK Hóa 9
Ngâm bột sắt dư trong 10 ml dung dịch đồng sunfat 1M. Sau khi phản ứng kết thúc, lọc được chất rắn A và dung dịch B.
a) Cho A tác dụng với dung dịch HCl dư. Tính khối iượng chất rắn còn lại sau phản ứng.
b) Tính thể tích dung dịch NaOH 1M vừa đủ để kết tủa hoàn toàn dung dịch B.
Đáp án hướng dẫn giải chi tiết
a) Số mol CuSO4 = 1.0,01 = 0,01 mol
Fe + CuSO4 → FeSO4 + Cu
Phản ứng: 0,01 0,01 → 0,01 0,01 (mol)
Chất rắn A gồm Cu và Fe dư, khi cho A vào dung dịch HCl dư chỉ có Fe phản ứng và bị hòa tan hết
Fe + 2HCl → FeCl2 + H2
Chất rắn còn lại là Cu = 0,01.64 = 0,64 gam
b) Dung dịch В có FeSO4 + NaOH?
FeSO4 + 2NaOH → Na2SO4 + Fe(OH)2
Phản ứng: 0,01 → 0,02 0,01 0,01 (mol)
VddNaOH = n/CM = 0,02/1 = 0,02 lít = 20ml
>> Bài tiếp theo: Giải Hóa 9 Bài 20: Hợp kim sắt: Gang, thép
B. Tóm tắt lý thuyết Hóa 9 bài 19
1. Tính chất vật lý
Sắt là kim loại màu trắng xám, đôi khi có dạng bột màu đen. Sắt có tính nhiễm từ (bị nam châm hút và sắt cũng có thể nhiễm từ trở thành nam châm). Khối lượng riêng D = 7,86g/cm3, nóng chảy ở 1539°C. Sắt dẻo nên dễ rèn.
2. Tính chất hóa học
Sắt là kim loại có hóa trị II và III.
a. Tác dụng với phi kim
- Tác dụng với oxi.
3Fe + 2O2 → Fe3O4 (oxit sắt từ, sắt có hóa trị II và III)
- Tác dụng với phi kim khác.
2Fe + 3Cl2 → 2FeCl3
b. Tác dụng với dung dịch axit:
- Sắt tác dụng với HCl, H2SO4 loãng tạo thành muối sắt (II) và giải phóng Hg.
Fe + 2HCl → FeCl2, + H2
- Chú ý: Sắt không tác dụng với HNO3, H2SO4 đặc, nguội.
c. Tác dụng với dung dịch muối của kim loại yếu hơn sắt.
Fe + CuSO4 -> FeSO4 + Cu
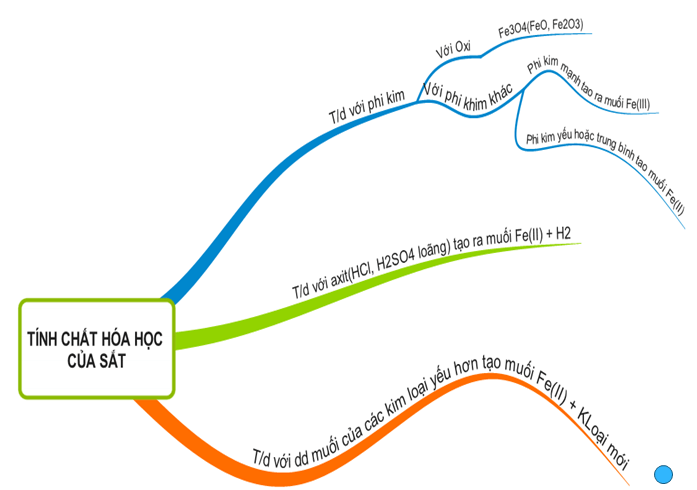
3. Sơ đồ tư duy
C. Giải SBT Hóa 9 bài 19
Để hỗ trợ bạn đọc trong quá trình học tập cũng như làm bài tập. VnDoc đã hương dẫn các bạn học sinh giải bài tập sách bài tập chi tiết tại: Giải Sách bài tập Hóa học 9 bài 19: Sắt
D. Bài tập trắc nghiệm Hóa 9 bài 19
Câu 1. Thực hiện các thí nghiệm sau:
(1) Đốt dây sắt trong bình khí clo dư
(2) Cho Fe vào dung dịch HNO3 đặc, nguội
(3) Cho Fe vào dung dịch HCl loãng, dư
(4) Cho Fe vào dung dịch HCl loãng, dư
(5) Cho Fe vào dung dịch H2SO4 đặc, nóng
Số thí nghiệm tạo ra muối Fe(II) là:
A. 3
B. 4
C. 2
D. 1
Câu 2. Sắt có tính chất vật lý nào dưới đây:
A. Màu trắng bạc, nhẹ, có ánh kim, dẫn điện và dẫn nhiệt kém.
B. Màu trắng bạc, nặng, có ánh kim, dẫn điện, dẫn nhiệt tốt
C. Màu trắng xám, nặng, có ánh kim, dẫn điện và dẫn nhiệt tốt
D. Màu trắng xám, nhẹ, có ánh kim, dẫn điện và dẫn nhiệt tốt.
Câu 3. Kim loại Fe không phản ứng được với
A. Dung dịch HCl
B. Dung dịch H2SO4 loãng
C. Dung dịch CuCl2
D. H2SO4 đặc, nguội
Câu 4. Để nhận biết sự có mặt của Fe trong hỗn hợp gồm Fe và Ag có thể dùng dung dịch nào
A. HCl
B. AgNO3
C. H2SO4 đặc, nguội
D. NaOH
Câu 5. Kim loại nào dưới đây không đẩy được Fe ra khỏi dung dịch muối FeSO4
A. Al
B. Zn
C. Cu
D. Mg
Câu 6. Cặp kim loại nào dưới đây đều phản ứng với dung dịch HCl, giải phóng khí H2
A. (Cu, Ag)
B. (Ag, Zn)
C. (Cu, Fe)
D. (Mg, Zn)
Câu 7. Một hợp chất có chứa 27,59% oxi về khối lượng, còn lại là Fe. Công thức của oxit sắt đó là:
A. FeO
B. Fe2O3
C. Fe3O4
D. Fe(OH)2
Để củng cố kiến thức nội dung bài học trên lớp, cũng như rèn luyện bổ sung kiến thức bài học. VnDoc đã biên soạn tổng hợp bộ câu hỏi trắc nghiệm hóa 9 bài 19 gồm 15 câu hỏi trắc nghiệm khách quan kèm đáp án hướng dẫn giải chi tiết tại:
............................
Ngoài Giải Hóa 9 Bài 19: Sắt, mời các bạn tham khảo thêm Giải bài tập Hóa học 9, Lý thuyết Hóa học 9, Tài liệu học tập lớp 9 mà VnDoc tổng hợp và đăng tải.

