Xác định biểu thức tính tốc độ trung bình của phản ứng
Cho phản ứng xảy ra trong pha khí sau: H2 + Cl2 ![]() 2HCl
2HCl
Biểu thức tốc độ trung bình của phản ứng là:
H2 + Cl2 2HCl
Biểu thức tốc độ trung bình của phản ứng là:
Cùng nhau thử sức với bài kiểm tra 15 phút Hóa 10 Chương 6: Tốc độ phản ứng.
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Xác định biểu thức tính tốc độ trung bình của phản ứng
Cho phản ứng xảy ra trong pha khí sau: H2 + Cl2 ![]() 2HCl
2HCl
Biểu thức tốc độ trung bình của phản ứng là:
H2 + Cl2 2HCl
Biểu thức tốc độ trung bình của phản ứng là:
Tìm nhận định đúng
Nhận định nào sau đây là đúng?
Nghiền nhỏ vừa phải CaCO3 giúp phản ứng nung vôi xảy ra dễ dàng hơn đúng vì khi nghiền nhỏ CaCO3 làm cho diện tích tiếp xúc lớn hơn
tốc độ phản ứng tăng
phản ứng nung vôi xảy ra dễ dàng hơn.
Phản ứng xảy ra nhanh
Trong các phản ứng hóa học sau, phản ứng nào xảy ra nhanh?
Phản ứng có tốc độ phản ứng lớn nhất
Trong các cặp phản ứng sau, nếu lượng Fe trong các cặp đều được lấy bằng nhau và có kích thước như nhau thì cặp nào có tốc độ phản ứng lớn nhất?
Ở phản ứng Fe + dung dịch HCl 0,5 M, HCl có nồng độ lớn nhất Tốc độ phản ứng lớn nhất.
Tính thời gian phân hủy khi phân huỷ cùng một lượng hydrogen peroxide
Enzyme catalase phân huỷ hydrogen peroxide thành oxygen và nước nhanh gấp khoảng 107 lần sự phân huỷ khi không có xúc tác. Giả sử một phản ứng không có xúc tác phân huỷ một lượng hydrogen peroxide mất 360 ngày, hãy tính thời gian (theo giây) cho sự phân huỷ cùng một lượng hydrogen peroxide đó khi sử dụng enzyme catalase làm xúc tác.
Thời gian phân hủy (theo giây) khi phân huỷ cùng một lượng hydrogen peroxide đó, sử dụng enzyme catalase làm xúc tác là:
t = 360.24.60.60.10-7 = 3,11 (giây).
Tính số tác động làm tăng tốc độ phản ứng
Cho phản ứng hóa học sau:
Na2S2O3(aq) + H2SO4(aq) ![]() Na2SO4(aq) + SO2(g) + S(s) + H2O(aq)
Na2SO4(aq) + SO2(g) + S(s) + H2O(aq)
Tác động vào phản ứng một trong các yếu tố (các yếu tố còn lại giữ nguyên):
(1) Tăng nhiệt độ.
(2) Tăng nồng độ Na2S2O3.
(3) Giảm nồng độ H2SO4.
(4) Giảm nồng độ Na2SO4.
(5) Giảm áp suất của SO2.
Số tác động làm tăng tốc độ của phản ứng là:
Na2S2O3(aq) + H2SO4(aq) Na2SO4(aq) + SO2(g) + S(s) + H2O(aq)
V = kCNa2S2O3.CH2SO4
Khi thay đổi một trong các yếu tố (giữ nguyên các yếu tố khác):
(1) Tăng nhiệt độ Làm tăng tốc độ phản ứng
(2) Tăng nồng độ Na2S2O3 Làm tăng tốc độ phản ứng
(3) Giảm nồng độ H2SO4 Làm giảm tốc độ phản ứng
(4) Giảm nồng độ Na2SO4 không ảnh hưởng tới tốc độ phản ứng
(5) Giảm áp suất của SO2 không ảnh hưởng tới tốc độ phản ứng
Tính giá trị của t
Hệ số nhiệt độ của một phản ứng là 4. Ở toC tốc độ của phản ứng đo được là 5.10-3 mol.L-1.s-1; còn ở 150oC tốc độ của phản ứng đo được là 3,215.10-4 mol.L-1.s-1. Giá trị của t là
Ta có biểu thức:
Tốc độ phản ứng
Cho phản ứng hóa học có dạng: A + B → C.
Tốc độ phản ứng thay đổi như thế nào khi nồng độ A tăng 2 lần, giữ nguyên nồng độ B là:
Phản ứng: A + B → C.
Ta có: v = k.[A].[B]
Khi [A] tăng 2 lần thì: va = k.[2A].[B] = 2k.[A].[B] = 2v
Vậy tốc độ phản ứng tăng lên 2 lần.
Cách làm củ khoai tây nhanh chín nhất
Cách làm nào sau đây sẽ làm củ khoai tây nhanh chín nhất?
Nhiệt độ càng cao thì tốc độ phản ứng càng nhanh.
Nướng ở 180oC sẽ làm củ khoai nhanh chín nhất.
Khí được bơm vào các túi đựng thực phẩm trước khi đóng gói
Để hạn chế sự ôi thiu thực phẩm do các phản ứng của oxygen cũng như sự hoạt động của vi khuẩn, người ta thường bơm khí nào sau đây vào các túi đựng thực phẩm trước khi đóng gói?
Thực phẩm bị ôi thiu do các phản ứng oxi hóa của oxygen cũng như hoạt động của vi khuẩn. Để hạn chế sự ôi thiu, người ta bơm khí N2 hoặc CO2 vào túi đựng thực phẩm trước khi đóng gói. Khi đó nồng độ khí oxygen sau khi bơm N2 hoặc CO2 chỉ còn 2 – 5%.
Yếu tố ảnh hưởng đến tốc độ phản ứng
Cho hiện tượng sau: Tàn đóm đỏ bùng lên khi cho vào bình oxygen nguyên chất.
Hiện tượng trên thể hiện ảnh hưởng của yếu tố nào đến tốc độ phản ứng?
Khi cho tàn đóm vào bình oxygen nguyên chất ⇒ nồng độ oxygen tăng cao ⇒ tốc độ phản ứng tăng ⇒ tàn đóm đỏ bùng cháy.
Vậy yếu tố ảnh hưởng đến tốc độ phản ứng trong trường hợp trên là nồng độ.
Ảnh hưởng của diện tích bề mặt đến tốc độ phản ứng
Việc làm nào dưới đây thể hiện sự ảnh hưởng của diện tích bề mặt đến tốc độ phản ứng: CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Nếu kích thước hạt càng nhỏ thì tổng diện tích bề mặt càng lớn dẫn đến số va chạm hiệu quả tăng làm cho tốc độ phản ứng tăng.
Vì vậy, có thể tăng diện tích tiếp xúc bằng cách đập nhỏ đá vôi thành dạng hạt.
Tìm phát biểu đúng
Thực hiện 2 thí nghiệm theo hình vẽ sau:
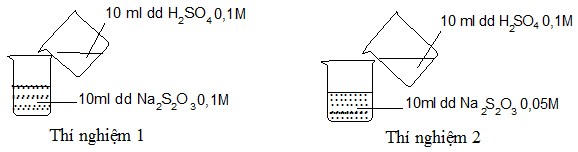
Phát biểu nào sau đây là đúng?
Sử dụng yếu tố nồng độ, thí nghiệm 1, nồng độ Na2S2O3 lớn hơn, tốc độ phản ứng xảy ra nhanh hơn Thí nghiệm 1 có kết tủa xuất hiện trước.
Tốc độ phản ứng không phụ thuộc vào yếu tố
Tốc độ phản ứng không phụ thuộc vào yếu tố
Tốc độ phản ứng không phụ thuộc vào yếu tố thời gian xảy ra phản ứng.
So sánh tốc độ của 2 phản ứng
So sánh tốc độ của 2 phản ứng sau (thực hiện ở cùng nhiệt độ):
(1) Zn (bột) + dung dịch CuSO4 1M
(2) Zn (hạt) + dung dịch CuSO4 1M
Kết quả thu được là:
Sử dụng yếu tố diện tích tiếp xúc:
Ở thí nghiệm (1) Zn dạng bột sẽ làm tăng diện tích tiếp xúc, tốc độ phản ứng xảy ra nhanh hơn so với thí nghiệm (2).
Sự cháy chịu ảnh hưởng của yếu tố
Than củi đang cháy, dùng quạt thổi thêm không khí vào, sự cháy diễn ra mạnh hơn chịu ảnh hưởng của yếu tố nào?
Ảnh hưởng bởi yếu tố nồng độ. Than cháy luôn cần oxygen để duy trì sự cháy, khi thổi không khí vào, làm tăng nồng độ oxygen, than cháy mạnh hơn.
Yếu tố làm tăng tốc độ phản ứng
Chẻ củi nhỏ khi đốt để nhanh cháy hơn là vận dụng yếu tố làm tăng tốc độ phản ứng nào sau đây?
Chẻ củi nhỏ khi đốt để nhanh cháy hơn là vận dụng yếu tố diện tích bề mặt để làm tăng tốc độ phản ứng.
Tính chất của sự va chạm
Tăng nhiệt độ của một hệ phản ứng sẽ dẫn đến sự va chạm có hiệu quả giữa các phân tử chất phản ứng. Tính chất của sự va chạm đó là:
Khi tăng nhiệt độ của một hệ phản ứng sẽ dẫn đến sự va chạm có hiệu quả giữa các phân tử chất phản ứng là tăng tốc.
độ phản ứng, nhưng khi đến một lúc nào đó, thì sự chạm có hiệu quả đó sẽ giảm dần do các chất đã kết hợp với nhau thành sản phẩm.
Yếu tố không ảnh hưởng đến tốc độ phản ứng
Cho phản ứng hóa học sau:
2H2O2(l) ![]() 2H2O(l) + O2(l)
2H2O(l) + O2(l)
Yếu tố nào sau đây không ảnh hưởng đến tốc độ của phản ứng trên?
Yếu tố không ảnh hưởng đến tốc độ của phản ứng là áp suất vì chất tham gia không có chất khí.
Yếu tố đã ảnh hưởng đến tốc độ phản ứng
Cho 2 quá trình:
(1) Zinc dạng bột phản ứng với dung dịch hydrochloric acid nhanh hơn so với Zinc dạng lá.
(2) Để thực phẩm trong tủ lạnh giúp cho thực phẩm dược tươi lâu hơn.
Yếu tố nào đã ảnh hưởng đến tốc độ phản ứng của 2 quá trình trên?
(1) Zinc dạng bột phản ứng với dung dịch hydrochloric acid nhanh hơn so với Zinc dạng lá ⇒ Diện tích tiếp xúc
(2) Để thực phẩm trong tủ lạnh giúp cho thực phẩm dược tươi lâu hơn ⇒ Nhiệt độ
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: