Chất nào sau đây dùng làm đèn xì hàn
Chất nào sau đây dùng làm đèn xì hàn, cắt kim loại?
Khí được ứng dụng trong đèn xì để hàn cắt kim loại là: Acetylene.
Đề kiểm tra 15 phút Hóa 11 Chương 4 Hydrocarbon sách Kết nối tri thức giúp bạn học tổng hợp lại kiến thức của cả nội dung chương. Cùng nhau luyện tập nha!
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Chất nào sau đây dùng làm đèn xì hàn
Chất nào sau đây dùng làm đèn xì hàn, cắt kim loại?
Khí được ứng dụng trong đèn xì để hàn cắt kim loại là: Acetylene.
Butane phản ứng với chlorine
Cho butane phản ứng với chlorine thu được sản phẩm chính là
Butane phản ứng với chlorine thu được sản phẩm chính là 2-chlorobutane vì ở trường hợp này Cl thế vị trí của nguyên tử H ở C2 là carbon bậc cao hơn.
Xác định công thức Alkane
Alkane X có công thức phân tử C5H12. Xác định tên gọi của X, biết X chỉ có thể tạo ra một dẫn xuất monochloro duy nhất.
X chỉ có thể tạo ra một dẫn xuất monochloro duy nhất do đó chỉ có thể là:
2,2 – dimethylpropane.

Tìm sản phẩm và số mol
Cho hỗn hợp gồm 2 mol C6H6 và 3 mol Cl2, trong điều kiện có xúc tác bột Fe, to, hiệu suất 100%. Sau phản ứng sản phẩm thu được chất gì và bao nhiêu mol?
Sản phẩm thu được là C6H5Cl và C6H4Cl2.
Gọi số mol của C6H5Cl và C6H4Cl2 lần lượt là x, y:
C6H6 + Cl2 C6H5Cl + HCl
x x x x
C6H6 + 2Cl2 C6H4Cl2 + 2HCl
y 2y y 2y
Ta có hệ:
Dãy chất thuộc đồng đẳng của methane
Dãy nào sau đây chỉ gồm các chất thuộc dãy đồng đẳng của methane?
Số đồng phân anken C4H8 tác dụng HCl
Ứng với công thức phân tử C4H8 có bao nhiêu đồng phân alkene khi tác dụng với dung dịch HCl chỉ cho một sản phẩm hữu cơ duy nhất?
HCl là tác nhân bất đối xứng, để anken C4H8 cộng HCl cho 1 sản phẩn hữu cơ duy nhất thì C4H8 phải đối xứng
Công thức cấu tạo:
CH3-CH=CH-CH3 có đồng phân hình học nên tính là 2 alkene.
Tìm CTPT hai anken
Thực hiện phản ứng phân hủy bằng nhiệt hoàn toàn 0,1 mol hỗn hợp X chứa hai chất là đồng đẳng liên tiếp của anken ta thu được CO2 và H2O có khối lượng hơn kém nhau là 6,76 gam. Tìm công thức phân tử của 2 anken có trong phản ứng?
Đốt cháy hoàn toàn anken thu được số mol CO2 và H2O bằng nhau nên:
Gọi nCO2 = nH2O = x mol
mCO2 – mH2O = 44x – 18x = 6,76 ⇒ x = 0,26 mol
⇒ số C trung bình = 0,26/0,1 = 2,6
⇒ công thức phân tử của 2 anken là C2H4 và C3H6
Tìm phát biểu không đúng
Phát biểu nào sau đây là không đúng?
Có chất trong phân tử có vòng benzene nhưng không là hydrocarbon thơm.
Ví dụ: potassium benzoate.
Iso-propylbezene còn gọi
Iso-propylbezene còn gọi là:
Iso-propylbezene còn gọi là cumene
Để làm sạch ethylene phải dùng hoá chất
Khi điều chế ethylene trong phòng thí nghiệm từ ethyl alcohol với xúc tác sulfuric acid đặc ở nhiệt độ trên 170oC thì khí ethylene thu được thường có lẫn các oxide như CO2 và SO2. Để làm sạch ethylene phải dùng hoá chất nào dưới đây?
NaOH có tính kiềm mạnh nên hấp thụ rất tốt những oxide acid như CO2 và SO2.
Ở nội dung câu hỏi này không phải là phân biệt CO2 và SO2 nên ta không dung Br2 và KMnO4.
Giá trị của V
Khi đốt cháy hoàn toàn V lít hỗn hợp khí CH4, C2H6, C3H8 (đkc) thu được 5,28 gam CO2 và 3,456 gam H2O. Giá trị của V là:
nCO2 = 5,28 : 44 = 0,12 mol
nH2O = 3,456 : 18 = 0,192 mol
Hỗn hợp khí CH4, C2H6, C3H8 đều là alkane
⇒ nalkane = nH2O - nCO2 = 0,192 - 0,12 = 0,072 mol
Valkane = 0,072.24,79 = 1,78488 L
Tính số liên kết σ
Số liên kết σ trong mỗi phân tử propene; acetylene; isoprene lần lượt là
Propene: CH2=CH-CH3 gồm 1 liên kết π và 8 liên kết σ.
Acetylene: CHCH gồm 2 liên kết π và 3 liên kết σ.
Isoprene: CH2=C(CH3)-CH=CH2 gồm 2 liên kết π và 12 liên kết σ.
Chất tác dụng với AgNO3/NH3
Chất nào sau đây tác dụng với dung dịch AgNO3 trong NH3 tạo kết tủa?
Xác định alkane
Phần trăm khối lượng carbon trong phân tử alkane Y bằng 83,33%. Công thức phân tử của Y là
Gọi công thức phân tử của ankan Y có dạng CnH2n+2:
n = 5
Công thức phân tử của Y là C5H12.
Công thức của hai hydrocarbon
Hỗn hợp X gồm một ankan và một alkene. Cho X tác dụng với 3,4706 lít hydrogen tới phản ứng hoàn toàn thu được hỗn hợp Y gồm 2 khí trong đó có hydrogen dư và một hydrocarbon. Đốt cháy hoàn toàn hỗn hợp Y rồi dẫn hỗn hợp khí và hơi sinh ra vào bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 13,52 gam đồng thời có 16 gam kết tủa được tạo thành. Chất khí được đo ở điều kiện tiêu chuẩn. Công thức của hai hydrocarbon là:
nH2 = 3,4706 : 24,79 = 0,14 mol
Công thức Alkane và Alkene lần lượt CnH2n+2 và CnH2n ( n > 2)
Hydrocarbon trong Y là CnH2n+2 x mol và y mol H2. Ta có:
Khi đốt cháy hỗn hợp Y ta thu được: nx mol CO2 và (nx + x + y) mol H2O.
Từ đây ta có:
nx = 16 : 100 = 0,16 mol
Khối lượng bình tăng là tổng khối lượng của CO2 và H2O.
44nx + 18(nx + x + y) = 13,52
⇒ x + y = 0,2
⇒ Số mol alkane ban đầu là: 0,2 – 0,14 = 0,06 ⇒ 0,6 < x < 0,2.
Vậy 0,8 = 0,16 : 0,2 < n < 0,16 : 0,06 = 2,67
Vậy n = 2. Công thức hai hydrocarbon là C2H6 và C2H4.
Tên gọi hợp chất hữu cơ X
Tên của hợp chất hữu cơ X có công thức cấu tạo như sau là:
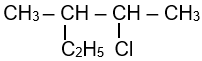

2-chloro-3-methylpentane
Alkane mạch phân nhánh
Alkane mạch phân nhánh chứa nguyên tử carbon:
Alkane mạch phân nhánh chứa nguyên tử carbon liên kết với ba hoặc bốn nguyên tử carbon khác
Xác định các chất là đồng đẳng của alkane
Trong các chất sau:
(1) C4H8 (2) C3H8
(3) CH4 (4) C5H12
(5) C3H6 (6) C2H4
(7) C6H14
Các chất thuộc dãy đồng đẳng của alkane là:
Các chất thuộc dãy đồng đẳng của alkane có công thức chunng là CnH2n+2.
Các chất thõa mãn: (2) C3H8; (3) CH4; (4) C5H12; (7) C6H14.
Chất làm mất màu dung dịch Br2
Chất nào sau đây làm mất màu dung dịch Bromine?
Ethylene là hydrocarbon không no nên có phản ứng cộng với Br2, làm mất màu Bromine.
CH2=CH2 + Br2 → CH2Br−CH2Br
Đồng phân hình học
Chất nào sau đây có đồng phân hình học:
Trong phân tử của hai alkenen CH3-CH2-CH=CH-CH 2-CH3, ta thấy nguyên tử C trong liên kết đôi liên kết với hai nhóm thế khác nhau nên chúng có đồng phân hình học.
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: