Tên gọi CH3-CH(C2H5)-CH2-CHO
Tên gọi của hợp chất với công thức cấu tạo CH3-CH(C2H5)-CH2-CHO là:
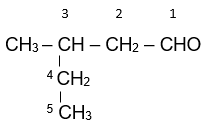
3-methylpentanal.
Cùng nhau thử sức với bài kiểm tra 45 phút Hóa 11 Chương 6: Hợp chất Carbonyl – Carboxylic acid nha!
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Tên gọi CH3-CH(C2H5)-CH2-CHO
Tên gọi của hợp chất với công thức cấu tạo CH3-CH(C2H5)-CH2-CHO là:
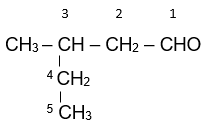
3-methylpentanal.
Dãy các chất có thứ tự nhiệt độ sôi tăng dần
Dãy nào sau đây có các chất được sắp xếp theo thứ tự tăng dần nhiệt độ sôi
Nhiệt độ sôi của carboxylic acid cao hơn nhiệt độ sôi của alcohol, aldehyde, ketone tương ứng vì có liên kết hydrogen giữa 2 phân tử hoặc giữa nhiều phân tử.
Tính thể tích dung dịch NaOH 2M cần để trung hoà
Một loại giấm ăn có chứa hàm lượng 4,5% acetic acid về thể tích. Tính thể tích dung dịch NaOH 2M cần để trung hoà hết 5 L giấm trên, biết khối lượng riêng của acetic acid là D = 1,05 g/mL.
Thể tích acetic acid có trong 5 L giấm ăn:
VCH3COOH = 5.4,5% = 0,225 (L) = 225 (mL)
Khối lượng acetic acid tương ứng là:
mCH3COOH = 225.1,05 = 236,25 (g)
Phương trình phản ứng:
CH3COOH + NaOH → CH3COONa + H2O
Tìm giá trị của m
X có CTPT C20H36Om. Biết X là một aldehyde no, mạch hở. Giá trị của m là
Ta có X là một aldehyde no, mạch hở nên X chỉ chứa liên kết π ở nhóm chức CHO:
Độ bất bão hòa trong X:
m = 3
Công thức của X và Y
X và Y có cùng công thức phân tử C3H4O2. Cho X tác dụng với CaCO3 thấy có bọt khí thoát ra, còn Y có thể tham gia phản ứng tráng bạc. Công thức của X và Y lần lượt là:
X phản ứng được với CaCO3 thì công thức cấu tạo là Carboxylic acid
2CH2=CHCOOH + CaCO3 (CH2CHCOO)2Ca + CO2 + H2O
HOC-CH2-CHO + 2Ag2O HOOCCH2COOH + 4Ag
Hợp chất không tham gia phản ứng iodoform
Hợp chất nào sau đây có phản ứng tạo iodoform?
Phản ứng tạo iodoform là phản ứng của hợp chất chứa nhóm methyl ketone (CH3CO-R) với iodine trong môi trường kiềm tạo kết tủa iodoform màu vàng.
Tìm nhận xét đúng
Nhận xét nào sau đây là đúng?
Formaldehyde là hợp chất carbonyl mạch ngắn tan tốt trong nước là do tạo được liên kết hydrogen với nước.
Tìm phát biểu sai
Phát biểu nào sai trong các phát biểu sau?
Các hợp chất carbonyl mạch ngắn tan tốt trong nước nhờ tạo liên kết hydrogen với nước. Ví dụ: Acetaldehyde, acetone,...
Tính nồng độ % HCHO
Cho 1,97 gam dung dịch Formaldehyde tác dụng với dung dịch AgNO3/NH3 dư thu được 10,8 gam Ag. Nồng độ % của Formaldehyde là:
nAg = 10,8 : 108 = 0,1 mol
Phương trình phản ứng hóa học
HCH=O + 4AgNO3 + 6NH3 + 2H2O → (NH4)2CO3 + 4Ag↓ + 4NH4NO3
nHCHO = 1/4nAg = 0,025 mol
→ mHCHO = 0,025.30 = 0,75 gam
Vậy nồng độ % của Formaldehyde trong dung dịch là:
C%HCHO = 0,75:1,97.100% = 38,07%
Chất có độ tan trong nước kém nhất
Trong các hợp chất HCHO, CH3CHO, CH3COCH3 và CH3CH2CH2CHO, hợp chất có độ tan trong nước kém nhất là
Hợp chất carbonyl mạch ngắn tan tốt trong nước là do tạo được liên kết hydrogen với nước. Khi số nguyên tử carbon trong gốc hydrocarbon tăng, khả năng tan của hợp chất carbonyl giảm xuống.
⇒ CH3CH2CH2CHO có độ tan trong nước kém nhất trong 4 chất.
Tính nồng độ phần trăm
Cho 3,94 gam dung dịch formalin tác dụng với dung dịch AgNO3/NH3 dư thu được 21,6 gam Ag. Nồng độ phần trăm của aldehyde formic trong formalin là:
nAg = 0,2 mol
HCHO + 2H2O + 4AgNO3 + 6NH3 → (NH4)2CO3 + 4Ag + 4NH4NO3
0,05 ← 0,2
Hợp chất phản ứng với HCN
Trong các hợp chất dưới đây, hợp chất nào phản ứng được với HCN cho sản phẩm là cyanohydrin
Hydrogen cyanide (HCN) phản ứng được với aldehyde hoặc ketone tạo thành sản phẩm là các cyanohydrin.
CH3-CH=O + HCN → CH3-CH(CN)-OH
Alcohol bị oxi hóa tạo ketone
Alcohol nào sau đây bị oxi hóa tạo ketone?
Alcohol bậc II bị oxi hóa tạo thành ketone.
Phương trình phản ứng minh họa
CH3 -CH(OH)-CH3 + CuO CH3 -CO-CH3 + Cu + H2O
Hợp chất tham gia phản ứng tạo iodoform
Trong các hợp chất sau, hợp chất nào tham gia phản ứng tạo iodoform?
Hiện tượng quan sát được
Cho aldehyde formic vào dung dịch chứa AgNO3 trong NH3, hiện tượng sau phản ứng quan sát được là:
Phương trình phản ứng minh họa
HCHO + 4AgNO3 + 6NH3 + 2H2O → 4Ag + 4NH4NO3 + (NH4)2CO3
Hiện tượng là tạo kết tủa màu trắng xám của kim loại bạc, bám vào thành ống nghiệm, có thể soi gương được.
Xác định công thức tổng quát của aldehyde
Đốt cháy hoàn toàn một aldehyde cho CO2 và H2O có số mol bằng nhau. Aldehyde đó có công thức tổng quát là:
Đốt cháy aldehyde X thu được nCO2 = nH2O X là aldehyde no, mạch hở, đơn chức.
Aldehyde đó có công thức tổng quát là: CnH2n+1CHO.
Tìm phát biểu không đúng
Phát biểu nào sau đây là không đúng?
Trong phân tử aldehyde có chứa nhóm -CHO. Trong nhóm -CHO nguyên tử carbon liên kết với nguyên tử oxygen bằng 1 liên kết bền và 1 liên kết
kém bền.
Xác định tên gọi của acid X
Trong phân tử carboxylic acid X có số nguyên tử carbon bằng số nhóm chức. Đốt cháy hoàn toàn một lượng X thu được số mol CO2 bằng số mol H2O. Tên gọi của X là
Vì đốt cháy X thu được nCO2 = nH2O X có dạng CnH2nOz
Số nguyên tử C = số nhóm chức số O trong X gấp đôi số C
X có dạng: CnH2nO2n
Với n = 1 X là CH2O2
X là formic acid: HCOOH
Với n = 2 X là C2H4O4 (không thỏa mãn)
Tính khối lượng Ag
Cho hỗn hợp A gồm 2 aldehyde là aldehyde formic và aldehyde acetic có số mol lần lượt là 0,01 mol, 0,01 mol vào dung dịch AgNO3 trong NH3 dư đun nóng. Sau khi phản ứng xảy ra hoàn toàn khối lượng Ag thu được là:
Ta có:
Aldehyde formic: HCHO → 4Ag
Aldehyde acetic: CH3CHO → 2Ag
Theo sơ đồ phản ứng ta có
nAg = 4.nHCHO + 2.nCH3CHO
⇔ 4.0,01 + 2.0,01 = 0,06 mol
⇒mAg = 0,06.108 = 6,48 gam
Tính giá trị của H
Oxi hóa 1,8 gam HCHO thành acid tương ứng với hiệu suất H% thu được hỗn hợp X. Cho X tham gia hết vào phản ứng tráng bạc thu được 16,2 gam bạc. Giá trị của H là
nHCHO = 0,06 mol
Gọi số mol HCHO phản ứng là x mol
nAg = 2 nHCOOH + 4nHCHO dư = 2x + 4.(0,06 -x) = 0,15
x = 0,045 mol
Chất tác dụng được với NaHCO3 tạo khí CO2
Chất nào sau đây tác dụng được với NaHCO3 tạo khí CO2?
Acetic acid là acid hữu cơ tác dụng được với NaHCO3 tạo khí CO2:
CH3COOH + NaHCO3 → CH3COONa + CO2↑ + H2O
Xác định công thức của 2 acid
Cho 16,4 gam hỗn hợp X gồm 2 carboxylic acid là đồng đẳng kế tiếp nhau phản ứng hoàn toàn với 200 ml dung dịch NaOH 1M và KOH 1M, thu được dung dịch Y. Cô cạn dung dịch Y, thu được 31,1 gam hỗn hợp chất rắn khan. Công thức của 2 acid trong X là
Gọi công thức tổng quát của hai acid trong hỗn hợp X là :
nNaOH = 0,2 mol; nKOH = 0,2 mol
Áp dụng định luật bảo toàn khối lượng:
mX + mNaOH + mKOH = mchất rắn + mH2O
mH2O = 4,5 gam
nH2O = 0,25 mol
2 acid là CH3COOH và C2H5COOH.
Xác định dãy chất là đồng phân
Trong những chất sau đây, dãy các chất là đồng phân của nhau là
Dãy các chất đồng phân của nhau là C2H5OH, CH3OCH3 (cùng 1 công thức phân tử).
Tính số aldehyde 2 chức có công thức C2H3O
Có bao nhiêu aldehyde 2 chức có công thức đơn giản nhất là C2H3O?
Aldehyde 2 chức có 2 nhóm –CHO phân tử có 2 nguyên tử O
Công thức phân tử là: C4H6O2
Có 2 công thức thỏa mãn là:
OHC-CH2-CH2-CHO
CH3-CH(CHO)2
Xác định X, Y
Cho sơ đồ chuyển hóa sau: Tinh bột → X → Y → acetic acid. X và Y lần lượt là:
X là glucose; Y là ethanol:
Các phương trình phản ứng xảy ra:
(C6H10O5)n + nH2O nC6H12O6
C6H12O6 2C2H5OH + 2CO2
C2H5OH + O2 CH3COOH + H2O
Đặc điểm đúng về phản ứng ester hoá
Đặc điểm nào sau đây là của phản ứng ester hoá?
Phản ứng ester hóa diễn ra thuận nghịch, cần chất xúc tác, đun nóng để phản ứng xảy ra nhanh hơn.
Đồng phân của acid và ester C4H6O2
Số đồng phân cấu tạo mạch hở của acid và ester có công thức phân tử C4H6O2 (không tính đồng phân hình học) là:
Các công thức thỏa mãn là: HCOOCH2CH=CH2; HCOOCH=CH-CH3; HCOOC(CH3)=CH2; CH3CH=CH-COOH; CH2=CH-CH2COOH; CH2=C(CH3)-COOH; CH2=CH-COOCH3; CH3COOCH=CH2.
Số đồng phân cacrboxylic acid
Ứng với công thức phân tử C5H10O2 số đồng phân cacrboxylic acid là:
Số đồng phân acid ưng với công thức phân tử C5H10O2 là
CH3CH2CH2CH2COOH
CH3CH2CH(CH3)COOH
CH3CH(CH3)CH2COOH
CH3C(CH3)2COOH.
Xác định công thức của X
Hợp chất X có công thức phân tử là C3H6O tác dụng với Na, H2 và tham gia phản ứng trùng hợp. Vậy X là:
- X tác dụng với Na X có nhóm -OH.
- X tác dụng với H2, và tham gia phản ứng trùng hợp
X có không no, có liên kết đôi trong phân tử:
Xét đáp án ta thấy CH2=CH-CH2-OH thõa mãn.
Vậy X là allyl alcohol
Công thức chung
Công thức phân tử chung của aldehyde no, mạch hở, đơn chức là:
Tìm giá trị gần nhất của m
Hỗn hợp X gồm nhiều alcohol, aldehyde và acid đều mạch hở. Cho NaOH dư vào m gam X thấy có 0,2 mol NaOH phản ứng. Nếu cho Na dư vào m gam X thì thấy có 12,32 lít khí H2 (đktc) bay ra. Cho m gam X vào dung dịch AgNO3/NH3 dư thấy có 43,2 gam kết tủa xuất hiện. Mặt khác, đốt cháy hoàn toàn m gam X thu được 57,2 gam CO2. Biết các phản ứng xảy ra hoàn toàn, tổng số mol các alcohol trong X là 0,4 mol, trong X không chứa HCHO và HCOOH. Giá trị đúng của m gần nhất với:
- X phản ứng với NaOH: nCOOH = nNaOH = 0,2 mol
- X phản ứng với Na: nOH + nCOOH = 2.nH2 = 2.(12,32/22,4) = 1,1 mol
⇒ nOH = 0,9 mol
- X phản ứng với AgNO3/NH3, vì X không chứa HCHO và HCOOH nên:
nAg = 0,4 mol ⇒ nCHO = 0,2 mol
- Đem đốt cháy X:
nCO2 = 1,3 mol
Số C trong gốc R: nC = 1,3 - 0,2 – 0,2 = 0,9 mol (Bảo toàn ngyên tố C)
Nhận thấy nC trong gốc R = nCOH ⇒ Số nhóm OH bằng số nguyên tử C của alcohol no:
⇒ Số nguyên tử C trung bình của alcohol = 0.9/ 0,4 = 2,25
⇒ Alcohol có công thức trung bình là C2,25H6,5O2,25
⇒ mX = 0,2.45 + 0,2.29 + 0,4.69,5 = 42,6 gam
Tính giá trị của m
Khử hoàn toàn m gam hỗn hợp X gồm hai aldehyde no, đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng thu được (m + 1) gam hỗn hợp hai alcohol. Mặt khác, khi đốt cháy hoàn toàn cũng m gam X thì cần vừa đủ 17,92 lít khí O2 (đktc). Giá trị của m là
nO2 = 0,8 mol
Gọi công thức chung của 2 aldehyde là CnH2nO: x mol
Phản ứng hiđro hóa:
CnH2nO + H2 CnH2n+2O
mancol = mX + mH2 (Bảo toàn khối lượng)
⇒ mH2 = (m + 1) – m = 1 gam
⇒ nH2 = 0,5 mol = nX
CnH2nO + (3n-1)/2O2 nCO2 + nH2O
0,5 → 0,25(3n – 1)
⇒ 0,25(3n-1) = 0,8
⇒ n = 1,4
⇒ mX = m = (1,4.14 + 16).0,5 = 17,8 gam
Số phát biểu đúng
Cho các phát biểu sau:
(a) Phenol dễ tham gia phản ưng thế bromine và thế nitro hơn benzene do ảnh hưởng của nhóm -OH..
(b) Cho ethane-1,2-diol vào ống nghiệm có Cu(OH)2 và dung dịch NaOH, lắc nhẹ, hiện tượng quan sát được là dung dịch có màu xanh đậm.
(c) Formalin hay formon là dung dịch của methanal trong nước.
(d) Có thể điều chế aldehyde trực tiếp từ bất kì alcohol nào.
(e) Toluene (C6H5CH3) tác dụng được với nước bromine, dung dịch thuốc tím ở điều kiện thường.
Số phát biểu đúng là
(d) sai vì aldehyde không được điều chế trực tiếp từ alcohol
(e) sai vì Toluene (C6H5CH3) không tác dụng được với nước bromine, dung dịch thuốc tím ở điều kiện thường.
Phương pháp hiện đại điều chế acetic acid
Phương pháp được xem là hiện đại để điều chế acetic acid là:
Công thức cấu tạo của propionic acid
Propionic acid có công thức cấu tạo là
Propionic acid có công thức cấu tạo là CH3CH2COOH.
Sản xuất giấm ăn
Để sản xuất giấm ăn người ta dùng phương pháp nào trong các phương pháp sau?
Phương pháp lên men giấm: Sử dụng men giấm để oxi hóa ethanol bằng oxygen không khí thành acetic acid.
Tính khối lượng kết tủa thu được
Cho 20 gam dung dịch formalin 33% tác dụng với AgNO3/NH3 dư thì lượng kết tủa thu được là
Khối lượng formaldehyde trong formalin là:
mHCHO = 20.0,33 = 6,6 (g)
⇒ nHCHO = 0,22 (mol)
HCHO + 4AgNO3 + 6NH3 + 2H2O → 4Ag + 4NH4NO3 + (NH4)2CO3
mol: 0,22 → 0,88
⇒ mAg = 0,88.108 = 95,04 (g)
Xác định công thức cấu tạo của X
Cho X là hợp chất thơm; a mol X phản ứng vừa hết với a lít dung dịch NaOH 1M. Mặt khác, nếu cho a mol X phản ứng với Na (dư) thì sau phản ứng thu được 24,79a lít khí H2 (đkc). Công thức cấu tạo thu gọn của X là:
nH2 = a mol
Theo bài ra ta có:
a mol X + Na → a mol H2
X có 2 nguyên tử H linh động.
a mol X + a mol NaOH
X có 1 nguyên tử H linh động thuộc nhóm OH phenol hoặc nhóm –COOH
Nguyên tử H còn lại thuộc nhóm –OH alcohol.
Số chất tham gia phản ứng tráng bạc
Cho dãy các chất sau: HCHO, CH3COOH, CH3CHO, HCOOH, C2H5OH. Số chất trong dãy có thể tham gia phản ứng tráng bạc là
Chất có thể tham gia phản ứng tráng bạc là: HCHO, CH3CHO, HCOOH.
Tìm công thức phân tử của A
Cho 5,8 gam aldehyde A tác dụng hết với một lượng dư AgNO3/NH3 thu được 43,2 gam Ag. Tìm công thức phân tử của A
nAg = 43,2/108 = 0,4 mol
TH1: A có 1 nhóm CHO trong phân tử nA:nAg = 1:2
nA = 0,4/2 = 0,2 (mol)
Không thõa mãn.
TH2: A có 2 nhóm CHO trong phân tử nA:nAg = 1:4
nA = 0,4/4 = 0,1 (mol)
A là OHCCHO
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: