Tìm phát biểu không đúng
Phát biểu nào sau đây là không đúng?
Có chất trong phân tử có vòng benzene nhưng không là hydrocarbon thơm.
Ví dụ: potassium benzoate.
Cùng nhau thử sức với bài đánh giá năng lực cuối kì 2 Hóa học 11 nha!
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Tìm phát biểu không đúng
Phát biểu nào sau đây là không đúng?
Có chất trong phân tử có vòng benzene nhưng không là hydrocarbon thơm.
Ví dụ: potassium benzoate.
Xác định công thức cấu tạo của X
Cho phản ứng CH3CH2OH + CuO → X + Cu + H2O. Công thức cấu tạo của X là
Phương trình phản ứng:
CH3CH2OH + CuO → CH3CHO + Cu + H2O
X là CH3CHO.
Thứ tự giảm dần nhiệt độ sôi
Thứ tự giảm dần nhiệt độ sôi của ba hợp chất hữu cơ sau: C3H8; C2H5OH, CH3CHO.
Thứ tự nhiệt độ sôi:
C2H5OH > CH3CHO > C3H8.
Công thức tổng quát của dichloro mạch hở
Công thức tổng quát của dẫn xuất dichloro mạch hở có chứa một liên kết ba trong phân tử là
CnH2n+2 CnH2nCl2
CnH2n-4Cl2
Hợp chất chứa nhóm C=O
Hợp chất chứa nhóm C=O liên kết với nguyên tử carbon hoặc nguyên tử hydrogen được gọi là
Hợp chất chứa nhóm C=O liên kết với nguyên tử carbon hoặc nguyên tử hydrogen được gọi là hợp chất carbonyl.
Chất phản ứng với phenol và alcohol
Cả phenol và ethyl alcohol đều phản ứng được với:
Nhận biết các chất
Nhận biết các chất sau: aldehyde acetic, acetone và acetylene đựng trong 3 lọ mất nhãn chỉ dùng một hóa chất.
Dùng AgNO3/NH3 để nhận biết 3 chất:
- Acetylene tạo kết tủa màu vàng.
- Aldehyde acetic tham gia phản ứng tráng gương tạo lớp kết tủa sáng.
- Acetone không có hiện tượng.
Sản xuất giấm ăn
Để sản xuất giấm ăn người ta dùng phương pháp nào trong các phương pháp sau?
Phương pháp lên men giấm: Sử dụng men giấm để oxi hóa ethanol bằng oxygen không khí thành acetic acid.
Xác định các chất là đồng đẳng
Cho các chất: C6H5OH (X); C6H5CH2OH (Y); HOC6H4OH (Z); C6H5CH2CH2OH (T). Các chất đồng đẳng của nhau là:
C6H5CH2OH (Y); C6H5CH2CH2OH (T) cùng thuộc dãy đồng đẳng của alcohol thơm.
Xác định hợp chất hữu cơ X
Cho hợp chất X no, mạch hở biết phần trăm khối lượng C và H lần lượt bằng 66,67% và 11,11 %, còn lại là O. Trên phổ MS tìm thấy tín hiệu ứng với phân tử khối của X là 72. X không tác dụng với dung dịch AgNO3 trong NH3 nhưng có phản ứng tạo iodoform. Công thức cấu tạo của hợp chất X là:
Ta có %mO = 100% - 66,67% - 11,11 % = 22,22%
Gọi công thức đơn giản nhất của X có dạng CxHyOz
Ta có
Công thức đơn giản nhất của X là C4H8O.
Gọi cống thức phân tử của X là (C4H8O)n
⇒ Mx = (4.12 + 8 + 16)n = 72n = 72 ⇒ n = 1.
Vậy công thức phân tử của X là C4H8O.
X không tác dụng được với dung dịch AgNO3 trong NH3 nên X là ketone. Do X có phản ứng tạo iodoform nên phân tử của X có chứa nhóm CH3CO−.
Vậy công thức cấu tạo của X là CH3COCH2CH3 (ethyl methyl ketone hay butanone).
Tìm sản phẩm và số mol
Cho hỗn hợp gồm 2 mol C6H6 và 3 mol Cl2, trong điều kiện có xúc tác bột Fe, to, hiệu suất 100%. Sau phản ứng sản phẩm thu được chất gì và bao nhiêu mol?
Sản phẩm thu được là C6H5Cl và C6H4Cl2.
Gọi số mol của C6H5Cl và C6H4Cl2 lần lượt là x, y:
C6H6 + Cl2 C6H5Cl + HCl
x x x x
C6H6 + 2Cl2 C6H4Cl2 + 2HCl
y 2y y 2y
Ta có hệ:
Nhận biết HCOOH, CH3COOH, C2H5OH
Có thể phân biết 3 lọ mất nhãn chứa: HCOOH, CH3COOH, C2H5OH bằng hóa chất nào dưới đây?
Phân tích các đáp án:
Nếu dùng dung dịch AgNO3/NH3 chỉ phân biệt được HCOOH.
NaOH chỉ nhận biết được C2H5OH không phản ứng
Cả 3 chất đều phản ứng với Na không thể nhận biết được
Cu(OH)2/OH-
Tác dụng với với CH3COOH như bình thường còn HCOOH tạo kết tủa đỏ gạch
Không phản ứng với C2H5OH.
Sự biến đổi nhiệt độ sôi của các chất
Sự biến đổi nhiệt độ sôi của các chất theo dãy: CH3CHO, CH3OH, C2H5OH là:
Ta có nhiệt độ sôi: alcohol > aldehyde
Dãy: CH3CHO, CH3OH, C2H5OH có nhiệt độ sôi tăng dần.
Tính thành phần phần trăm khối lượng
Hai chất hữu cơ X và Y, thành phần nguyên tố đều gồm C, H, O, có cùng số nguyên tử carbon (MX < MY). Khi đốt cháy hoàn toàn mỗi chất trong oxygen dư đều thu được số mol H2O bằng số mol CO2. Cho 0,1 mol hỗn hợp gồm X và Y phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 28,08 gam Ag. Thành phần phần trăm khối lượng của X trong hỗn hợp ban đầu là:
Ta có:
nAg:nhh = 2,6 mà hỗn hợp đều có dạng là hợp chất no, đơn chức (vì nH2O = nCO2)
1 chất tráng gương tỉ lệ 1:2 và 1 chất tráng gương tỉ lệ 1:4
Vậy hai chất là HCHO và HCOOH.
Gọi số mol của HCHO và HCOOH lần lượt là x, y:
nhh = x + y = 0,1 mol (1)
nAg = 4x + 2y = 0,26 mol (2)
Từ (1) và (2) ta được: x = 0,03 mol; y = 0,07 mol
Số đồng phân cacrboxylic acid
Ứng với công thức phân tử C5H10O2 số đồng phân cacrboxylic acid là:
Số đồng phân acid ưng với công thức phân tử C5H10O2 là
CH3CH2CH2CH2COOH
CH3CH2CH(CH3)COOH
CH3CH(CH3)CH2COOH
CH3C(CH3)2COOH.
Alcohol nào không có phản ứng tách nước tạo ra alkene
Alcohol nào sau đây không có phản ứng tách nước tạo ra alkene?
Alkene có phân tử nhỏ nhất là ethylene (C2H4), do đó CH3OH không có phản ứng tách nước tạo alkene.
Dẫn xuất không có đồng phân hình học
Dẫn xuất halogen không có đồng phân hình học là:
Điều kiện có đồng phân hình học:
+ Phân tử có liên kết đôi.
+ Mỗi nguyên tử carbon ở liên kết đôi liên kết với các nguyên tử/ nhóm nguyên tử khác nhau.
Chất không có đồng phân hình học là CH2=CH-CH2F.
Alcohol bị oxi hóa tạo thành ketone
Oxi hóa alcohol nào sau đây thu được ketone?
Tìm công thức phân tử và tính khối lượng
Thủy phân hoàn toàn m gam dẫn xuất X chứa Chlorine trong dung dịch NaOH thu được 7,4 gam alcohol Y. Đốt cháy hoàn toàn lượng Y tạo thành rồi dẫn sản phẩm qua 1 bình chứa H2SO4 đặc, bình 2 chứa dung dịch nước vôi trong dư thấy khối lượng bình 1 tăng 9,0 gam, bình 2 có 40,0 gam kết tủa. Công thức phân tử của X và giá trị của m lần lượt là:
Đốt cháy alcohol Y thu được sản phẩm cháy gồm CO2 và H2O.
Khối lượng bình 1 tăng là khối lượng của H2O:
Kết tủa ở bình 2 là CaCO3:
nC = nCO2 = nCaCO3 = 4:100 = 0,4 mol
mY = mC + mH + mO
mO = 7,4 – 1.1 – 0,4.12 = 1,6 gam
nO = 0,1 mol
nC : n H : nO = 0,4 : 1 : 0,1 = 4 : 10 : 1
Alcohol Y là C4H10O
X là C4H9Cl
nX = nC4H10O = 0,4:4 = 0,1 mol
m= 0,1.92,5 = 9,25 gam.
Xác định tên gọi của acid X
Trong phân tử carboxylic acid X có số nguyên tử carbon bằng số nhóm chức. Đốt cháy hoàn toàn một lượng X thu được số mol CO2 bằng số mol H2O. Tên gọi của X là
Vì đốt cháy X thu được nCO2 = nH2O X có dạng CnH2nOz
Số nguyên tử C = số nhóm chức số O trong X gấp đôi số C
X có dạng: CnH2nO2n
Với n = 1 X là CH2O2
X là formic acid: HCOOH
Với n = 2 X là C2H4O4 (không thỏa mãn)
Sản phẩm của phản ứng trùng ngưng
Keo dán phenol formaldehyde (PF) có độ kết dính cao, chịu nhiệt và nước, thường được dùng để ép gỗ, dán gỗ trong xây dựng (gỗ coppha). PF là sản phẩm của phản ứng trùng ngưng giữa formaldehyde (H-CHO) với
PF là sản phẩm của phản ứng trùng ngưng giữa formaldehyde (H-CHO) với phenol (C6H5OH).
Sắp xếp acid
Cho các acid sau: (CH3)2CHCOOH (1), CH3COOH (2), HCOOH (3), (CH3)3CCOOH (4). Dãy được sắp xếp theo chiều tăng dần tính acid là:
Tìm tên gọi của A
A là hợp chất hữu cơ CxHyOz được 0,1 mol A cho toàn bộ sản phẩm vào nước vôi thu được 30 gam kết tủa. Đun nóng dụng dịch thu được tiếp 20 gam kết tủa. A vừa tác dụng với Na và NaOH. Biết 1 mol A tác dụng hết với Na thu được 0,5 mol khí H2 và A tác dụng với dung dịch bromine theo tỉ lệ 1:3 .Tên gọi cả A là
n↓ = 0,3 mol
Gọi công thức của A là CxHyOz
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,3 ← 0,3
2CO2 + Ca(OH)2 → Ca(HCO3)2
a → a/2
Ca(HCO3)2 CaCO3 + CO2 + H2O
0,2 ← 0,2
Theo bài ra ta có: a/2 = 0,2 ⇒ a = 0,4 (mol)
⇒ nCO2 = 0,3 + 0,4 = 0,7 (mol)
⇒ 0,1x = 0,7 mol
⇒ x = 7
Theo giả thiết:
Vậy công thức phân tử của A là C7H8O
Mặt khác: A phản ứng với Br2 theo tỉ lệ mol 1:3 nên A có công thức cấu tạo:
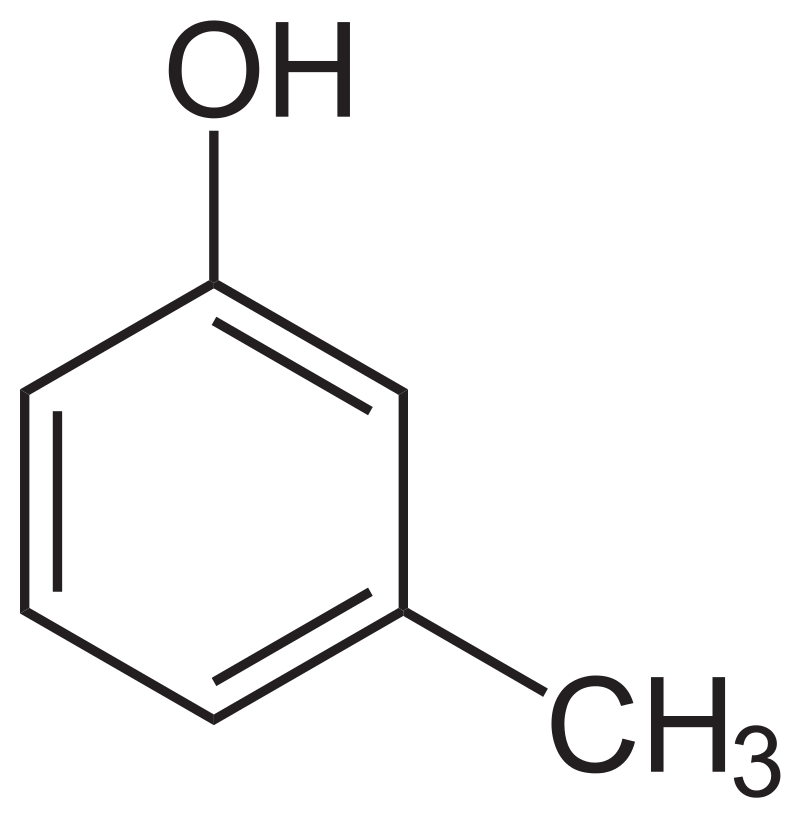
(m-cresol)
Công thức của hai hydrocarbon
Hỗn hợp X gồm một ankan và một alkene. Cho X tác dụng với 3,4706 lít hydrogen tới phản ứng hoàn toàn thu được hỗn hợp Y gồm 2 khí trong đó có hydrogen dư và một hydrocarbon. Đốt cháy hoàn toàn hỗn hợp Y rồi dẫn hỗn hợp khí và hơi sinh ra vào bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 13,52 gam đồng thời có 16 gam kết tủa được tạo thành. Chất khí được đo ở điều kiện tiêu chuẩn. Công thức của hai hydrocarbon là:
nH2 = 3,4706 : 24,79 = 0,14 mol
Công thức Alkane và Alkene lần lượt CnH2n+2 và CnH2n ( n > 2)
Hydrocarbon trong Y là CnH2n+2 x mol và y mol H2. Ta có:
Khi đốt cháy hỗn hợp Y ta thu được: nx mol CO2 và (nx + x + y) mol H2O.
Từ đây ta có:
nx = 16 : 100 = 0,16 mol
Khối lượng bình tăng là tổng khối lượng của CO2 và H2O.
44nx + 18(nx + x + y) = 13,52
⇒ x + y = 0,2
⇒ Số mol alkane ban đầu là: 0,2 – 0,14 = 0,06 ⇒ 0,6 < x < 0,2.
Vậy 0,8 = 0,16 : 0,2 < n < 0,16 : 0,06 = 2,67
Vậy n = 2. Công thức hai hydrocarbon là C2H6 và C2H4.
Tìm sản phẩm chính của phản ứng
Sản phẩm chính của phản ứng sau đây là chất nào?
CH3–CH2–CHCl–CH3 ![]()
Theo quy tắc Zaitsev: Trong phản ứng tách hydrogen halide (HX) ra khỏi dẫn xuất halogen, nguyên tử halogen (X) được ưu tiên tách ra cùng với nguyên tử hydrogen (H) ở nguyên tử carbon bên cạnh có bậc cao hơn, tạo ra sản phẩm chính.
CH3–CH2–CHCl–CH3 CH3–CH=CH–CH3 + HCl
Xác định công thức cấu tạo của Y
Hợp chất Y là dẫn xuất chứa oxygen của benzene, khối lượng phân tử của Y bằng 94 đvC. Cho biết công thức cấu tạo của Y.
Khối lượng phân tử của Y bằng 94 đvC Trong Y chỉ có 1 nguyên tử O.
Gọi công thức phân tử của Y là C6H5OR
MY = 93 + R = 94 đvC
R = 1 đvC (H).
công thức phân tử của Y là C6H5OH.
Gọi tên acid theo danh pháp thay thế
Chất có công thức sau:
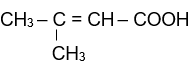
Tên thay thế là:
Chọn mạch chinh là mạch carbon dài nhất chứa nhóm -COOH và được đánh số bắt đầu từ nhóm -COOH
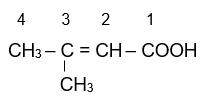
3-methylbut-2-enoic acid.
Chất tác dụng với dung dịch KMnO4 ở điều kiện thường
Chất nào sau đây tác dụng với dung dịch KMnO4 ở điều kiện thường?
Các alkene tác dụng được với dung dịch KMnO4 ở điều kiện thường:
3C2H4 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2MnO2↓ + 2KOH
Thực hiện phản ứng tách HCl với ethyl chloride
Thực hiện phản ứng tách HCl với ethyl chloride thu được
CH3CH2Cl CH2=CH2 + HCl
ethyl chloride Ethylene
Tìm phát biểu sai về phenol
Phát biểu nào sau đây về phenol là sai?
Phát biểu sai là: Phenol thuộc loại alcohol thơm, đơn chức vì phenol không phải alcohol thơm.
Màu của quỳ tím khi cho vào dung dịch acetic acid
Cho quỳ tím vào dung dịch acetic acid, quỳ tím
Acetic acid làm cho quỳ tìm chuyển sang màu đỏ.
Nhận xét nào sau đây đúng
Cho công thức cấu tạo sau: CH3CH=CHCH2OH. Nhận xét nào sau đây đúng
Bậc của alcohol là bậc của carbon liên kết với nhóm OH
CH3CH=CHCH2OH là Alcohol không no, bậc I
Công thức cấu tạo của propionic acid
Propionic acid có công thức cấu tạo là
Propionic acid có công thức cấu tạo là CH3CH2COOH.
Oxi hóa propan-2-ol bằng CuO
Oxi hóa propan-2-ol bằng CuO nung nóng, thu được sản phẩm nào sau đây?
Khi phản ứng với các chất oxi hóa CuO
Sản phẩm khác nhau tùy theo bậc của alcohol
+ Alcohol bậc I bị oxi hóa thành aldehyde
+ Alcohol bậc II bị oxi hóa thành ketone.
+ Alcohol bậc III không bị oxi hóa.
CH3-CHOH-CH3 + CuO CH3COCH3 + Cu ↓+ H2O
Alcohol bậc II ketone
Tính khối lượng muối khan thu được
Cho 9,2 gam formic acid phản ứng với dung dịch KOH (dư). Khối lượng muối khan thu được là:
nHCOOH = 0,2 (mol)
Phương trình phản ứng:
HCOOH + NaOH → HCOONa + H2O
mol: 0,2 → 0,2
⇒ mmuối = 0,2.68 = 13,6 (g)
Đốt cháy alkyne
Khi đốt cháy hoàn toàn alkyne, thu được
Gọi công thức chung của alkyne là CnH2n-2 (n ≥ 2)
Khi đốt cháy hoàn toàn alkyne, ta có:
CnH2n – 2 + (3n – 1)/2 O2 nCO2 + (n – 1) H2O
mol: a → an → a(n – 1)
⇒ a(n – 1) < an
⇒ nH2O < nCO2
Tính số nhận định đúng
Cho các nhận định sau:
(a) Aldehyde là hợp chất chỉ có tính khử.
(b) Aldehyde bị khử bởi NaBH4 tạo thành alcohol bậc một.
(c) Aldehyde tác dụng với AgNO3/NH3 tạo thành Ag.
(d) Aldehyde no, đơn chức, mạch hở có công thức tổng quát CnH2nO (n ≥ 1).
Số nhận định đúng là
(a) sai vì aldehyde là hợp chất vừa có tính khử vừa có tính oxi hóa.
(b), (c) (d) đúng.
Số đồng phân alkyne tác dụng với dung dịch AgNO3/NH3 tạo kết tủa
Có bao nhiêu đồng phân alkyne C5H8 tác dụng được với dung dịch AgNO3/NH3 tạo kết tủa?
Đồng phân alkyne tác dụng được với dung dịch AgNO3/NH3 tạo kết tủa khi có liên kết ba đầu mạch (alk - 1- yne).
⇒ Các alkyne thỏa mãn là:
CH≡C–CH2–CH2–CH3
CH≡C–CH(CH3)–CH3
Chất được sử dụng để tẩy rửa sơn mỏng tay, tẩy keo siêu dính,...
Chất nào dưới đây được sử dụng để tẩy rửa sơn mỏng tay, tẩy keo siêu dính, tẩy trên các đồ gốm sứ, thuỷ tinh; ngoài ra, còn được sử dụng làm phụ gia bảo quản thực phẩm.
Acetone (CH3COCH3) được sử dụng để tẩy rửa sơn mỏng tay, tẩy keo siêu dính, tẩy trên các đồ gốm sứ, thuỷ tinh; ngoài ra, còn được sử dụng làm phụ gia bảo quản thực phẩm.
Xác định tên của alcohol A
Dẫn m gam hơi alcohol đơn chức A qua ống đựng CuO (dư, to). Phản ứng hoàn toàn thấy khối lượng chất rắn trong ống giảm đi 0,5m gam. Alcohol A có tên là
Khối lượng chất rắn giảm = mO = 0,5m
Vì alcohol đơn chức nên
M = 32
A là CH3OH (methanol).
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: