2-methylpent-2-en tác dụng với Br2
Sản phẩm tạo thành khi 2-methylpent-2-en tác dụng với Br2 có tên gọi là
Phương trình phản ứng:
(CH3)2C=CH−CH3 + Br2 → (CH3)2CBr−CHBr−CH3
Sản phẩm có tên là 2,3-dibromo-2-methylpentane.
Cùng nhau ôn tập, thử sức với đề kiểm tra giữa học kì 2 Hóa 11 nha!
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
2-methylpent-2-en tác dụng với Br2
Sản phẩm tạo thành khi 2-methylpent-2-en tác dụng với Br2 có tên gọi là
Phương trình phản ứng:
(CH3)2C=CH−CH3 + Br2 → (CH3)2CBr−CHBr−CH3
Sản phẩm có tên là 2,3-dibromo-2-methylpentane.
Tên gọi alkane đúng
Tên gọi của alkane nào sau đây đúng?
Công thức cấu tạo của 2,2-dimethylbutane là

Chất không có đồng phân hình học
Chất nào sau đây không có đồng phân hình học?
Hợp chất (CH3)2C=CH-CH 3 không có đồng phân hình học
Xác định công thức phân tử của 2 hydrocarbon
Cho 4,958 lít hỗn hợp X (ở đkc) gồm 2 hydrocarbon mạch hở lội từ từ qua bình chứa 1,4 lít dung dịch Br2 0,5M. Sau khi phản ứng hoàn toàn, số mol Br2 giảm đi một nửa và khối lượng bình tăng thêm 6,7 gam. Xác định công thức phân tử của 2 hydrocarbon.
Trường hợp 1: Nếu chỉ có 1 hydrocarbon phản ứng với dung dịch Bromine thì ta có:
nC2H2 = 1/2.nBr2 = 0,175 mol
⇒ nC3H8 = 0,2 - 0,175 = 0,025 mol
⇒ mhỗn hợp = 0,175.26 + 0,025.44 = 5,65 ≠ 6,7 (Loại)
Trường hợp 2: Cả hai hydrocarbon cùng phản ứng với dung dịch nước bromine
nX = 4,958 : 24,79 = 0,2 mol;
nBr2 ban đầu = 1,4.0,5 = 0,7 mol;
nBr2 pư = 0,7 : 2 = 0,35 mol
Khối lượng bình Br2 tăng 6,7 gam là số gam của hỗn hợp X. Đặt công thức trung bình của hai hydrocarbon mạch hở là (
là số liên kết
trung bình)
Phương trình phản ứng:
0,2 → 0,2 = 0,35 (mol)
⇒ = 0,35 : 0,2 = 1,75
⇒ Trong hỗn hợp có một chất chứa 2 liên kết chất còn lại chứa 1 liên kết
.
⇒ 14 + 2 - 2
= 6,7:0,2 ⇒
= 2,5
⇒ Trong hỗn hợp phải có một chất là C2H2 (có hai liên kết ) chất còn lại phải có một liên kết
và có số C từ 3 trở lên đó là C4H8.
Xác định tên gọi X, Y
Cho các alkene X và Y có công thức như sau:
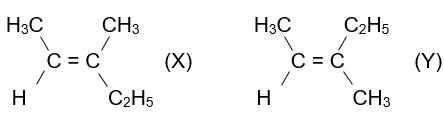
Tên gọi của X và Y tương ứng là
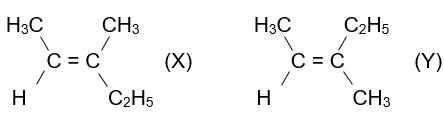
Tên gọi của X và Y tương ứng là: trans-3-methylpent-2-ene và cis-3-methylpent-2-ene.
Nitro hoá benzene
Nitro hoá benzene bằng hỗn hợp HNO3 đặc và H2SO4 đặc ở nhiệt độ ≤50oC, tạo thành chất hữu cơ A. Phát biểu nào sau đây về A không đúng?
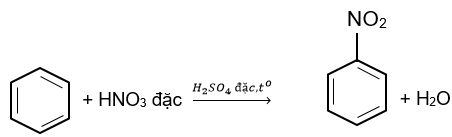
C6H5NO2 có tên là nitrobenzene; là chất lỏng màu vàng, sánh như dầu; không tan trong nước.
Xác định số đồng phân
Số alkene có cùng công thức C4H8 và số alkyne có cùng công thức C4H6 lần lượt là
Các đồng phân alkene có cùng công thức C4H8:
CH2=CH-CH2-CH3
CH3-CH=CH-CH3 (có đồng phân hình học cis, trans)
CH2=C(CH3)-CH3
Có tất cả 4 đồng phân alkene có công thức phân tử C4H8.
Các đồng phân alkyne có cùng công thức C4H6:
HC≡C-CH2-CH3
H3C-C≡C-CH3
Có tất cả 2 đồng phân alkyne có công thức phân tử C4H6.
Tên gọi của X
Alkane X có công thức phân tử C5H12. Cho X tác dụng với chlorine khi đun nóng chỉ tạo một dẫn xuất monochloro duy nhất. Tên gọi của X là
Alkane có công thức phân tử C5H12, tạo ra một dẫn xuất monochloro duy nhất là 2,2 – dimethylpropane
. 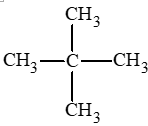
2,2 – dimethylpropane
Đun nóng toluene với dung dịch KMnO4
Đun nóng toluene với dung dịch KMnO4 nóng, thì tỉ lệ mol C6H5COOK sinh ra so với KMnO4 phản ứng bằng
Phương trình phản ứng đun nóng toluene với dung dịch KMnO4 nóng
C6H5CH3 + 2KMnO4 → C6H5COOK + KOH + 2MnO2+ H2O
Vậy tỉ lệ mol C6H5COOK sinh ra so với KMnO4 phản ứng bằng 1:2
Sản phẩm của phản ứng monochlorine hoá propane
Cho các chất sau: (X) 1-chloropropane và (Y) 2-chloropropane. Sản phẩm của phản ứng monochlorine hoá propane là
Phương trình phản ứng xảy ra như sau:
CH3- CH2 - CH3 CH3 - CH2- CH2- Cl + CH3 - CH(Cl) - CH3
(X) 1-chloropropane (Y) 2-chloropropane
2-methylpropane tác dụng với chlorine
Cho 2-methylpropane tác dụng với chlorine (tỉ lệ mol 1 : 1, có ánh sáng) thu được tối đa bao nhiêu sản phẩm thế monochloro?
Cho 2-methylpropane tác dụng với chlorine (tỉ lệ mol 1 : 1, có ánh sáng) thu được 2 sản phẩm thế monochloro
.
Neopentane tác dụng với chlorine
Trộn neopentane với chlorine và chiếu ánh sáng tử ngoại thì thu được tối đa bao nhiêu sản phẩm monochlorine?
Sản phẩn duy nhất thu được là 1-chloro-2,2-dimethylpropane.

Đun nóng hydrocarbon thơm X có công thức phân tử C8H10
Đun nóng hydrocarbon thơm X có công thức phân tử C8H10 với dung dịch KMnO4 nóng thu được dung dịch có chứa C6H5COOK và K2CO3. Chất X là
Đồng phân của C8H10

C6H5CH2CH3 + 4KMnO4 C6H5COOK + K2CO3 + 4MnO2 + KOH + 2H2O
Chất X là ethylbenzene.
Tên thay thế (CH3)2CH-CH3
(CH3)2CH-CH3 có tên theo danh pháp thay thế là

(CH3)2CH-CH3 có tên theo danh pháp thay thế là 2-methylpropane.
Công thức phân tử của X
Trong phân tử hydrocarbon X, hydrogen chiếm 25% về khối lượng. Công thức phân tử của X là
Gọi công thức của hydrocarbon X là CxHy.
Ta có:
Công thức phân tử của X là CH 4 .
Gọi tên alkane
Cho alkane sau:
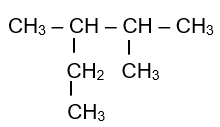
Danh pháp thay thế của alkane trên là
Cần chọn mạch chính dài nhất (5 nguyên tử C), nhiều nhánh nhất (hai nhánh). Đánh số thứ tự theo chiều sao cho tổng chỉ số của các nhánh là nhỏ nhất (vị trí số 1 ở đầu mạch carbon và gần nhánh nhất).

2,3-dimethylpentane
Xác định công thức phân tử
Cho công thức cấu tạo sau:
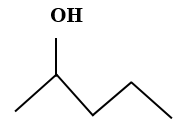
Công thức phân tử tương ứng là:
 có công thức phân tử là C5H12O
có công thức phân tử là C5H12O
Phân tử chất có thể cộng thêm 5 phân tử H2
Phân tử chất nào sau đây có thể cộng thêm 5 phân tử H2 (xúc tác Ni, đun nóng)?
Naphthalen có công thức
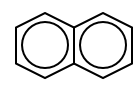
gồm có 5 liên kết đôi trong phân tử, nên khi gặp xúc tác Ni ở nhiệt độ thích hợp có thể cộng thêm 5 phân tử H2.
Khái niệm arene
Arene hay còn gọi là hydrocarbon thơm là những hydrocarbon trong phân tử có chứa một hay nhiều
Arene hay còn gọi là hydrocarbon thơm là những hydrocarbon trong phân tử có chứa một hay nhiều vòng bezene.
Xác định công thức cấu tạo của X
Một hydrocarbon X trong phân tử có phần trăm khối lượng carbon bằng 94,117%. Trên phổ khối lượng của X có peak ion phân tử ứng với giá trị m/z = 102. X có khả năng tác dụng được với bromine khi có xúc tác FeBr3. Xác định công thức cấu tạo của X.
X là hydrocarbon nên hợp chất gồm các nguyên tố C, H.
Gọi công thức tổng quát của hydrocarbon X là CxHy
Theo đề bài ta tìm được % khối lượng của H trong X: 100% - 94,117% = 5,883 %.
⇒ Công thức thực nghiệm của X là: (C8H6)n
Ta có:
MX = 102 ⇒ 102n = 102 ⇒ n = 1
Công thức phân tử của chất X là C8H6
Vì X có khả năng phản ứng với bromine khi có xúc tác FeBr3, chứng tỏ phân tử X có vòng benzene. Vậy công thức cấu tạo phù hợp với X là
C6H5C≡CH
Tạo duy nhất một sản phẩm thế monochloro
Có bao nhiêu alkane (có số nguyên tử C ≤ 5) khi tác dụng với chlorine (có ánh sáng hoặc đun nóng) tạo duy nhất một sản phẩm thế monochloro?
Các alkane (có số nguyên tử C ≤ 5) khi tác dụng với chlorine (có ánh sáng hoặc đun nóng) tạo duy nhất một sản phẩm thế monochloro:
CH4: Methane
H3C-CH3: ethane
 : 2,2 – dimethylpropane
: 2,2 – dimethylpropane
Công thức phân tử của X
Phân tích thành phần nguyên tố của hợp chất hữu cơ (X) thu được kết quả %C và %H (theo khối lượng) lần lượt là 84,21% và 15,79%. Phân tử khối của hợp chất (X) này được xác định thông qua kết quả phổ khối lượng) với peak ion phân tử có giá trị m/z lớn nhất là 114. Công thức phân tử của (X).
Ta có vì
%mH + %mC = 15,79% + 84,21% = 100%
nên phân tử (X) chỉ chứa nguyên tố hydrogen và carbon.
Gọi công thức phân tử của (X) là CxHy.
Công thức đơn giản nhất của (X) là (C4H9)n
Khối lượng mol phân tử của (X) được xác định trên phổ khối lượng tương ứng với peak có giá trị m/z lớn nhất. Do đó, từ phổ khối lượng của (X), ta có: MX = 114
⇒ (C4H9)n = 114 ⇒ n = 2
Vậy công thức phân tử của (X) là C8H18.
Số chất tạo kết tủa với dung dịch AgNO3 trong NH3
Cho các chất sau: acetylene; methyl acetylene; propene và dimethyl acetylene. Số chất tạo được kết tủa khi tác dụng với dung dịch AgNO3 trong NH3 là
Các alkyne có liên kết ba ở đầu mạch (alk-1-yne) có khả năng tham gia phản ứng với dung dịch AgNO3 trong NH3 tạo thành kết tủa.
acetylene: CH≡CH
methyl acetylene: CH3C≡CH
propene: CH3CH=CH2
dimethyl acetylene: CH3C≡CCH3
Phát biểu đúng về đồng đẳng
Phát biểu nào sau đây là đúng?
Đồng đẳng là những chất có cấu tạo hoá học tương tự nhau nên có tính chất hoá học cơ bản giống nhau, nhưng phân tử khác nhau một hay nhiều nhóm CH2.
Hiện tượng quan sát được
Nhỏ 1 mL nước bromine vào ống nghiệm đựng 1 mL hexane, chiếu sáng và lắc đều. Hiện tượng quan sát được là
Do xảy ra phản ứng thế của hexane với bromine nên màu của nước bromine bị mất.
Tên gọi alkane
Alkane (CH3)3C-CH2-CH(CH3)2 có tên gọi là
Alkane (CH3)3C-CH2 -CH(CH3)2 có tên gọi là 2,2,4-trimethylpentane.

2,2,4-trimethylpentane
Phát biểu không đúng
Phát biểu nào sau đây là không đúng?
Trong công nghiệp, acetylene được sản xuất chủ yếu từ methane.
Phương pháp chủ yếu nhất để điều chế acetylene hiện nay là nhiệt phân methane ở nhiệt độ 1500oC (phản ứng thu nhiệt mạnh)
2CH4 C2H2 + 3H2
Methane tác dụng với chlorine
Cho các chất sau: chloromethane, dichloromethane, trichloromethane và tetrachloromethane. Số chất là sản phẩm của phản ứng xảy ra khi trộn methane với chlorine và chiếu ánh sáng tử ngoại là
Các chất là sản phẩm của phản ứng xảy ra khi trộn methane với chlorine và chiếu ánh sáng tử ngoại là chloromethane, dichloromethane, trichloromethane và tetrachloromethane.
CH4 + Cl2 CH3Cl + HCl
chloromethane
CH3Cl + Cl2 CH2Cl2 + HCl
dichloromethane
CH2Cl2 + Cl2 CHCl3 + HCl
trichloromethane
CHCl3 + Cl2 CCl4 + HCl.
tetrachloromethane
Nhận xét không đúng
Nhận xét nào sau đây không đúng đối với phản ứng cộng chlorine vào benzene?
Phương trình phản ứng:
C6H6 + 3Cl2 → C6H6Cl6
(1,2,3,4,5,6 - hexachlorocyclohexane)
Tỉ lệ mol các chất phản ứng là 1:3.
Phân biệt but-2-yne với but-1-yne
Để phân biệt but-2-yne (CH3C≡CCH3) với but-1-yne (CH≡CCH2CH3) có thể dùng thuốc thử nào sau đây?
Chỉ có alk-1-yne mới có phản ứng với dung dịch AgNO3/NH3 để tạo kết tủa.
CH≡C-CH2-CH3 + AgNO3 + NH3 → AgC≡C–CH2-CH3 + NH4NO3
2,2-dimethylbutane tác dụng với chlorine
Khi cho 2,2-dimethylbutane tác dụng với chlorine thu được tối đa bao nhiêu dẫn xuất monochloro?
Khi cho 2,2-dimethylbutane tác dụng với chlorine thu được 3 dẫn xuất monochloro.

Phát biểu không đúng alkane
Phát biểu nào sau đây về alkane là không đúng?
(1) Trong phân tử alkane chỉ có liên kết đơn.
(2) Chỉ các alkane là chất khí ở điều kiện thường được dùng làm nhiên liệu.
(3) Các alkane lỏng được dùng sản xuất xăng, dầu và làm dung môi.
(4) Các alkane rắn được dùng làm nhựa đường, nguyên liệu cho quá trình cracking.
(5) Công thức chung của alkane là CxH2x+2, với x ≥ 1.
Số phát biểu không đúng là:
Phát biểu (2) chưa chính xác vì Một số alkane lỏng, rắn cũng có thể được sử dụng làm nhiên liệu
Công thức phân tử không phải alkane
Công thức phân tử nào sau đây không phải là công thức của một alkane?
Alkane là những hydrocarbon no mạch hở, có công thức chung CnH2n+2 (n ≥ 1).
⇒ C2H4 không phải là alkane.
Phản ứng không phải phản ứng đặc trưng của hydrocarbon không no
Phản ứng nào sau đây không phải là phản ứng đặc trưng của hydrocarbon không no?
Phản ứng thế không phải là phản ứng đặc trưng của hydrocarbon không no.
Phát biểu đúng
Phát biểu nào sau đây là đúng?
Hydrocarbon chỉ có liên kết đơn trong phân tử là hydrocarbon no.
Alkane tồn tại ở thể khí ở điều kiện thường
Cho các alkane kèm theo nhiệt độ nóng chảy và nhiệt độ sôi oC sau: propane (-187,7 và - 42,1), butane (-183,3 và -0,5), pentane (-129,7 và 36,1), hexane (- 95,3 và 68,7). Số alkane tồn tại ở thể khí ở điều kiện thường là
Các alkane tồn tại ở thể khí ở điều kiện thường là propane (-187,7 và - 42,1), butane (– 183,3 và – 0,5).
Chọn phát biểu không đúng
Phát biểu nào sau đây không đúng?
Trong phân tử methane, bốn liên kết C-H giống nhau tạo với nhau một góc 109,5o và hướng về bốn đỉnh của một tứ diện đều.

Hợp chất thuộc alkene
Hợp chất nào sau đây là một alkene?
Hợp chất CH3-CH=CH2 có mạch hở, một liên kết đôi và thuộc hợp chất alkene.
Oxi hoá butane
Oxi hoá butane bằng oxygen ở 180oC và 70 bar tạo thành sản phẩm hữu cơ X duy nhất. X là:
Phương trình phản ứng:
2CH3CH2CH2CH3 + 5O2 4CH3COOH + 2H2O
Chỉ số octane của xăng E5
Chỉ số octane (octane number) là đại lượng đặc trưng cho yếu tố đo lường khả năng chống kích nổ của một nhiên liệu khi nhiên liệu này bốc cháy với không khí bên trong xi lanh của động cơ đốt trong. Chỉ số octane của xăng E5 là:
Xăng E5 chứa 5% ethanol và 95% xăng RON 92 (theo thể tích).
⇒ Chỉ số octane của xăng E5 là:
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: