Hợp chất carbonyl
1. Khái niệm
Hợp chất carbonyl là các hợp chất hữu cơ trong phân tử có chứa nhóm chức carbonyl (![]() ). Nhóm chức carbonyl có trong aldehyde, ketone ...
). Nhóm chức carbonyl có trong aldehyde, ketone ...
Aldehyde là hợp chất hữu cơ có nhóm –CHO liên kết với nguyên tử carbon (trong gốc hydrocarbon hoặc –CHO) hoặc nguyên tử hydrogen.
Ketone là hợp chất hữu cơ có nhóm ![]() liên kết với hai gốc hydrocarbon.
liên kết với hai gốc hydrocarbon.
2. Danh pháp
2.1. Danh pháp thay thế
- Tên aldehyde
 Ví dụ:
Ví dụ:
| CH3-CH2-CH=O | 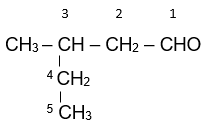 |
| propanal | 3-methylpentanal |
- Tên ketone
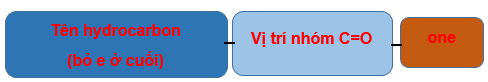
Ví dụ:
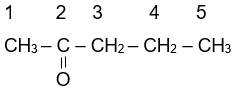
pentan-2-one
Chú ý
- Mạch carbon là mạch dài nhất chứa nhóm
 .
. - Mạch carbon được đánh số từ nhóm –CHO (đối với aldehyde) hoặc từ phía gần nhóm
 hơn (đối với ketone).
hơn (đối với ketone). - Đối với ketone, nếu nhóm
 chỉ có một vị trí duy nhất thì không cần số chỉ vị trí nhóm
chỉ có một vị trí duy nhất thì không cần số chỉ vị trí nhóm  .
. - Nếu mạch carbon có nhánh thì cần thêm vị trí và tên nhánh ở phía trước.
Ví dụ:
| HCHO | CH3CHO | 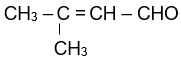 |
| methanal | Ethanal | 3-methylbut-2-enal |
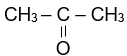 |
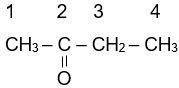 |
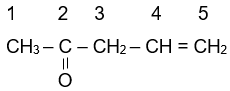 |
| propanone | butanone | pent-4-en-2-one |
2.2. Tên gọi thông thường
Một số aldehyde, ketone đơn giản được gọi theo tên thông thường có nguồn gốc lịch sử. Tên thông thường của các aldehyde có nguồn gốc từ tên của acid tương ứng.
| HCHO | aldehyde formic | formaldehyde |
| CH3CHO | aldehyde acetic | acetaldehyde |
| C6H5CHO | aldehyde benzoic | bezaldehyde |
II. Đặc điểm cấu tạo
Liên kết đôi C=O phân cực về phía nguyên tử oxygen:
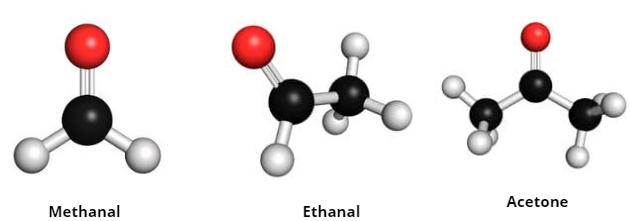
Mô hình phân tử của một số hợp chất carbonyl
III. Tính chất vật lí
Các aldehyde, ketone có nhiệt độ sôi cao hơn các hydrocarbon có khối lượng phân tử tương đương.
Ở nhiệt độ thường, các aldehyde ở thể khí và có phân tử khối nhỏ, tan tốt trong nước. Khi số nguyên tử carbon tăng thì độ tan của hợp chất carbonyl giảm dần.
IV. Tính chất hoá học
1. Phản ứng khử
Các hợp chất carbonyl bị khử bởi các tác nhân khử như NaBH4, LiAlH4,... (kí hiệu [H]) tạo thành các alcohol tương ứng, aldehyde bị khử tạo thành alcohol bậc I, ketone bị khử tạo thành alcohol bậc II.
Ví dụ:
CH3CH=O + 2[H] → CH3CH2OH;
ethanal ethanol
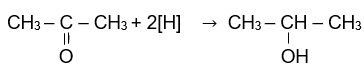
propanone propan-2-ol
2. Phản ứng oxi hóa aldehyde
Aldehyde dễ bị oxi hoá bởi các tác nhân oxi hoá thông thường như: Br2/H2O, [Ag(NH3)2]OH, Cu(OH)2/OH - ….
2.1. Oxi hóa aldehyde bởi nước bromine
Aldehyde bị oxi hoá bởi nước bromine tạo thành carboxylic acid.
Ví dụ:
CH3CHO + Br2 + H2O → CH3COOH + 2HBr
2.2. Oxi hoá aldehyde bởi thuốc thử Tollens
Thuốc thử Tollens là phức chất của ion Ag+ với ammonia, có công thức [Ag(NH3)2]OH. Ion Ag+ trong thuốc thử Tollens đóng vai trò là chất oxi hoá.
RCHO + 2[Ag(NH3)2 ]OH ![]() \(\overset{t^{o} }{\rightarrow}\) RCOONH4 + 2Ag + 3NH3 + H2O
\(\overset{t^{o} }{\rightarrow}\) RCOONH4 + 2Ag + 3NH3 + H2O
Ví dụ:
CH3CHO + 2[Ag(NH3)2]OH ![]() \(\overset{t^{o} }{\rightarrow}\) CH3COONH4 + 2Ag + 3NH3 + H2O
\(\overset{t^{o} }{\rightarrow}\) CH3COONH4 + 2Ag + 3NH3 + H2O
2.3. Oxi hoá aldehyde bång copper(II) hydroxide
Aldehyde có thể bị oxi hoá bởi copper(II) hydroxide Cu(OH)2 trong môi trường kiềm khi đun nóng tạo thành kết tủa copper(I) oxide (Cu2O) màu đỏ gạch:
RCHO + 2Cu(OH)2 + NaOH → RCOONa + Cu2O + 3H2O
Ví dụ:
CH3CHO + 2Cu(OH)2 + NaOH → CH3COONa + Cu2O + 3H2O
3. Phản ứng cộng
Hợp chất carbonyl có thể tham gia phản ứng cộng với HCN vào liên kết đối C=O.
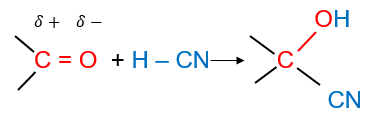
Ví dụ
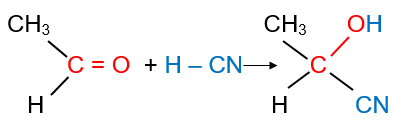
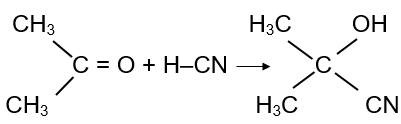
4. Phản ứng tạo iodoform
Các hợp chất aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl có thể phản ứng với I2, trong môi trường kiềm.
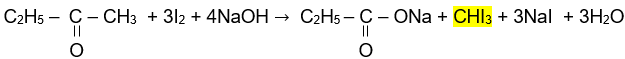
Idoform
(kết tủa màu vàng)
CH3-CHO + 3I2 + 4NaOH → H-COONa + CHI3 + 3NaI + H2O
Phản ứng tạo sản phẩm kết tủa indoform nên phản ứng này được gọi là phản ứng lodoform và được dùng để nhận biết các aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl.
V. Ứng dụng
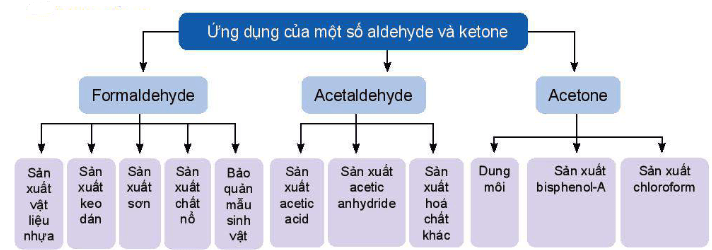
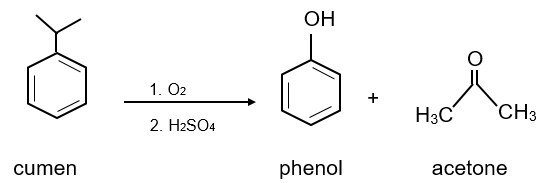
VI. Điều chế
Một số hợp chất carbonyl được tổng hợp trong công nghiệp bằng phương pháp oxi hoá các hydrocarbon, oxi hóa ethylene thành acetaldehyde, oxi hoá cumene thành acetone.
2CH2=CH2 + O2 ![]() \(\xrightarrow[]{PdCl_{2}/CuCl_{2} }\) 2CH3CHO
\(\xrightarrow[]{PdCl_{2}/CuCl_{2} }\) 2CH3CHO