Phương pháp nhận biết Methane, Ethylene, Acetylene
Phương pháp nhận biết CH4, C2H4, C2H2
Chuyên đề Hóa học lớp 9: Phương pháp nhận biết Methane, Ethylene, Acetylene được VnDoc sưu tầm và giới thiệu nhằm giúp các em học sinh nắm được các phương pháp cơ bản nhận biết Methane, Ethylene, Acetylene
>> Mời các bạn tham khảo thêm một số tài liệu liên quan
- Phân biệt Benzene Toluee Styrene
- Nhận biết CH4, C2H4, C2H2, H2
- Nhận biết hỗn hợp khí CH4, C2H4, CO2
- Hóa chất nào sau đây dùng để phân biệt hai chất CH4 và C2H4
- Để tinh chế khí methane có lẫn ethylene và acetylene ta dùng
- Nhận biết butane, but-1-yne, but-2-yne
- Trùng hợp ethylene sản phẩm thu được có cấu tạo là
A. Lý thuyết và phương pháp giải
I. Phương pháp nhận biết
Bước 1: Xác định tính chất riêng của từng chất cụ thể.
Bước 2: Lựa chọn thuốc thử.
Bước 3: Trình bày phương pháp nhận biết theo các bước sau:
Đánh số thứ tự các lọ hóa chất.
Tiến hành nhận biết.
Ghi nhận hiện tượng.
Viết phương trình hóa học.
| Chất cần nhận | Loại thuốc thử | Hiện tượng | Phương trình hóa học |
| Methane (CH4) | Khí Chlorine | Mất màu vàng lục của khí Chlorine. | CH4 + Cl2 → CH3Cl + HCl |
| Ethylene (C2H4) | Dung dịch Bromine | Mất màu vàng nâu của Dung dịch Bromine. | C2H4 + Br2 → C2H4Br2 |
| Acetylene (C2H2) |
- Dung dịch Bromine - AgNO3/NH3 |
- Mất màu vàng nâu của Dung dịch Bromine. - Có kết tủa vàng |
- C2H2 + Br2 → C2H2Br4 - C2H2 + AgNO3 + NH3 → NH4NO3 + C2Ag2 |
II. Phương pháp tách
1) Phương pháp vật lý
Phương pháp chưng cất để tách rời các chất lỏng hòa lẫn vào nhau, có thể dùng phương pháp chưng cất rồi ngưng tụ thu hồi hóa chất
Phương pháp chiết (dùng phễu chiết) để tách riêng những chất hữu cơ tan được trong nước với các chất hữu cơ không tan trong nước do chất lỏng sẽ phân thành 2 lớp.
Phương pháp lọc (dùng phễu lọc) để tách các chất không tan ra khỏi dung dịch.
2) Phương pháp hóa học
Chọn những phản ứng hóa học thích hợp cho từng chất để lần lượt tách riêng các chất ra khỏi hỗn hợp, đồng thời chỉ dùng những phản ứng hóa học mà sau phản ứng dễ dàng tái tạo lại các chất ban đầu.
III. Phương pháp tinh chế
* Nguyên tắc: Tinh chế là làm sạch hóa chất nguyên chất nào đó bằng cách loại bỏ đi tạp chất ra khỏi hỗn hợp.
* Phương pháp: Dùng hóa chất tác dụng với tạp chất mà không phản ứng với nguyên chất tạo ra chất tan hoặc tạo ra kết tủa lọc bỏ đi.
B. Bài tập vận dụng liên quan
Bài 1: Nhận biết các lọ khí mất nhãn: N2, H2, CH4, C2H2, C2H4
Hướng dẫn giải chi tiết
Nhận xét :
N2: không cho phản ứng cháy.
H2: phản ứng cháy, sản phẩm cháy không làm đục nước vôi trong.
CH4: phản ứng cháy, sản phẩm cháy làm đục nước vôi trong.
Các khí còn lại dùng các phản ứng đặc trưng để nhận biết.
Tóm tắt cách giải :
Lấy mỗi khí một ít làm mẫu thử.
Dẫn lần lượt các khí đi qua dd AgNO3/NH3. Khí nào tạo được kết tủa vàng là C2H2.
C2H2 + Ag2O → AgC≡CAg ↓ + H2O
Dẫn các khí còn lại qua dung dịch nước Bromine (màu nâu đỏ). Khí nào làm nhạt màu nước bromine là C2H4.
H2C=CH2 + Br2 → BrH2C-C2Br
Lần lượt đốt cháy 3 khí còn lại. Khí không cháy là N2. Sản phẩm cháy của hai khí kia được dẫn qua dung dịch nước vôi trong. Sản phẩm cháy nào làm đục nước vôi trong là CH4. Mẫu còn lại là H2.
CH4 + 2O2 → CO2 + 2H2O
CO2 + Ca(OH)2 → CaCO3↓ +H2O
H2 + ½ O2 → H2O
Bài 2: Tách riêng từng khí ra khỏi hỗn hợp khí gồm CH4, C2H4, C2H2 và CO2
Đáp án hướng dẫn giải
Dẫn hỗn hợp qua dd Ca(OH)2 dư thu được CaCO3
CO2 + Ca(OH)2 → CaCO3 + H2O
Thoát ra ngoài là hỗn hợp khí CH4, C2H4, C2H2
Dẫn hỗn hợp khí này qua dung dịch AgNO3/NH3 thì C2H2 bị giữ lại trong kết tủa, thoát ra ngoài là CH4 và C2H4.
C2H2 + AgNO3 + NH3 → Ag-C≡C-Ag↓+ NH4NO3
Dẫn hỗn hợp CH4 và C2H4 qua dd Brom thì C2H4 bị giữ lại, thu được CH4 tinh khiết.
C2H4 + Br2 → C2H4Br2
*Tái tạo:
Tái tạo CO2 bằng cách nhiệt phân muối CaCO3
CaCO3 → CaO + CO2
Tái tạo C2H2 bằng cách cho Ag-C≡C-Ag tác dụng với HCl
Ag-C≡C-Ag + 2HCl →C2H2 + 2AgCl
Tái tạo C2H4 bằng cách cho C2H4Br2 tác dụng với Zn/rượu
C2H4Br2 + Zn → C2H4 + ZnBr2
Bài 3: Một hỗn hợp gồm có khí ethylene, CO2 và hơi nước. Trình bày phương pháp thu được khí ethylene tinh khiết.
Đáp án hướng dẫn giải
Khí CO2 là oxide acid nên bị hấp thụ bởi dung dịch kiềm theo pt:
CO2 + Ca(OH)2 → CaCO3 + H2O
H2SO4 đậm đặc rất háo nước vì vậy để thu được ethylene tinh khiết ta dẫn hỗn hợp lần lượt qua bình 1 chứa Ca(OH)2 dư, bình 2 chứa H2SO4 đậm đặc dư
Bài 4: Nêu phương pháp hóa học để loại bỏ khí ethylene có lẫn trong khí methane để thu được methane tinh khiết
Đáp án hướng dẫn giải
Dẫn hỗn hợp qua dung dịch nước Bromine dư, khi đó etilen sẽ bị giữ lại, còn khí methane tinh khiết sẽ thoát ra:
C2H4 + Br2 → C2H4Br2
Với chuyên đề: Phương pháp nhận biết Methane, Ethylene, Acetylene trên đây chúng ta có thể hiểu rõ các bước, các chất để nhận biết được một số chất như methane, ethylene...
Bài 5. Bằng phương pháp hóa học hãy nhận biết các chất Methane, Ethylene, Acetylene
Đáp án hướng dẫn giải
Methane (CH4) có phản ứng thế vì phân tử chỉ có liên kết đơn
Ethylene (C2H4), acetylene (C2H2) có phản ứng cộng vào liên kết kém bền trong liên kết đôi và liên kết ba dùng dd AgNO3/ NH3 trước, rồi dùng dd KMnO4 (thuốc tím)
Các phản ứng tác dụng dd AgNO3/ NH3 cho màu Mầu vàng nhạt suy ra C2H2 (Alkyne)
C2H2 + AgNO3 + NH3 → C2HAg↓ + NH4NO3
làm mất màu dung dịch KMnO4 (thuốc tím) suy ra C2H4
3C2H4 + KMnO4 + 4H2O → 3C2H4(OH)2 + 2MnO2 + 2KOH
Còn lại là CH4
Câu 6. Nhận biết các lọ khí mất nhãn: SO2, CO2, C3H8, C2H2
Đáp án hướng dẫn giải
Dẫn 4 khí trên lần lượt qua dd nước vôi trong dư.
+ Có 2 khí làm đục nước vôi trong: SO2, CO2 (nhóm 1)
SO2 + Ca(OH)2 → CaSO3 + H2O
CO2 + Ca(OH)2 → CaCO3 + H2O
+ 2 khí không làm đục nước vôi trong: C3H8, C2H2 (nhóm 2).
Cho 2 khí ở mỗi nhóm lần lượt qua dd nước Bromine. Khí ở nhóm 1 làm mất màu nâu đỏ của dd Brom là SO2 và khí ở nhóm 2 cũng có hiện tượng như vậy là C2H2. Hai khí còn lại là CO2 và C3H8.
SO2 + Br2 + 2H2O → H2SO4 + 2HBr
C2H2 + Br2 → C2H2Br4
Câu 7. Phân biệt các dung dịch keo: hồ tinh bột, xà phòng, lòng trắng trứng, ta dùng
Đáp án hướng dẫn giải
Lòng trắng trứng tạo kết tủa vàng với HNO3
I2 làm dung dịch hồ tinh bột chuyển sang màu xanh
Còn lại là xà phòng
=> Dùng HNO3, I2 sẽ phân biệt được 3 chất trên
Câu 8. Để nhận biết các bình khí CH4, C2H4, CO2, và SO2 nên dùng phương pháp hóa học nào. Trình bày viết phương trình nếu có
Đáp án hướng dẫn giải
Dẫn mỗi khí một ít làm mẫu thử và đánh số thứ tự :
- Dẫn các khí qua dung dịch nước vô trong dư:
+ Các chất làm đục nước vôi trong là CO2, SO2 tạo thành nhóm ( I )
Phương trình hóa học: Ba(OH)2 + SO2 → BaSO3↓ + H2O
Ba(OH)2 + CO2 → BaCO3↓ + H2O
+ Các chất không có hiện tượng gì là CH4, C2H4 tạo thành nhóm ( II )
- Đưa các khí ở nhóm (I) và nhóm (II) qua dung dịch Bromine dư:
+ Chất ở nhóm (I) làm dung dịch nhạt màu là SO2:
Phương trình hóa học: SO2 + 2H2O + Br2 → H2SO4 + 2HBr
+ Chất còn lại ở nhóm (I) là CO2.
+ Chất ở nhóm ( II ) làm nhạt màu dung dịch Bromine là C2H4:
Phương trình hóa học: C2H4 + Br2 → C2H4Br2
+ Chất ở còn lại ở nhóm (II) là CH4.
Câu 9. Nhận biết các lọ khí mất nhãn sau: CO2, SO2, Cl2, C2H4, C2H2
Đáp án hướng dẫn giải
Đưa quỳ ẩm vào các khí.
Cl2 làm mất màu quỳ, trước đó quỳ hoá đỏ.
Cl2 + H2O ⇔ HCl + HClO
HClO ⇔ HCl + O
CO2, SO2 làm quỳ hoá đỏ nhạt
CO2 + H2O ⇔ H2CO3
SO2 + H2O ⇔ H2SO3
Hai khí này cho vào bình khí H2S. SO2 tạo kết tủa vàng, CO2 không hiện tượng
SO2 + 2H2S → 3S + 2H2O
Hai hydrocarbon ko hiện tượng
* Dẫn 2 hydrocarbon qua dung dịch AgNO3/NH3. C2H2 tạo kết tủa vàng Ag2C2, C2H4 ko hiện tượng
C2H2 + 2AgNO3 + 2NH3 → Ag2C2 + 2NH4NO3
Câu 10. Trình bày phương pháp hóa học phân biệt các chất sau: Buthane, but-1-yne và but-2-yne. Viết phương trình hóa học minh họa.
Đáp án hướng dẫn giải
Trích mẫu thử và đánh số thứ tự
Cho các mẫu thử tác dụng với dung dịch AgNO3 trong NH3
Mẫu thử nào tạo kết tủa vàng là but-1-yne
CH≡C-CH2-CH3 + AgNO3 + NH3→ CAg≡C-CH2-CH3 + NH4NO3
Cho 2 mẫu tử còn tác dụng với dd bromine
Mẫu thử nào làm mất màu dd bromine là but-2-yne
CH3-C≡C-CH3 + 2Br2 → C4H6Br4
Mẫu thử không có hiện tượng gì là Butane
C. Câu hỏi trắc nghiệm liên quan
Câu 1: Dùng một hoá chất nào sau đây để nhận biết styrene, toluene, phenol?
A. Dung dịch Br2.
B. Dung dịch HCl.
C. Dung dịch NaOH.
D. Dung dịch HNO3.
Để nhận biết 3 chất trên ta sử dụng dung dịch Br2:
Cho dung dịch Br2 vào ống nghiệm chứa mẫu thử 3 chất cần xác định
Ống nghiệm xuất hiện kết tủa trắng → phenol
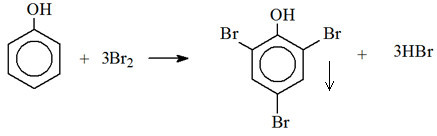
+ Ống nghiệm mất màu dung dịch bromine → styrene
C6H5CH=CH2 + Br2 → C6H5CHBr-CH2Br
+ Ống nghiệm không có hiện tượng → toluene
Đáp án A
Câu 2: Có 4 chất lỏng đựng trong 4 lọ bị mất nhãn: ethylic alcohol, toluene, phenol, formic acid. Để nhận biết 4 chất đó có thể dùng nhóm thuốc thử nào sau đây ?
A. Quỳ tím, nước Br2, dung dịch NaOH.
B. Dung dịch Na2CO3, nước Br2, Na.
C. Quỳ tím, nước Br2, dung dịch K2CO3.
D. Na, dung dịch HCl, dung dịch AgNO3 trong NH3.
Na2CO3 nhận biết được formic acid
Nước bromine nhận biết được phenol
Na nhận biết được ethylic alcohol
Còn lại là toluene
Câu 3: Chỉ dùng thêm một chất nào trong các chất dưới đây để nhận biết các chất: ethylic alcohol, acetic acid, glycerol, glucose đựng trong 4 lọ mất nhãn?
A. dung dịch AgNO3 trong NH3.
B. Quỳ tím.
C. CaCO3.
D. Cu(OH)2.
Trích mẫu thử và đánh số thứ tự
Để nhận biết các mẫu thử mất nhãn trên ta sử dung dung dịch Cu(OH)2/OH-:
Phản ứng ở nhiệt độ thường:
Mẫu thử nào xuất hiện màu xanh lam nhạt thì chất ban đầu chính là acetic acid
Cu(OH)2 + CH3COOH → (CH3COO)2Cu + H2O
Mẫu thử tạo dung dịch xanh lam đặc trưng chính là glycerol, glucose
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
2C6H12O6 + Cu(OH)2 ⟶ 2H2O+ (C6H11O6)2Cu
Mẫu thử không có hiện tượng gì là ethylic alcohol
Để nhận biết 2 mẫu thử glycerol, glucose ta tiến hành đun nóng
Mẫu thử nào xuất hiện kết tủa đỏ gạch thì dung dịch ban đầu chính là glucose
Không có kết tủa đỏ gạch là glycerol
Câu 4: Để loại bỏ SO2 có lẫn trong C2H4 người ta cho hỗn hợp khí qua dung dịch
A. KMnO4
B. Ca(OH)2
C. K2CO3
D. Br2.
Sục hỗn hợp khí qua nước vôi trong thì SO2 bị giữ lại, khí thoát ra chính là C2H4
SO2 + Ca(OH)2 → CaSO3 + H2O
Câu 5: Để làm sạch khí CH3NH2 có lẫn các khí CH4, C2H2, H2, người ta dùng
A. dung dịch HCl và dung dịch NaOH
B. dung dịch Br2 và dung dịch NaOH
C. dung dịch HNO3 và dung dịch Br2
D. dung dịch HCl và dd K2CO3
Sử dụng dung dịch HCl và NaOH:
+) Dẫn khí cần làm sạch qua dung dịch HCl à CH3NH2 bị giữ lại trong dung dịch
CH3NH2 + HCl → CH3NH3Cl
+) Cho thêm NaOH dư vào để thu hồi CH3NH2:
CH3NH3Cl + NaOH → CH3NH2 + NaCl + H2O
Khí còn lại không phản ứng chính là H2
Câu 6: Khi làm khan rượu C2H5OH có lẫn một ít nước người ta dùng cách nào sau đây?
A. Cho CaO mới nung vào rượu.
B. Cho CuSO4 khan vào rượu.
C. Chưng cất phân đoạn.
D. Cho rượu đi qua tháp chứa zeolit (một chất hút nước mạnh).
Ts của nước là 100oC
Ts của ethylic alcohol là 78,3oC
2 chất có ts chênh lệch không nhiều và khi chưng cất thì H2O bay hơi khi chưa tới 100 độ (kinh nghiệm thực tế khi đung nước) nên hh bay ra luôn chứa cả rượu và nước.
Câu 7. Để làm sạch Ethylene có lẫn Acetylene ta cho hỗn hợp đi qua dung dịch nào sau đây
A. dung dịch bromine dư.
B. dung dịch KMnO4 dư.
C. dung dịch AgNO3/NH3 dư.
D. cả A, B, C đều đúng.
Để làm sạch ethylene có lẫn acetylene, ta cho hỗn hợp đi qua dung dịch AgNO3/NH3 dư vì acetylene có phản ứng tạo kết tủa còn ethylene không phản ứng
C2H2 + 2AgNO3 + 2NH3 → C2Ag2 ↓ + 2NH4NO3
Câu 8. Phân biệt các chất methane, ethylene, acetylene bằng phương pháp hóa học, ta dùng
A. dung dịch AgNO3/NH3 và nước bromine.
B. dung dịch AgNO3/NH3
C. dung dịch NaOH.
D. dung dịch KMnO4
Phân biệt các chất methane, ethylene, acetylene bằng phương pháp hóa học, ta dùng dung dịch AgNO3/NH3 và nước bromine.
Acetylene phản ứng được với dung dịch AgNO3/NH3 tạo ra kết tủa vàng
Dùng dung dịch Bromine nhận biết nốt 2 chất còn lại
Ethylene làm mất màu dung dịch bromine, methane không phản ứng
Phương trình hóa học
CH≡CH + 2AgNO3 + 2NH3 → Ag–C≡C–Ag ↓(vàng) + 2NH4NO3
CH2=CH2 + Br2 → CH2Br–CH2Br
...............................
