Khoa học tự nhiên 7 Bài 7: Hóa trị và công thức hóa học KNTT
Giải Khoa học tự nhiên 7 Kết nối tri thức Bài 7: Hóa trị và công thức hóa học
Khoa học tự nhiên 7 Bài 7: Hóa trị và công thức hóa học KNTT được VnDoc biên soạn hướng dẫn bạn đọc trả lời chi tiết các nội dung câu hỏi, thảo luận, bài tập luyện tập SGK Khoa học tự nhiên lớp 7 Kết nối tri thức. Hy vong tài liệu sẽ cung cấp các nội dung hữu ích, cần thiết cho bạn đọc trong quá trình học tập, soạn bài và làm bài tập. Mời các bạn tham khảo chi tiết nội dung KHTN 7 Bài 7 dưới đây.
>> Bài trước đó: Khoa học tự nhiên 7 Bài 6: Giới thiệu về liên kết hóa học KNTT
I. Công thức hóa học
Câu hỏi: Trang 41 Khoa học tự nhiên 7 KNTT
Copper sulfate (CuSO4) được dùng làm chất chống xoăn lá cho cây cà chua. Em hãy cho biết số nguyên tử của từng nguyên tố có trong một phân tử copper sulfate và xác định phần trăm khối lượng của các nguyên tố trong hợp chất này.
Hướng dẫn trả lời câu hỏi
Trong một phân tử copper sulfate (CuSO4) có một nguyên tử Cu, một nguyên tử S và bốn nguyên tử O.
Khối lượng phân tử CuSO4 bằng: 64.1 + 32.1 + 16.4 = 160 (amu)
Phần trăm khối lượng các nguyên tố trong CuSO4 là:
![]() \(\%Cu\;=\frac{\;64.1}{160}\;100\%=\;40\%\)
\(\%Cu\;=\frac{\;64.1}{160}\;100\%=\;40\%\)
![]() \(\%S=\;\frac{32.1}{160\;}.100\%=\;20\%\)
\(\%S=\;\frac{32.1}{160\;}.100\%=\;20\%\)
%O = 100% - 40% - 20% = 40%
II. Hóa trị
1. Khái niệm hóa trị
Câu hỏi: Trang 42 Khoa học tự nhiên 7 KNTT
Sơ đồ sau mô tả sự hình thành liên kết cộng hóa trị trong phân tử HCl:
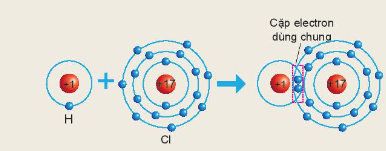
Xác định hóa trị của chlorine trong hợp chất trên.
Hướng dẫn trả lời câu hỏi
Trong phân tử HCl, nguyên tử H và nguyên tử Cl liên kết với nhau bằng 1 cặp electron chung nên cả H và Cl đều có hóa trị I.
2. Quy tắc hóa trị
Hoạt động thảo luận: Trang 42 Khoa học tự nhiên 7 KNTT
Quan sát bảng 7.1 và thực hiện các yêu cầu sau:
| Hóa trị của lưu huỳnh/carbon | Tích của chỉ số và hóa trị của lưu huỳnh/carbon | Tích của chỉ số và hóa trị của hydrogen | |
| H2S | II | 1.II | 2.I |
| CH4 | IV | 1.IV | 4.I |
1. Xét phân tử H2S, hãy so sánh tích của chỉ số và hóa trị của nguyên tố lưu huỳnh với tích của chỉ số và hóa trị của nguyên tố hydrogen.
2. Đối với phân tử CH4, thực hiện tương tự như phân tử H2S. Em hãy so sánh về tích của chỉ số và hóa trị của các nguyên tố thành phần.
Hướng dẫn trả lời câu hỏi
1. Ta thấy: 1 × II = 2 × I
⇒ Tích của chỉ số và hóa trị của nguyên tố lưu huỳnh bằng tích của chỉ số và hóa trị của nguyên tố hydrogen.
2. Xét phân tử CH4.
Ta thấy: 1× IV = 4 × I
⇒ Tích của chỉ số và hóa trị của nguyên tố carbon bằng tích của chỉ số và hóa trị của nguyên tố hydrogen.
Câu hỏi: Trang 43 Khoa học tự nhiên 7 KNTT
Câu 1. Xác định hóa trị của lưu huỳnh trong hợp chất sulfur dioxide (một nguyên tử S liên kết với hai nguyên tử O)
Hướng dẫn trả lời câu hỏi
Trong phân tử sulfur dioxide, một nguyên tử S liên kết với hai nguyên tử O nên S có hóa trị IV.
Câu 2. Hãy xác định hóa trị của carbon trong hợp chất methane có trong hình 5.3b
Hướng dẫn trả lời câu hỏi
Trong hợp chất methane, C liên kết với 4 nguyên tử H nên C có hóa trị IV
Câu 3. Dựa vào quy tắc hóa trị và Bảng 7.2, cho biết công thức hóa học của potassium oxide là KO hay K2O
Hướng dẫn trả lời câu hỏi
Từ bảng 7.2 cho biết K có hóa trị I, O có hóa trị II
Giả sử, công thức hóa học của potassium oxide là KO.
Nhận thấy: I × 1 ≠ II × 1
⇒ Giả sử sai.
⇒ Công thức hóa học của potassium oxide là K2O (vì I × 2 = II × 1)
III. Lập công thức hóa học của hợp chất
Câu hỏi. Trang 44 Khoa học tự nhiên 7 KNTT
Câu 1. Khí carbon dioxide luôn có thành phần như sau: cứ 1 phần khối lượng carbon có tương ứng 2,667 phần khối lượng oxygen. Hãy lập công thức hóa học của khí carbon dioxide, biết khối lượng phân tử của nó là 44 amu.
Hướng dẫn trả lời câu hỏi
Bước 1: Gọi công thức của khí carbon dioxide là CxOy.
Bước 2: Khối lượng phân tử của khí carbon dioxide là: 12x + 16y = 44. (1)
Bước 3: Lập biểu thức tỉ lệ khối lượng C và O tính để tìm x, y
Ta có:
![]() \(\frac{12x}{16y} =\frac{1}{2,667} ⇒ \frac{x}{y} =\frac{1}{2} ⇒ y = 2x\) (2)
\(\frac{12x}{16y} =\frac{1}{2,667} ⇒ \frac{x}{y} =\frac{1}{2} ⇒ y = 2x\) (2)
Thế y = 2x vào (1) ta được: 12x + 16.2x = 44
Giải ra được: x = 1 ⇒ y = 2
Vậy công thức của khí carbon dioxide là CO2.
Câu 2. Hãy mô tả sự hình thành liên kết cộng hoá trị trong phân tử carbon dioxide, ammonia (gồm một nguyên tử N liên kết với ba nguyên tử H)
Hướng dẫn trả lời câu hỏi
Gọi công thức hóa học khí hydeogen sulfide là ![]() \(H_x^IS_y^{II}\)
\(H_x^IS_y^{II}\)
Theo quy tắc hóa trị ta có: x . I = y . II
Chuyển biểu thức này thành tỉ lệ: ![]() \(\frac{x}{y} =\frac{II}{I} =\frac{2}{1}\)
\(\frac{x}{y} =\frac{II}{I} =\frac{2}{1}\)
Thường tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất:
Vì vậy chọn x = 2, y = 1
Công thức khí hydrogen sulfide là H2S
Khối lượng phân tử H2S là: 2.1 + 32 = 34
![]() \(\%H\;=\;\frac{2.1\;}{34}.100=\;5,9\%\)
\(\%H\;=\;\frac{2.1\;}{34}.100=\;5,9\%\)
% S = 100 % - 5,9 % = 94,1 %
>> Bài tiếp theo: Khoa học tự nhiên 7 Bài 8: Tốc độ chuyển động
IV. Trắc nghiệm Khoa học tự nhiên 7 Bài 8
Để có thể giúp bạn đọc nắm được các nội dung lý thuyết của bài, cũng như nâng cao kĩ năng, rèn luyện kĩ thuật làm bài tập. VnDoc đã biên soạn bộ câu hỏi trắc nghiệm có đáp án. Mời các bạn làm trực tiếp tại:
-------------------------------------------------
Ngoài lời giải chi tiết Khoa học tự nhiên 7 Bài 7: Hóa trị và công thức hóa học KNTT trên đây các bạn có thể tham khảo Toán lớp 7 tập 1 Kết nối tri thức và Ngữ Văn 7 Tập 1 Kết nối tri thức , Công Nghệ 7 KNTT,...... theo chuẩn kiến thức, kỹ năng của Bộ GD&ĐT ban hành. VnDoc.com liên tục cập nhật Lời giải, đáp án các dạng bài tập Chương trình sách mới cho các bạn cùng tham khảo.
Để lên kế hoạch bài dạy, chuẩn bị cho các bài học trên lớp cho chương trình sách mới lớp 7 GDPT đạt kết quả cao. Các thây cô tham khảo các nhóm mới lớp 7 sau đây. Đồng thời, các em học sinh tham khảo để chuẩn bị các bài giải sách mới đạt kết quả cao.
Tất cả các tài liệu tại đây được VnDoc chia sẻ miễn phí cho các bạn và thầy cô tham khảo.
