Khoa học tự nhiên 7 Bài 5: Giới thiệu về liên kết hóa học Cánh diều
Giải Khoa học tự nhiên 7 Cánh diều Bài 5 Giới thiệu về liên kết hóa học
- I. Câu hỏi thảo luận
- Câu 1 trang 33 SGK KHTN 7 Cánh diều
- Câu 2 trang 34 SGK KHTN 7 Cánh diều
- Câu 3 trang 34 SGK KHTN 7 Cánh diều
- Câu 4 trang 35 SGK KHTN 7 Cánh diều
- Câu 5 trang 35 SGK KHTN 7 Cánh diều
- Câu 6 trang 36 SGK KHTN 7 Cánh diều
- Câu 7 trang 37 SGK KHTN 7 Cánh diều
- Câu 8 trang 37 SGK KHTN 7 Cánh diều
- Câu 9 trang 38 SGK KHTN 7 Cánh diều
- II. Câu hỏi luyện tập
Khoa học tự nhiên 7 Bài 5: Giới thiệu về liên kết hóa học Cánh diều được VnDoc biên soạn hướng dẫn bạn đọc trả lời các nội dung câu hỏi bài tập SGK Khoa học tự nhiên lớp 7 Cánh diều Bài 5 Giới thiệu về liên kết hóa học. Hy vọng thông qua nội dung tài liệu sẽ giúp bạn đọc có thêm các thông tin, phương pháp làm bài tập hay, để học tập tốt hơn Khoa học tự nhiên lớp 7. Mời các bạn tham khảo chi tiết.
>> Bài trước đó: Khoa học tự nhiên 7 Bài 4: Phân tử, đơn chất, hợp chất Cánh diều
I. Câu hỏi thảo luận
Câu 1 trang 33 SGK KHTN 7 Cánh diều
Quan sát hình 5.1, hãy cho biết số electron ở lớp ngoài cùng của vỏ nguyên tử khí hiếm.
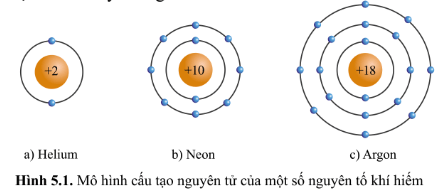
Hướng dẫn trả lời câu hỏi
Hình a) nguyên tử Helium có 2 electron lớp ngoài cùng.
Hình b) nguyên tử Neon có 8 electron lớp ngoài cùng.
Hình c) nguyên tử Argon có 8 electron lớp ngoài cùng.
Nhận xét: Lớp vỏ ngoài cùng của các nguyên tử khí hiếm đều có 8 electron (riêng He có 2 electron).
Câu 2 trang 34 SGK KHTN 7 Cánh diều
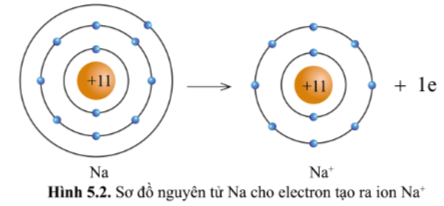
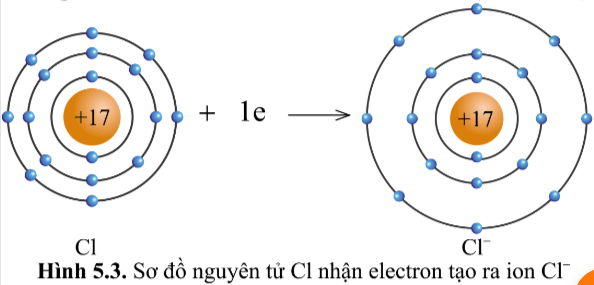
Quan sát hình 5.2 và hình 5.3, cho biết lớp vỏ của các ion Na+, Cl- tương tự vỏ nguyên tử của nguyên tố khí hiếm nào?
 |
 |
Hướng dẫn trả lời câu hỏi
Lớp vỏ của ion Na+ có 10 electron tương tự lớp vỏ nguyên tử của nguyên tố khí hiếm Neon (hình 5.1b)
Lớp vỏ của ion Cl- có 18 electron tương tự lớp vỏ nguyên tử của nguyên tố khí hiếm Argon (hình 5.1c)
Câu 3 trang 34 SGK KHTN 7 Cánh diều
Quan sát hình 5.2, hãy so sánh về số electron, số lớp electron giữa nguyên tử Na và ion Na+.

Hướng dẫn trả lời câu hỏi
Ion Na+ ít hơn 1 eletron so với nguyên tử Na .
Ion Na+ ít hơn một lớp electron so với nguyên tử Na .
Có thể nói nguyên tử Na cho đi 1 electron ở lớp ngoài cùng để trở thành ion mang điện tích dương, kí hiệu là Na+.
Câu 4 trang 35 SGK KHTN 7 Cánh diều
Quan sát các hình 5.5 và 5.6 cho biết các ion Mg2+ và O2- có lớp vỏ tương tự khí hiếm nào.
 |
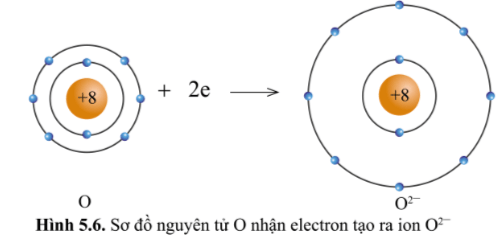 |
Hướng dẫn trả lời câu hỏi
Ion Mg2+ lớp vỏ có 10 electron tương tự như khí hiếm Neon (xem lại hình 5.1b)
Ion O2- lớp vỏ có 10 electron tương tự như khí hiếm Neon (xem lại hình 5.1b)
Câu 5 trang 35 SGK KHTN 7 Cánh diều
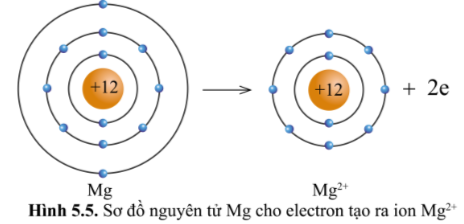
Quan sát hình 5.5, hãy so sánh về số electron, số lớp electron giữa nguyên tử Mg và ion Mg2+.

Hướng dẫn trả lời câu hỏi
Ion Mg2+ có ít hơn 2 electron so với nguyên tử Mg
Ion Mg2+ có ít hơn một lớp electron so nguyên tử Mg .
Nhận xét: Nguyên tử Mg cho đi 2 electron lớp ngoài cùng trở thành ion mang hai điện tích dương, kí hiệu là Mg2+.
Câu 6 trang 36 SGK KHTN 7 Cánh diều
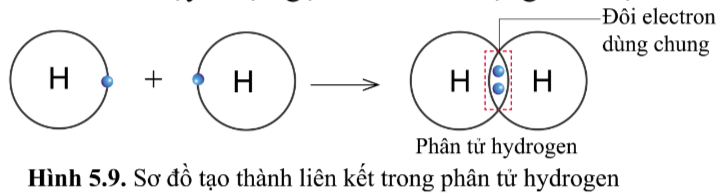
Quan sát hình 5.9, hãy cho biết nguyên tử H trong phân tử hydrogen có lớp vỏ tương tự khí hiếm nào.
Hướng dẫn trả lời câu hỏi
Trong phân tử hydrogen gồm hai nguyên tử H, mỗi nguyên tử H có 2 electron ở lớp vỏ.
Giống với lớp vỏ của khí hiếm Helium (xem lại hình 5.1a)
Câu 7 trang 37 SGK KHTN 7 Cánh diều
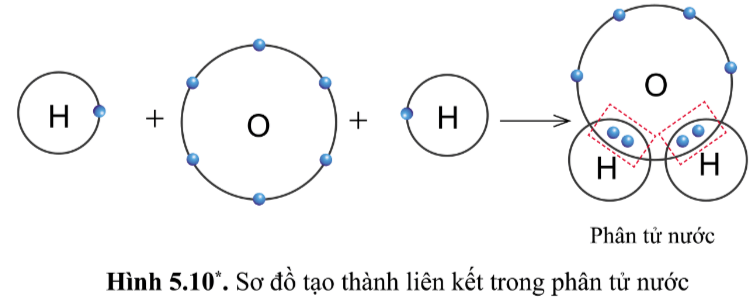
Quan sát hình 5.10, cho biết trong phân tử nước, mỗi nguyên tử H và O có bao nhiêu electron ở lớp ngoài cùng.
Hướng dẫn trả lời câu hỏi
Trong phân tử nước, nguyên tử O có 8 electron lớp ngoài cùng tương tự như khí hiếm.
Mỗi nguyên tử H có 2 electron lớp ngoài cùng tương tự như khí hiếm helium.
Câu 8 trang 37 SGK KHTN 7 Cánh diều
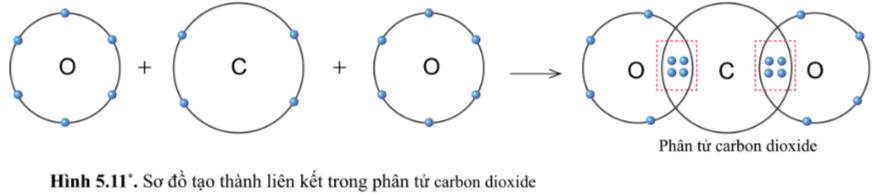
Quan sát hình 5.11, hãy cho biết trong phân tử khí carbonic nguyên tử C có bao nhiêu electron dùng chung với nguyên tử O.
Hướng dẫn trả lời câu hỏi
Trong phân tử khí carbonic, nguyên tử C có 4 electron dùng chung với nguyên tử O (mỗi nguyên tử O góp 2 electron).
Câu 9 trang 38 SGK KHTN 7 Cánh diều
So sánh một số tính chất chung của chất cộng hóa trị với chất ion.
Hướng dẫn trả lời câu hỏi
| Chất cộng hóa trị | Chất ion | |
| Trạng thái | Rắn, lỏng, khí | Rắn |
| Nhiệt độ sôi | Thấp | Cao |
| Nhiệt độ nóng chảy | Thấp | Cao |
| Tính dẫn điện | Tan trong nước tạo dung dịch dẫn điện | Nhiều chất không có khả năng dẫn điện (đường ăn, Ethanol,...) |
II. Câu hỏi luyện tập
Luyện tập 1 trang 35 KHTN 7 Cánh diều
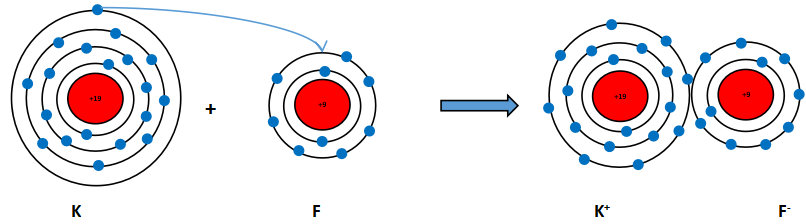
Số electron ở lớp ngoài cùng của nguyên tử K và F lần lượt là 1 và 7. Hãy cho biết khi K kết hợp với F để tạo thành phân tử potassium fluoride, nguyên tử K cho hay nhận bao nhiêu electron. Vẽ sơ đồ tạo thành liên kết trong phân tử potassium fluoride.
Hướng dẫn giải bài tập
Khi K kết hợp với F để tạo thành phân tử potassium fluoride sẽ diễn ra cho và nhận electron giữa hai nguyên tử như sau:
+ Nguyên tử K cho đi 1 electron ở lớp ngoài cùng trở thành ion mang điện tích dương, kí hiệu là K+.
+ Nguyên tử F nhận 1 electron từ nguyên tử K trở thành ion mang một điện tích âm, kí hiệu là F-.
Các ion K+ và F- hút nhau tạo thành liên kết trong phân tử sodium chloride.
Luyện tập 2 trang 35 KHTN 7 Cánh diều
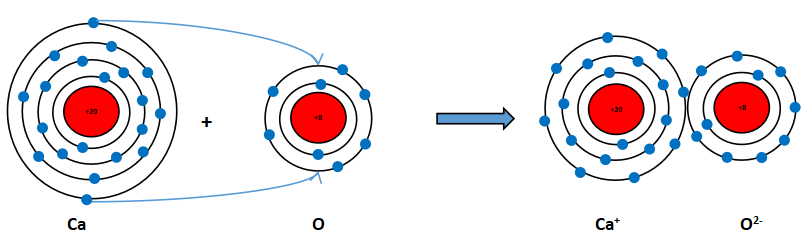
Nguyên tử Ca có 2 electron ở lớp ngoài cùng. Hãy vẽ sơ đồ tạo thành liên kết khi nguyên tử Ca kết hợp với nguyên tử O khi nguyên tử Ca kết hợp với nguyên tử O tạo ra phân tử calcium oxide.
Hướng dẫn giải bài tập
Khi Ca kết hợp với O tạo thành phân tử calcium oxide sẽ diễn ra sự cho và nhận electron giữa hai nguyên tử như sau:
+ Nguyên tử Ca cho đi 2 electron lớp ngoài cùng trở thành ion mang hai điện tích dương, kí hiệu là Ca2+.
+ Nguyên tử O nhận 2 electron từ nguyên tử Ca tạo thành ion mang điện tích âm kí hiệu là O2-.
Các ion Ca2+ và O2- hút nhau tạo thành liên kết trong phân tử calcium oxide.
Luyện tập 3 trang 36 KHTN 7 Cánh diều
Nguyên tử K kết hợp với nguyên tử Cl tạo thành phân tử potassium chloride. Theo em, ở điều kiện thường, potassium chloride là chất rắn, chất lỏng hay chất khí? Vì sao?
Hướng dẫn giải bài tập
Ở điều kiện thường, potassium chloride là chất rắn vì:
Khi nguyên tử K (kim loại điển hình) kết hợp với nguyên tử Cl (phi kim điển hình) thì kim loại K sẽ cho electron tạo thành ion dương, nguyên tử Cl sẽ nhận electron tạo thành ion âm. Các ion dương và ion âm hút nhau tạo ra hợp chất ion là potassium chloride.
Các hợp chất ion đều là chất rắn ở điều kiện thường.
Luyện tập 4 trang 36 KHTN 7 Cánh diều
Hai nguyên tử Cl liên kết với nhau tạo thành phân tử chlorine.
a) Mỗi nguyên tử Cl cần thêm bao nhiêu electron vào lớp ngoài cùng để có lớp vỏ tương tự khí hiếm?
b) Hãy vẽ sơ đồ tạo thành liên kết trong phân tử chlorine.
Hướng dẫn giải bài tập
a)
Nguyên tử Cl có 7 electron lớp ngoài cùng và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
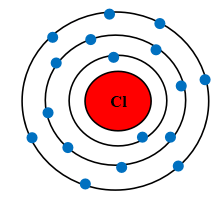
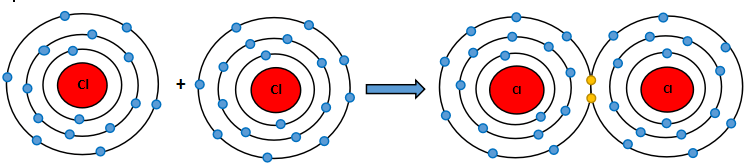
b) Khi hai nguyên tử Cl liên kết với nhau, mỗi nguyên tử góp 1 electron để tạo ra đôi electron dùng chung.
Hạt nhân của hai nguyên tử Cl cùng hút đôi electron dùng chung và liên kết với nhau tạo thành phân tử chlorine.
Luyện tập 5 trang 37 KHTN 7 Cánh diều
Mỗi nguyên tử H kết hợp với một nguyên tử Cl tạo thành phân tử hydrogen chloride. Hãy vẽ sơ đồ tạo thành phân tử hydrogen chloride từ nguyên tử H và nguyên tử Cl.
Hướng dẫn giải bài tập
Nguyên tử Cl có 7 electron lớp ngoài cùng và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
Nguyên tử H chỉ có 1 electron và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
Khi nguyên tử H kết hợp với nguyên tử Cl, nguyên tử Cl góp 1 electron, nguyên tử H góp 1 electron. Như vậy giữa nguyên tử H và nguyên tử Cl có 1 đôi electron dùng chung. Hạt nhân nguyên tử H và Cl cùng hút đôi electron dùng chung, liên kết với nhau tạo ra phân tử hydrogen chloride.
vẽ hình
Luyện tập 6 trang 37 KHTN 7 Cánh diều
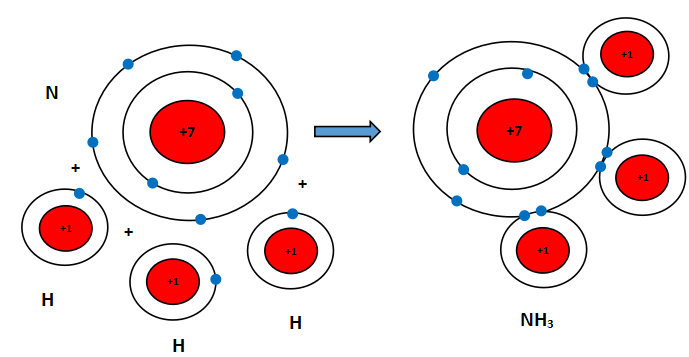
Mỗi nguyên tử N kết hợp với 3 nguyên tử H tạo thành phân tử ammonia. Hãy vẽ sơ đồ tạo thành liên kết trong phân tử ammonia.
Hướng dẫn giải bài tập
Nguyên tử N có 7 electron, trong đó có 5 electron lớp ngoài cùng, cần thêm 3 electron để có lớp vỏ bền vững tương tự khí hiếm.
Nguyên tử H chỉ có 1 electron và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
Khi N kết hợp với H, nguyên tử N góp 3 electron, mỗi nguyên tử H góp 1 electron. Như vậy giữa nguyên tử N và mỗi nguyên tử H có 1 đôi electron dùng chung. Hạt nhân nguyên tử N và H cùng hút đôi electron dùng chung, liên kết với nhau tạo ra phân tử ammonia.
Luyện tập 7 trang 37 KHTN 7 Cánh diều
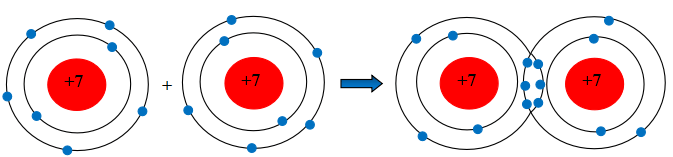
Hai nguyên tử N kết hợp với nhau tạo thành phân tử nitrogen. Hãy vẽ sơ đồ tạo thành liên kết trong phân tử nitrogen.
Hướng dẫn giải bài tập
Nguyên tử N có 7 electron, trong đó có 5 electron lớp ngoài cùng, cần thêm 3 electron để có lớp vỏ bền vững tương tự khí hiếm.
Khi hai nguyên tử N liên kết với nhau, mỗi nguyên tử góp chung 3 electron để tạo ra 3 cặp electron dùng chung. Hạt nhân của hai nguyên tử N cùng hút các đôi electron dùng chung và liên kết với nhau tạo thành phân tử nitrogen.
>> Bài tiếp theo: Khoa học tự nhiên 7 Bài 6: Hóa trị, công thức hóa học
----------------------------
Ngoài lời giải chi tiết Khoa học tự nhiên 7 Bài 5: Giới thiệu về liên kết hóa học Cánh diều trên đây các bạn có thể tham khảo Toán lớp 7 Tập 1 Cánh diều và Ngữ Văn 7 tập 1 Cánh diều, Tiếng Anh 7 Cánh Diều ,Công nghệ 7 Cánh diều theo chuẩn kiến thức, kỹ năng của Bộ GD&ĐT ban hành. VnDoc.com liên tục cập nhật Lời giải, đáp án các dạng bài tập Chương trình sách mới cho các bạn cùng tham khảo.
