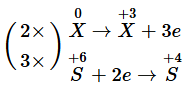Khi xảy ra va chạm mạnh, NaN3 phân hủy rất nhanh tạo khí N2 làm túi khí phồng lên
Xét tính đúng sai các phát biểu sau:
a. Phương trình hóa học của phản ứng phân hủy sodium azide được cân bằng là:
b. Phản ứng trên không phải là phản ứng oxi hóa – khử vì chỉ là phản ứng phân hủy một chất thành các chất đơn giản hơn.
c. Trong hợp chất NaN3, số oxi hóa của Na là +1 và số oxi hóa trung bình của N là .
d. Trong phản ứng NaN3 phân hủy, N bị oxi hóa còn Na bị khử.
Khi xảy ra va chạm mạnh, NaN3 phân hủy rất nhanh tạo khí N2 làm túi khí phồng lên
Xét tính đúng sai các phát biểu sau:
a. Phương trình hóa học của phản ứng phân hủy sodium azide được cân bằng là:
![]()
b. Phản ứng trên không phải là phản ứng oxi hóa – khử vì chỉ là phản ứng phân hủy một chất thành các chất đơn giản hơn.
c. Trong hợp chất NaN3, số oxi hóa của Na là +1 và số oxi hóa trung bình của N là ![]() .
.
d. Trong phản ứng NaN3 phân hủy, N bị oxi hóa còn Na bị khử.
a) Đúng
b) Sai vì Phản ứng này là phản ứng oxi hóa – khử vì có sự thay đổi số oxi hóa.
c) Đúng Trong NaN3: Na = + 1 → tổng số oxi hóa bằng 0 ⇒ trung bình mỗi N = .
d) Sai Trong phản ứng:
N: → 0 → bị oxi hóa .
Na: +1→ 0 → bị khử.