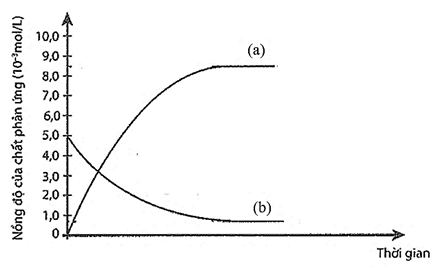
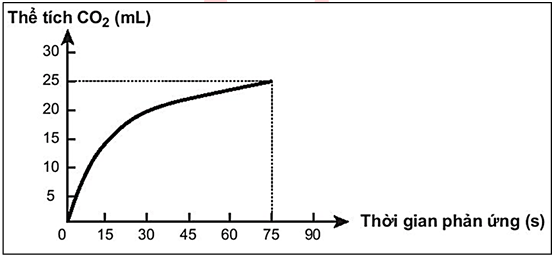
Cho bột Fe vào dung dịch HCl loãng, sau đó đun nóng hỗn hợp. Xét các phát biểu sau:
a. Khi đun nóng, khí H2 thoát ra nhanh hơn. Đúng||Sai
b. Khi đun nóng, bột Fe tan nhanh hơn. Đúng||Sai
c. Khi đun nóng, lượng muối FeCl2 thu được nhiều hơn. Sai||Đúng
d. Khi đun nóng, nồng độ HCl giảm nhanh hơn. Đúng||Sai
Cho bột Fe vào dung dịch HCl loãng, sau đó đun nóng hỗn hợp. Xét các phát biểu sau:
a. Khi đun nóng, khí H2 thoát ra nhanh hơn. Đúng||Sai
b. Khi đun nóng, bột Fe tan nhanh hơn. Đúng||Sai
c. Khi đun nóng, lượng muối FeCl2 thu được nhiều hơn. Sai||Đúng
d. Khi đun nóng, nồng độ HCl giảm nhanh hơn. Đúng||Sai
a. Đúng
b. Đúng
c. Sai vì Đun nóng phản ứng làm tốc độ phản ứng tăng ⇒ Khí H2 thoát ra nhanh hơn, bột Fe tan nhanh hơn, nồng độ HCl giảm nhanh hơn, thu được muối nhanh hơn.
d. Đúng