Giải bài tập Hóa học 11 SBT bài 2
Giải bài tập Hóa học 11 SBT bài Axit, bazơ và muối
VnDoc xin giới thiệu tới bạn đọc tài liệu Giải bài tập Hóa học 11 SBT bài 2. Tài liệu kèm theo lời giải chi tiết sẽ giúp các bạn học sinh giải Hoá 11 nhanh và hiệu quả hơn. Mời các bạn tham khảo chi tiết bài viết dưới đây nhé.
Giải bài tập Hóa học 11 SBT bài Axit, bazơ và muối vừa được VnDoc.com sưu tập và xin gửi tới bạn đọc cùng tham khảo. Bài viết được tổng hợp gồm có lời giải của 7 bài tập trong sách bài tập môn Hóa học lớp 11 bài Axit, bazơ và muối. Mời các bạn cùng tham khảo chi tiết và tải về tại đây nhé.
Bài tập trắc nghiệm 1.8, 1.9, 1.10 trang 4 sách bài tập (SBT) hóa học 11
1.8. Theo A-rê-ni-ut chất nào dưới đây là axit?
A. Cr(N03)3
B. HBr03
C. CdS04
D. CsOH
1.9. Theo A-rê-ni-ut chất nào được đưa ra ở câu 1.8 là bazơ?
1.10. Axit mạnh HN03 và axit yếu HN02 có cùng nồng độ 0,1 mol/l và ở cùng nhiệt độ. Sự so sánh nồng độ mol ion nào sau đây là đúng?
A. [H+]HN03 < [H+]HN02
B. [H+]HN03 > [H+]HN02
C. [H+]HN03 =[H+]HN02
D. [NO3-]HN03 < [NO3-]HN02
Hướng dẫn trả lời:
1.8. B
1.9. D
1.10. B
Bài tập 1.11 trang 4 sách bài tập (SBT) hóa học 11
1.11. Viết phương trình điện li của các chất sau trong dung dịch:
1. Axit mạnh H2Se04 (nấc thứ nhất điện li mạnh).
2. Axit yếu ba nấc H3P04.
3. Hiđroxit lưỡng tính Pb(OH)2.
4. Na2HP04.
5. NaH2P04.
6. Axit mạnh HMn04.
7. Bazơ mạnh RbOH.
Hướng dẫn trả lời:
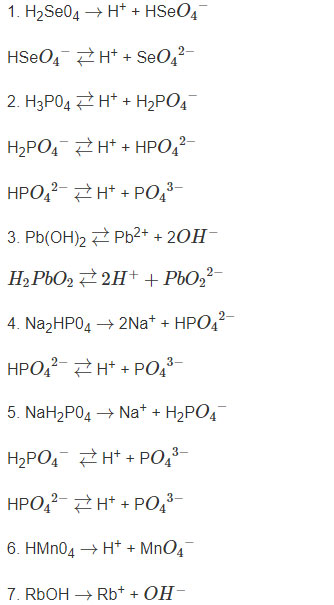
Bài tập 1.12 trang 5 sách bài tập (SBT) hóa học 11
1.12. Các muối thường gọi là "không tan", ví dụ BaS04, AgCl có phải là các chất điện li mạnh không? Giải thích, biết rằng ở 25°C độ hoà tan trong nước của BaS04 là 1,0.10-5 mol/l, của AgCl là 1,2.10-5 mol/l. Dung dịch các muối này chỉ chứa các ion, không chứa các phân tử hoà tan.
Hướng dẫn trả lời:
BaS04 và AgCl là các chất điện li mạnh, vì các phân tử hoà tan của chúng đều phân li ra ion.
Bài tập 1.13 trang 5 sách bài tập (SBT) hóa học 11
1.13. Hai chất điện li mạnh A và B khi tan trong nước phân li ra a mol Mg2+, b mol Na+, c mol SO4- và d mol Cl:
1. Biết a = 0,001 ; b = 0,01 ; c = 0,005 ; vậy d bằng bao nhiêu?
2. Viết công thức phân tử của A và B.
Hướng dẫn trả lời:
1. Trong dung dịch, điện tích của các cation bằng điện tích của các anion, nên:
2a + b = 2c + d
0,001.2 + 0,01 = 0,005.2 + d
⇒ d = 0,002
2. MgCl2 và Na2S04.
Bài tập 1.14 trang 5 sách bài tập (SBT) hóa học 11
1.14*. Trong một dung dịch CH3COOH, người ta xác định được nồng độ H+ bằng 3.10-3M và nồng độ CH3COOH bằng 3,97.10-1M. Tính nồng độ mol ban đầu của CH3COOH
Hướng dẫn trả lời:
Gọi C là nồng độ moi ban đầu của CH3COOH, ta có:
CH3COOH ![]() CH3COO− + H+
CH3COO− + H+
(C - 3.10-3)M 3.10-3M 3.10-3M
C - 3.10-3 = 3,97.10-1 = 397.10-3
C = 397.10-3 + 3.10-3 = 400.10-3
⇒ C = 0,4M.
----------------------------------
Trên đây VnDoc.com đã giới thiệu tới bạn đọc tài liệu: Giải bài tập Hóa học 11 SBT bài 2 Axit, bazơ và muối. Mong rằng qua bài viết này các bạn có thêm tài liệu để học tập tốt hơn môn Hóa học lớp 11 nhé. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Sinh học lớp 11, Vật lý lớp 11, Giải bài tập Hóa học lớp 11, Giải bài tập Toán 11 mà VnDoc tổng hợp và đăng tải.
Mời bạn đọc cùng tham gia nhóm Tài liệu học tập lớp 11 để có thêm tài liệu học tập nhé





