Giải bài tập Hóa học 11 SBT bài 25
Giải bài tập Hóa học 11 SBT bài Ankan
- Bài tập trắc nghiệm 5.1, 5.2, 5.3 trang 35 sách bài tập (SBT) hóa học 11
- Bài tập trắc nghiệm 5.4, 5.5, 5.6, 5.7, 5.8, 5.9 trang 36 sách bài tập (SBT) hóa học 11
- Bài tập 5.10 trang 36 sách bài tập (SBT) hóa học 11
- Bài tập 5.11 trang 37 sách bài tập (SBT) hóa học 11
- Bài tập 5.12 trang 37 sách bài tập (SBT) hóa học 11
- Bài tập 5.13 trang 37 sách bài tập (SBT) hóa học 11
- Bài tập 5.14 trang 37 sách bài tập (SBT) hóa học 11
- Bài tập 5.15 trang 37 sách bài tập (SBT) hóa học 11
- Bài tập 5.16 trang 37 sách bài tập (SBT) hóa học 11
- Bài tập 5.17 trang 38 sách bài tập (SBT) hóa học 11
VnDoc xin giới thiệu tới các bạn học sinh Giải bài tập Hóa học 11 SBT bài 25. Chắc chắn bộ tài liệu sẽ giúp các bạn học sinh sẽ giải bài tập Hóa học lớp 11 tốt hơn. Mời các bạn học sinh và thầy cô cùng tham khảo chi tiết bài viết dưới đây nhé.
Giải bài tập Hóa học 11 SBT bài 25 Ankan vừa được VnDoc.com sưu tập và xin gửi tới bạn đọc cùng tham khảo. Bài viết được tổng hợp gồm có lời giải của 17 bài tập trong sách bài tập môn Hóa học lớp 11 bài Ankan. Quan bài viết bạn đọc có thể thấy được khái niệm về ankan, số liên kết cộng hoá trị trong một phân tử, cách viết công thức cấu tạo... Mời các bạn cùng tham khảo chi tiết và tải về tại đây nhé.
Bài tập trắc nghiệm 5.1, 5.2, 5.3 trang 35 sách bài tập (SBT) hóa học 11
5.1. Cho các từ và cụm từ sau: ankan, xicloankan, hiđrocacbon no, hiđrocacbon không no, phản ứng thế. Hãy điền vào chỗ khuyết những từ thích hợp.
Hiđrocacbon mà phân tử chỉ có liên kết đơn được gọi là (1);
Hiđrocacbon no có mạch không vòng được gọi là (2);
Hiđrocacbon no có một mạch vòng được gọi là (3);
Tính chất hoá học đặc trưng của hiđrocacbon no là (4).
5.2. Trong các nhận xét dưới đây, nhận xét nào sai?
A. Tất cả các ankan đều có công thức phân tử CnH2n+2.
B. Tất cả các chất có công thức phân tử CnH2n+2 đều là ankan.
C. Tất cả các ankan đều chỉ có liên kết đơn trong phân tử.
D. Tất cả các chất chỉ có liên kết đơn trong phân tử đều là ankan.
5.3. Chất có tên là gì?
A. 3-isopropylpentan
B. 2-metyl-3-etylpentan
C. 3-etyl-2-metylpentan
D. 3-etyl-4-metylpentan
Hướng dẫn trả lời:
5.1.
(1) : hiđrocacbon no;
(2) : ankan;
(3) : xicloankan;
(4) : phản ứng thế.
5.2. D.
5.3. C.
Bài tập trắc nghiệm 5.4, 5.5, 5.6, 5.7, 5.8, 5.9 trang 36 sách bài tập (SBT) hóa học 11
5.4 Cho công thức:
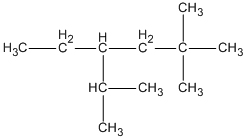
A. 3-isopropyl-5,5-đimetylhexan.
B. 2,2-đimetyl-4-isopropylhexan.
C. 3-etyl-2,5,5-trimetylhexan.
D. 4-etyl-2,5,5-trimetylhexan.
Trong 4 tên đó, tên nào đúng với công thức ở trên?
5.5. Tổng số liên kết cộng hoá trị trong một phân tử C3H8 là bao nhiêu?
A. 11
B. 10
C. 3
D. 8
5.6. Hai chất 2-metylpropan và butan khác nhau về
A. Công thức cấu tạo.
B. công thức phân tử.
C. số nguyên tử cacbon.
D. số liên kết cộng hoá trị.
5.7. Tất cả các ankan có cùng công thức gì?
A. Công thức đơn giản nhất
B. Công thức chung
C. Công thức cấu tạo
D. Công thức phân tử
5.8. Trong các chất dưới đây, chất nào có nhiệt độ sôi thấp nhất?
A. Butan
B. Etan
C. Metan
D. Propan
5.9. Gọi tên IUPAC của các ankan có công thức sau đây:
1. (CH3)2CH−CH2−C(CH3)3 (tên thông dụng là isooctan)
2. CH3−CH2−CH(CH3)−CH(CH3)−[CH2]4−CH(CH3)2
Hướng dẫn trả lời:
5.4. D
5.5. B
5.6. A
5.7. B
5.8. C
5.9.
1. 2,2,4-trimetylpentan
2. 3,4,9-trimetylđecan
Bài tập 5.10 trang 36 sách bài tập (SBT) hóa học 11
5.5. Viết công thức cấu tạo thu gọn của:
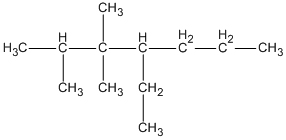
1. 4-etyl-2,3,3-trimetylheptan.
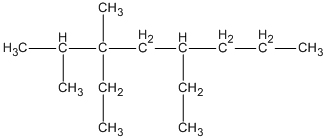
2. 3,5-đietyl-2,2,3-trimetyloctan.
Hướng dẫn trả lời:
1.
2. 
Bài tập 5.11 trang 37 sách bài tập (SBT) hóa học 11
5.5. Chất A là một ankan thể khí. Để đốt cháy hoàn toàn 1,2 lít A cần dùng vừa hết 6,0 lít oxi lấy ở cùng điểu kiện.
1. Xác định công thức phân tử chất A.
2. Cho chất A tác dụng với khí clo ở 25°c và có ánh sáng. Hỏi có thể thu được mấy dẫn xuất monoclo của A? Cho biết tên của mỗi dẫn xuất đó. Dẫn xuất nào thu được nhiều hơn?
Hướng dẫn trả lời:
1. ![]() \({C_n}{H_{2n + 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
\({C_n}{H_{2n + 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
Đối với các chất khí, tương quan về số mol trùng với tương quan vể thể tích. Vì thế từ phương trình hoá học ở trên, ta có:
Cứ 1 lít ankan tác dụng với ![]() \(\frac{{3n + 1}}{2}\) lít O2
\(\frac{{3n + 1}}{2}\) lít O2
Cứ 1,2 lít ankan tác dụng với 6,0 lít O2.
![]() \(\frac{{3n + 1}}{2} = \frac{6}{{1,2}} = 5\) ⇒ n = 3; CTPT chất A là C3H8.
\(\frac{{3n + 1}}{2} = \frac{6}{{1,2}} = 5\) ⇒ n = 3; CTPT chất A là C3H8.
2.
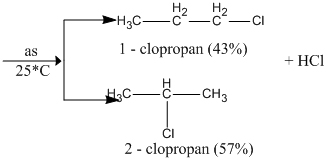
![]() \(C{H_3} - C{H_2} - C{H_3} + C{l_2}\)
\(C{H_3} - C{H_2} - C{H_3} + C{l_2}\)
Bài tập 5.12 trang 37 sách bài tập (SBT) hóa học 11
5.12. Để đốt cháy hoàn toàn 1,45 g một ankan phải dùng vừa hết 3,64 lít O2 (lấy ở đktc).
1. Xác định công thức phân tử của ankan đó.
2. Viết công thức cấu tạo các đổng phân ứng với công thức phân tử đó. Ghi tên tương ứng.
Hướng dẫn trả lời:
1. ![]() \({C_n}{H_{2n + 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
\({C_n}{H_{2n + 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
Theo phương trình: Cứ (14n + 2) gam ankan tác dụng với ![]() \(\frac{{3n + 1}}{2}\) mol O2
\(\frac{{3n + 1}}{2}\) mol O2
Theo đẩu bài: Cứ 1,45 gam ankan tác dụng với ![]() \(\frac{{3,64}}{22,4}\) mol O2
\(\frac{{3,64}}{22,4}\) mol O2
![]() \(\frac{{14n + 2}}{{1,45}} = \frac{{3n + 1}}{{{{3,25.10}^{ - 1}}}} \Rightarrow n = 4\)
\(\frac{{14n + 2}}{{1,45}} = \frac{{3n + 1}}{{{{3,25.10}^{ - 1}}}} \Rightarrow n = 4\)
CTPT: C4H10
2. CTCT: CH3 -CH2 -CH2 -CH3
butan
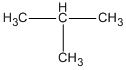
isobutan (2-metylpropan)
Bài tập 5.13 trang 37 sách bài tập (SBT) hóa học 11
5.13. Khi đốt cháy hoàn toàn 1,8 g một ankan, người ta thấy trong sản phẩm tạo thành khối lượng CO2 nhiều hơn khối lượng H2O là 2,8 g.
1. Xác định công thức phân tử của ankan mang đốt.
2. Viết công thức cấu tạo và tên tất cả các đồng phân ứng với công thức phân tử đó.
Hướng dẫn trả lời:
1. ![]() \({C_n}{H_{2n + 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
\({C_n}{H_{2n + 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
Khi đốt (14n + 2) g ankan thì khối lượng CO2 thu được nhiều hơn khối lượng H2O là 44n - 18(n + 1) = (26n - 18) g.
![]() \(\frac{{14n + 2}}{{1,8}} = \frac{{26n - 18}}{{2,8}} \Rightarrow n = 5\)
\(\frac{{14n + 2}}{{1,8}} = \frac{{26n - 18}}{{2,8}} \Rightarrow n = 5\)
CTPT: C5H12
2. CTCT: CH3 - CH2 - CH2 - CH2 - CH3
pentan
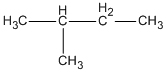
2-metylbutan (isopentan)
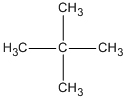
2,2-đimetylpropan (neopentan)
Bài tập 5.14 trang 37 sách bài tập (SBT) hóa học 11
5.14. Đốt cháy hoàn toàn 2,86 g hỗn hợp gồm hexan và octan người ta thu được 4,48 lít CO2 (đktc).
Xác định phần trăm về khối lượng của từng chất trong hỗn hợp ankan mang đốt.
Hướng dẫn trả lời:
Đặt lượng C6H14 là X mol, lượng C8H18 là y mol:
86x+ 114y = 2,86 (1)
2C6H14 + 19O2 ⇒ 12CO2 + 14H2O
x mol 6x mol
2C8H18 + 25O2 ⇒ 16CO2 + 18H2O
y mol 8y mol
1 48
Số mol CO2: 6x + 8y = ![]() \(\frac{{4,48}}{{22,4}}\) = 0,2. (2)
\(\frac{{4,48}}{{22,4}}\) = 0,2. (2)
Giải hệ phương trình (1) và (2), ta được x = 0,02 ; y = 0,01.
% về khối lương cùa C6H14: ![]() \(\frac{{0,02.86}}{{2,86}}\). 100% = 60,1%.
\(\frac{{0,02.86}}{{2,86}}\). 100% = 60,1%.
% về khối lượng của C8H18: 100% - 60,1% = 39,9%.
Bài tập 5.15 trang 37 sách bài tập (SBT) hóa học 11
5.15. Một loại xăng là hỗn hợp của các ankan có công thức phân tử là C7H16 và C8H18. Để đốt cháy hoàn toàn 6,95 g xăng đó phải dùng vừa hết 17,08 lít O2 (lấy ở đktc).
Xác định phần trăm về khối lượng của từng chất trong loại xăng đó.
Hướng dẫn trả lời:
Đặt lượng C7H16 là x mol, lượng C8H18 là y mol.
100x + 114y = 6,95 (1)
![]() \({C_7}{H_{16}} + 11{O_2} \to 7C{O_2} + 8{H_2}O\)
\({C_7}{H_{16}} + 11{O_2} \to 7C{O_2} + 8{H_2}O\)
x mol 11x mol
![]() \(2{C_8}{H_{18}} + 25{O_2} \to 16C{O_2} + 18{H_2}O\)
\(2{C_8}{H_{18}} + 25{O_2} \to 16C{O_2} + 18{H_2}O\)
y mol 12,5 y mol
![]() \(11x+12,5y=\frac{17,08}{22,4}=0,7625\ (2)\)
\(11x+12,5y=\frac{17,08}{22,4}=0,7625\ (2)\)
Từ (1) và (2), tìm được x = 0,0125 ; y = 0,05.
% về khối lượng của C7H16: ![]() \(\frac{{0,0125.100}}{{6,95}}\). 100% = 18,0%.
\(\frac{{0,0125.100}}{{6,95}}\). 100% = 18,0%.
% về khối lượng của C8H18: 100% - 18% = 82,0%.
Bài tập 5.16 trang 37 sách bài tập (SBT) hóa học 11
5.16. Hỗn hợp M chứa hai ankan kế tiếp nhau trong dãy đồng đẳng. Để đốt cháy hoàn toàn 22,20 g M cần dùng vừa hết 54,88 lít O2 (lấy ở đktc).
Xác định công thức phân tử và phần trăm về khối lượng của từng chất trong hỗn hợp
Hướng dẫn trả lời:
Cách 1:
Giả sử trong 22,2 g hỗn hợp M có x mol ![]() \({C_n}{H_{2n + 2}}\) và y mol
\({C_n}{H_{2n + 2}}\) và y mol ![]() \({C_{n + 1}}{H_{2n + 4}}\)
\({C_{n + 1}}{H_{2n + 4}}\)
(14n + 2)x + (14n + 16)y = 22,2 (1)
![]() \({C_n}{H_{2n + 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
\({C_n}{H_{2n + 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
x mol ![]() \(\frac{{3n + 1}}{2}\)x mol
\(\frac{{3n + 1}}{2}\)x mol
![]() \({C_{n + 1}}{H_{2n + 4}} + \frac{{3n + 4}}{2}{O_2} \to (n + 1)C{O_2} + (n + 2){H_2}O\)
\({C_{n + 1}}{H_{2n + 4}} + \frac{{3n + 4}}{2}{O_2} \to (n + 1)C{O_2} + (n + 2){H_2}O\)
y mol ![]() \(\frac{{3n + 4}}{2}\)y mol
\(\frac{{3n + 4}}{2}\)y mol
Số mol ![]() \(O_2=\frac{(3n+1)x+(3n+4)y}{2}=\frac{54,88}{22,4}=2,45\ (mol)\)
\(O_2=\frac{(3n+1)x+(3n+4)y}{2}=\frac{54,88}{22,4}=2,45\ (mol)\)
⇒ (3n + 1)x + (3n + 4)y = 4,9 (2)
Nhân (2) với 14: (42n + 14)x + (42n + 56)y = 68,6 (2')
Nhân (1) với 3: (42n + 6)x + (42n + 48)y = 66,6 (1')
Lấy (2') trừ đi (1'): 8x + 8y = 2
x + y =0,25
Biến đổi (2) : 3n(x + y) + x + 4y = 4,9
Thay x + y = 0,25 0,75n + 0,25 + 3y = 4,9
⇒ 3y = 4,65 - 0,75n
y = 1,55 - 0,25n
Vì 0 < y < 0,25 ⇒0 < 1,55 - 0,25n < 0,25
5,2 < n < 6,2
n = 6 ⇒ y = 1,55 - 0,25.6 = 5.![]() \({10^{ - 2}}\)
\({10^{ - 2}}\)
x = 0,25 - 5.![]() \({10^{ - 2}}\)= 0,2
\({10^{ - 2}}\)= 0,2
% về khối lượng C6H14 trong hỗn hợp M: ![]() \(\frac{{0,2.86}}{{22,2}}\). 100% = 77,48%.
\(\frac{{0,2.86}}{{22,2}}\). 100% = 77,48%.
% về khối lượng C7H16 trong hỗn hợp M: 100% - 77,48% = 22,52%.
Cách 2:
Đặt công thức chung của hai ankan là ![]() \({C_{\overline n }}{H_{2\overline n + 2}}\)
\({C_{\overline n }}{H_{2\overline n + 2}}\)
![]() \({C_{\overline n }}{H_{2\overline n + 2}} + \frac{{3\overline n + 1}}{2}{O_2} \to \overline n C{O_2} + (\overline n + 1){H_2}O\)
\({C_{\overline n }}{H_{2\overline n + 2}} + \frac{{3\overline n + 1}}{2}{O_2} \to \overline n C{O_2} + (\overline n + 1){H_2}O\)
Theo phương trình: Cứ ![]() \((14{\overline n } + 2)g\) ankan tác dụng với
\((14{\overline n } + 2)g\) ankan tác dụng với ![]() \(\frac{3\overline{n}+1}{2}mol\ O_2\)
\(\frac{3\overline{n}+1}{2}mol\ O_2\)
Theo đầu bài: cứ 22,2 g ankan tác dụng với ![]() \(\frac{54,88}{22,4}mol\ O_2\)
\(\frac{54,88}{22,4}mol\ O_2\)
![]() \(\frac{{14\overline n + 2}}{{22,2}} = \frac{{3\overline n + 1}}{{2.2,45}} \Rightarrow \overline n = 6,2\)
\(\frac{{14\overline n + 2}}{{22,2}} = \frac{{3\overline n + 1}}{{2.2,45}} \Rightarrow \overline n = 6,2\)
Vậy công thức phân tử hai ankan là C6H14 và C7H16
Đặt lượng C6H14 là x mol, lượng C7H16 là y mol
 \(\left\{ \begin{array}{l}
86{\rm{x}} + 100y = 22,2\\
\frac{{6{\rm{x + 7y}}}}{{x + y}} = 6,2
\end{array} \right. \Rightarrow \left\{ \begin{array}{l}
x = {2.10^{ - 1}}\\
y = {5.10^{ - 2}}
\end{array} \right.\)
\(\left\{ \begin{array}{l}
86{\rm{x}} + 100y = 22,2\\
\frac{{6{\rm{x + 7y}}}}{{x + y}} = 6,2
\end{array} \right. \Rightarrow \left\{ \begin{array}{l}
x = {2.10^{ - 1}}\\
y = {5.10^{ - 2}}
\end{array} \right.\)
Từ đó, tính được C6H14 chiếm 77,48% ; C7H16 chiếm 22,52% khối lượng hỗn hợp M.
Bài tập 5.17 trang 38 sách bài tập (SBT) hóa học 11
5.17. Hỗn hợp X chứa ancol etylic (C2H5OH) và hai ankan kế tiếp nhau trong dãy đồng đẳng. Khi đốt cháy hoàn toàn 18,9 g X, thu được 26,10 g H2O và 26,88 lít CO2 (đktc).
Xác định công thức phân tử và phần trăm về khối lượng của từng ankan trong hỗn hợp X.
Hướng dẫn trả lời:
5.12. Giả sử trong 18,9 g hỗn hợp X có x mol ancol etylic và y mol hai ankan (công thức chung ![]() \({C_{\overline n }}{H_{2\overline n + 2}}\)).
\({C_{\overline n }}{H_{2\overline n + 2}}\)).
![]() \(46x+(14\overline{n}+2)y=18,90\ (1)\)
\(46x+(14\overline{n}+2)y=18,90\ (1)\)
![]() \({C_2}{H_5}OH + 3{O_2} \to 2C{O_2} + 3{H_2}O\)
\({C_2}{H_5}OH + 3{O_2} \to 2C{O_2} + 3{H_2}O\)
x mol 2x mol 3x mol
![]() \({C_{\overline n }}{H_{2\overline n + 2}} + \frac{{3\overline n + 1}}{2}{O_2} \to \overline n C{O_2} + (\overline n + 1){H_2}O\)
\({C_{\overline n }}{H_{2\overline n + 2}} + \frac{{3\overline n + 1}}{2}{O_2} \to \overline n C{O_2} + (\overline n + 1){H_2}O\)
y mol ![]() \(\overline{n}y\ mol\)
\(\overline{n}y\ mol\) ![]() \((\overline{n}+1)\ mol\)
\((\overline{n}+1)\ mol\)
Số mol ![]() \(CO_2=2x+\overline{n}y=\frac{26,88}{22,4}=1,2\ (2)\)
\(CO_2=2x+\overline{n}y=\frac{26,88}{22,4}=1,2\ (2)\)
Số mol ![]() \({H_2}O = 3x + (\overline n + 1)y = \frac{{26,1}}{{18}} = 1,45 (3)\)
\({H_2}O = 3x + (\overline n + 1)y = \frac{{26,1}}{{18}} = 1,45 (3)\)
Giải hệ phương trình (1), (2), (3) tìm được x = 0,1 ; y = 0,15 ; ![]() \(\overline n\) = 6,6
\(\overline n\) = 6,6
Công thức của hai ankan là C6H14 và C7H16.
Đặt lượng C6H14 là a mol, lượng C7H16 là b mol:
![]() \(\left\{ \begin{array}{l}
a + b = 0,15\\
86{\rm{a}} + 100b = 18,9 - 46.0,1 = 14,3
\end{array} \right. \Rightarrow \left\{ \begin{array}{l}
a = 0,05\\
b = 0,1
\end{array} \right.\)
\(\left\{ \begin{array}{l}
a + b = 0,15\\
86{\rm{a}} + 100b = 18,9 - 46.0,1 = 14,3
\end{array} \right. \Rightarrow \left\{ \begin{array}{l}
a = 0,05\\
b = 0,1
\end{array} \right.\)
% về khối lương của C6H14: ![]() \(\frac{{0,05.86}}{{18,9}}\). 100% = 22,75%.
\(\frac{{0,05.86}}{{18,9}}\). 100% = 22,75%.
% về khối lượng của C7H16: ![]() \(\frac{{0,1.100}}{{18,9}}\). 100% = 52,91%.
\(\frac{{0,1.100}}{{18,9}}\). 100% = 52,91%.
Để có kết quả học tập lớp 11 tốt hơn. VnDoc Mời các bạn tham khảo thêm các bài viết dưới đây của chúng tôi:
- Giải bài tập Hóa học 11 SBT bài 23
- Giải bài tập Hóa học 11 SBT bài 24
- Câu hỏi trắc nghiệm Ankan - Phần 1
- Bài tập về ankan và xicloankan
----------------------------------
Trên đây VnDoc đã giới thiệu tới bạn đọc Giải bài tập Hóa học 11 SBT bài 25 Ankan. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Sinh học 11, Giải bài tập Vật lý 11, Giải bài tập Hóa học 11, Giải bài tập Toán 11 mà VnDoc tổng hợp và đăng tải.
Mời bạn đọc cùng tham gia nhóm Tài liệu học tập lớp 11 để có thêm tài liệu học tập nhé
