Giải Hóa 11 Bài 29: Anken
Giải bài tập Hóa học 11 bài 29: Anken
VnDoc xin giới thiệu tới các bạn học sinh và thầy cô tài liệu Giải Hóa 11 Bài 29: Anken, chắc chắn bộ tài liệu sẽ là nguồn thông tin hữu ích để giúp các bạn học sinh rèn luyện giải bài tập Hóa học 11 một cách đơn giản hơn. Cũng như đưa ra các nội dung câu hỏi lý thuyết, bài tập liên quan, giúp củng cố nâng cao kĩ năng, thao tác giải bài tập một cách chính xác nhất. Mời các bạn tham khảo chi tiết nội dung dưới đây.
A. Tóm tắt lý thuyết hóa 11 bài 29
1. Đồng đẳng, đồng phân, danh pháp
CTTQ dãy đồng đẳng CnH2n (n ≥ 2)
Đồng phân cấu tạo: Anken từ C4H8 trở đi có đồng phân cấu tạo mạch cacbon và vị trí nối đôi.
Đồng phân hình học: Nếu mỗi C mang liên kết đôi dính với 2 nhóm nguyên tử khác nhau thì sẽ có 2 cách phân bố không gian khác nhau là đồng phân cis và trans.
Cách đọc tên đồng phân hình học: ghi tiền tố cis- trans- trước tên gọi anken
Tên thông thường của một số ít anken lấy tên từ ankan tương ứng, nhưng đổi hậu tố an thành ilen.
Tên thay thế: số chỉ vị trí nhánh – Tên nhánh + Tên mạch chính – Số chỉ vị trí liên kết đôi – en
2. Tính chất vật lý
Ở điều kiện thường, các anken từ C2 → C4 ở dạng khí, từ C5 trở đi là chất lỏng hoặc rắn
Nhiệt độ sôi, nhiệt độ nóng chảy và khối lượng riêng tăng dần theo chiều tăng của phân tử khối
Anken nhẹ hơn nước và không tan trong nước
3. Tính chất hóa học
Trong phân tử anken có 1 π kém bền nên có phản ứng đặc trưng là phản ứng cộng
a. Phản ứng cộng
Cộng hiđro : CnH2n + H2 ![]() \(\overset{Ni, t^{\circ } }{\rightarrow}\)CnH2n + 2
\(\overset{Ni, t^{\circ } }{\rightarrow}\)CnH2n + 2
Cộng halogen: CnH2n + X2 → CnH2nX2
Cộng HA: Cộng nước, hiđro halogenua, axit sulfuric đậm đặc,…
PTTQ: CnH2n+ HA → CnH2n + 1A (A là X, OSO3H, OH,...)
Phản ứng cộng HA vào anken không đối xứng tuân theo Quy tắc Mac – cop –nhi – côp: “ nguyên tử H ưu tiên cộng vào nguyên tử cacbon bậc thấp hơn ở nối kép , A ưu tiên cộng vào nguyên tử cacbon bậc cao hơn”
b) Trùng hợp
Quá trình kết hợp liên tiếp nhiều phân tử nhỏ giống nhau hoặc tương tự nhau (gọi là monome) tạo thành những phân tử rất lớn (gọi là polime). Số lượng mắt xích monome trong phân tử polime gọi là hệ số trùng hợp, kí hiệu là n.
c) Phản ứng oxi hóa
Anken cháy hoàn toàn tạo thành CO2 và H2O và tỏa nhiều nhiệt.
Anken làm mất màu dung dịch KMnO4 (phản ứng được dùng để nhận ra sự có mặt của liên kết đôi) và bị oxi hóa không hoàn toàn thành hợp chất điol.
4. Điều chế
Trong phòng TN, etilen được điều chế từ ancol etylic
Trong công nghiệp, các anken được điều chế từ ankan
5. Ứng dụng
Là nguyên liệu quan trọng cho nhiều quá trình sản xuất hóa học. Nhiều anken được dùng làm chất đầu để tổng hợp các polime có nhiều ứng dụng trong đời sống và công nghiệp
B. Giải bài tập Hóa 11 Bài 29
Bài 1 trang 132 SGK Hóa 11
So sánh anken với ankan về đặc điểm cấu tạo và tính chất hóa học. Cho thí dụ minh họa.
Đáp án hướng dẫn giải chi tiết
Khác với ankan là phân tử chỉ chứa liên kết σ, phân tử anken có chứa 1 liên kết π kém bền, dễ gẫy, do đó không giống với ankan là cho phản ứng thế là phản ứng đặc trưng, anken cho phản ứng cộng là phản ứng đặc trưng,
Ví dụ:
C2H4 + H2 ![]() \(\overset{xt Ni}{\rightarrow}\) C2H6
\(\overset{xt Ni}{\rightarrow}\) C2H6
C2H4 + Br2 → C2H4Br2
C2H4 + HBr→C2H5Br
Ngoài ra anken còn cho phản ứng trùng hợp phản ứng làm mất màu dung dịch thuốc tím.
Ví dụ:
3C2H4 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2MnO2 + 2KOH
nCH2 = CH2 ![]() \(\overset{xt, t^{\circ } , p}{\rightarrow}\) (CH2 - CH2)n
\(\overset{xt, t^{\circ } , p}{\rightarrow}\) (CH2 - CH2)n
Bài 2 trang 132 SGK Hóa 11
Ứng với công thức C5H10 có bao nhiêu đồng phân cấu tạo?
A. 4
B. 5
C. 3
D. 7
Đáp án hướng dẫn giải chi tiết
Đáp án B
Anken có các loại đồng phân:
Đồng phân về mạch C:
mạch không phân nhánh
mạch nhánh
Đồng phân về vị trí liên kết đôi
Đồng phân cis - trans
Các công thức cấu tạo:
=> có 5 công thức
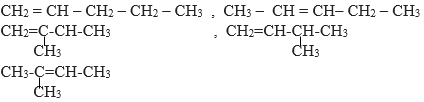
Bài 3 trang 132 SGK Hóa 11
Viết phương trình hóa học của phản ứng xảy ra khi:
a. Propilen tác dụng với hidro, đun nóng (xúc tác Ni).
b. But-2-en tác dụng với hirdo clorua.
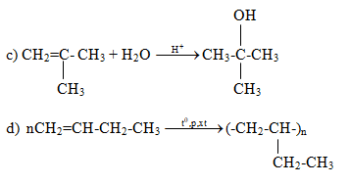
c. Metylpropen tác dụng với nước có xúc tác axit.
d. Trùng hợp but-1-en.
Đáp án hướng dẫn giải
a) CH2 = CH - CH3 + H2 ![]() \(\overset{Ni, t^{\circ } }{\rightarrow}\) CH3 - CH2 - CH3
\(\overset{Ni, t^{\circ } }{\rightarrow}\) CH3 - CH2 - CH3
b) CH3 - CH = CH - CH3 + HCl → CH3 - CH2 - CHCl - CH3
Bài 4 trang 132 SGK Hóa 11
Trình bày phương pháp hóa học để:
a. Phân biệt metan và etilen.
b. Tách lấy khí metan từ hỗn hợp etilen.
c. Phân biệt hai bình không dán nhãn đựng hexan và hex-1-en.
Viết phương trình hoá học của phản ứng đã dùng.
Đáp án hướng dẫn giải chi tiết
a. Lần lượt cho metan và etilen đi qua dung dịch nước brom, chất nào làm dung dịch nước brom nhật màu thì đó là etilen, chất nào không làm dung dịch nước brom nhạt màu thì đó là metan.
CH2=CH2 + Br2 → CH2Br-CH2Br
Br2 (dd nâu đỏ); CH2Br-CH2Br (không màu)
CH4 không tác dụng với dung dịch nước brom
b. Cho hỗn hợp khí (CH4 và C2H4) đi qua dung dịch nước brom dư, C2H4 sẽ tác dụng với dung dịch nước brom, khí còn lại ra khỏi bình dung dịch nước brom là CH4.(PTHH như câu a).
c. Tương tự câu a
Phương trình hóa học
CH2=CH-[CH2]3-CH3 + Br2 → CH2Br-CHBr-[CH2]3-CH3
Br2(dd nâu đỏ); CH2Br-CHBr-[CH2]3-CH3(không màu)
Hexan không tác dụng với dung dịch nước brom
Bài 5 trang 132 SGK Hóa 11
Chất nào sau đây làm mất màu dung dịch brom?
A. Butan
B. but-1-en
C. cacbon đioxi
D. metylpropan
Đáp án hướng dẫn giải chi tiết
Đáp án B
Phương trình hóa học
CH2=CH-CH2-CH3 + Br2 → CH2Br-CHBr-CH2-CH3
Br2(dd nâu đỏ); CH2Br-CHBr-CH2-CH3 (không màu)
Bài 6 trang 132 SGK Hóa 11
Dẫn từ từ 3,36 lít hỗn hợp gồm etilen và propilen (đktc) vào dung dịch brom thấy dung dịch bị nhạt màu và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tăng 4,90gam.
a. Viết các phương trình hóa học và giải thích các hiện tượng ở thí nghiệm trên.
b. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu.
Đáp án hướng dẫn giải
a. Phương trình hóa học:
CH2 = CH2 + Br2 → CH2Br -CH2Br
dd nâu đỏ → không màu
CH2 - CH - CH3 + Br2 → CH2Br-CHBr-CH3
dd nâu đỏ → không màu
b. Gọi số mol của etilen và propilen lần lượt là x và y mol.
Khối lượng dung dịch sau phản ứng tăng lên chính là khối lượng của hỗn hợp etilen và propilen.
Ta có hệ phương trình:
 \(\left\{ \begin{array}{l}
{n_{hh}} = x + y = \frac{{3,36}}{{22,4}} = 0,15\\
{m_{hh}} = 28x + 42y = 4,90
\end{array} \right. = > \left\{ \begin{array}{l}
x = 0,1mol\\
y = 0,05mol
\end{array} \right.\)
\(\left\{ \begin{array}{l}
{n_{hh}} = x + y = \frac{{3,36}}{{22,4}} = 0,15\\
{m_{hh}} = 28x + 42y = 4,90
\end{array} \right. = > \left\{ \begin{array}{l}
x = 0,1mol\\
y = 0,05mol
\end{array} \right.\)
Vậy phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu là:
%VC2H4 = nC2H4 = 0,1/0,15.100% = 66,67%
%VC3H6 = 100% - 66,67% = 33,33%
>> Mời các bạn tham khảo thêm giải Hóa 11 bài tiếp theo tại: Giải bài tập Hóa 11 bài 30: Ankađien
C. Trắc nghiệm Hóa 11 bài 20 Anken
Câu 1: Chất X có công thức CH3 – CH(CH3) – CH = CH2. Tên thay thế của X là
A. 2-metylbut-3-en
B. 3-metylbut-1-in.
C. 3-metylbut-1-en
D. 2-metylbut-3-in
Câu 2: Chất nào sau đây có đồng phân hình học?
A. but- 1- en
B. but- 2- en.
C. 1, 2- dicloetan
D. 2- clopropen
Câu 3: Chất nào sau đây có đồng phân hình học?
A. CH2 = CH – CH2 – CH3
B. CH3 – CH – C(CH3)2.
C. CH3 – CH = CH – CH2 – CH3
D. (CH3)2 – CH – CH = CH2
Câu 4: Ứng với công thức phân tử C4H8 có bao nhiêu đồng phân cấu tạo mạch hở?
A. 2
B. 4
C. 3
D. 5
Câu 5: Ứng với công thức phân tử C4H10 có bao nhiêu đồng phân cấu tạo mạch hở?
A. 4
B. 5
C. 6
D. 3
Câu 6: Số liên kết σ có trong một phân tử But -1-en là
A. 13
B. 10
C. 12
D. 11
>> Ngoài các dạng câu hỏi bài tập sách giáo khoa, sách bài tập. Để củng cố kiến thức, cũng như rèn luyện các thao tác kĩ năng giải bài tâp. VnDoc đã tổng hợp biên soạn, bộ câu hỏi trắc nghiệm Hóa 11 bài 29 có đáp án tại:
------------------------------------------
Trên đây VnDoc.com đã giới thiệu tới bạn đọc tài liệu: Giải bài tập Hóa 11 Bài 29: Anken. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Hóa học lớp 10, Giải bài tập Hóa học lớp 11, Thi thpt Quốc gia môn Văn, Thi thpt Quốc gia môn Lịch sử, Thi thpt Quốc gia môn Địa lý, Thi thpt Quốc gia môn Toán, đề thi học kì 1 lớp 11, đề thi học kì 2 lớp 11 mà VnDoc tổng hợp và đăng tải.
Để tiện trao đổi, chia sẻ kinh nghiệm giảng dạy và học tập môn học THPT, VnDoc mời các bạn truy cập nhóm riêng dành cho lớp 11 sau: Nhóm Tài liệu học tập lớp 11 để có thể cập nhật được những tài liệu mới nhất.

