Bài tập Alkane Hay Có đáp án
Đây là tài liệu Cao cấp - Chỉ dành cho Thành viên VnDoc ProPlus.
- Tải tất cả tài liệu lớp 11 (Trừ Giáo án, bài giảng)
- Trắc nghiệm không giới hạn
Bài tập về Alkane
Bài tập Alkane hay có đáp án được biên soạn bám sát chương trình Hóa học THPT, kết hợp hệ thống lý thuyết trọng tâm và bài tập vận dụng giúp học sinh nắm chắc kiến thức về ankan.
Nội dung bài tập được chia thành 4 dạng câu hỏi:
- Trắc nghiệm khách quan nhiều lựa chọn.
- Trắc nghiệm khách quan Đúng – Sai, mỗi câu gồm 4 ý, học sinh xác định đúng hoặc sai cho từng ý.
- Trắc nghiệm khách quan trả lời ngắn, yêu cầu học sinh ghi kết quả theo đề bài.
- Tự luận, rèn kỹ năng trình bày và lập luận hóa học.
Mỗi dạng câu hỏi đều có đáp án và lời giải chi tiết, giúp học sinh tự học hiệu quả, củng cố kiến thức và nâng cao kỹ năng làm bài kiểm tra, thi cử.
A. Tóm tắt kiến thức Lý thuyết Alkane
I. Khái niệm, danh pháp
1. Khái niệm và công thức chung của alkane
Alkane là các hydrocarbon no mạch hở chỉ chứa liên kết đơn C-H và C-C trong phân tử.
Công thức chung của alkane là: CnH2n+2 (n là số nguyên, n ≥ 1)
2. Danh pháp
2.1. Alkane không phân nhánh
Tên theo danh pháp thay thế của alkane mạch không phân nhánh:

Ví dụ: Tên thay thế của một số alkane mạch không nhánh
| Số nguyên tử carbon | Công thức alkane | Phần nền | Tên alkane |
| 1 | CH4 | meth- | meth ane |
| 2 | CH3CH3 | eth- | eth ane |
| 3 | CH3CH2CH3 | prop- | prop ane |
2.2. Alkane mạch nhánh
Gốc alkyl: Phần còn lại sau khi lấy đi một nguyên tử hydrogen từ phân tử alkane (công thức chung của gốc alkyl là CnH2n+1
Tên gốc alkyl:

Ví dụ: methyl CH3-, ethyl (C2H5-), propyl (C3H7-), ...
Alkane mạch nhánh gồm alkane mạch chính kết hợp với một hay nhiều nhánh.
Tên theo danh pháp thay thế của alkane mạch phân nhánh:
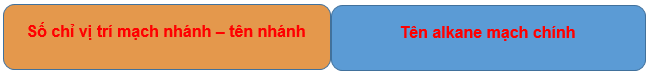
Lưu ý:
Chọn mạch dài nhất, có nhiều nhánh nhất là mạch chính.
Đánh số nguyên tử carbon mạch chính sao cho mạch nhánh có số chỉ vị trí nhỏ nhất.
Dùng chữ số (1, 2, 3, ...) và gạch nối (-) để chỉ vị trí nhánh, nhóm cuối cùng viết liền với tên mạch chính.
Nếu có nhiều nhánh giống nhau: dùng các từ như di-(2), tetra-(4),... để chỉ số lượng nhóm giống nhau, tên nhanh viết theo thứ tự bảng chữ cái.
Ví dụ:
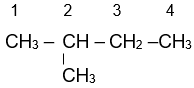
2-methylbutane
III. Tính chất vật lý
Ở điều kiện thường:
- Alkane từ C1 đến C4 và neopentane ở trang thái khí,
- Alkane từ C5 đến C17 (trừ neopentane) ở trạng thái lỏng, không màu, alkane
- Alkane từ C18 trở lên là chất rắn màu trắng (còn gọi là sáp parafin).
Các alkane mạch nhánh thường có nhiệt độ sôi thấp hơn so với đồng phân alkane mach không phân nhánh. Alkane không tan hoặc tan rất ít trong nước và nhẹ hơn nước, tan tốt hơn trong các dung môi hữu cơ.
III. Tính chất hoá học
1. Phản ứng thế
Phản ứng halogen hóa alkane là phản ứng xảy ra khi đặt bình chứa hỗn hợp của alkane với halogen ở nơi có ánh sáng hoặc ở nhiệt độ cao (đun nóng). Sản phẩm của phản ứng halogen hóa là các dẫn xuất halogen.
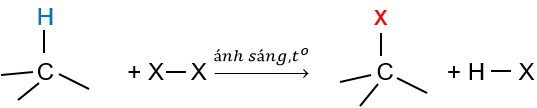
X (Cl, Br)
Phản ứng thế có thể tiếp tục diễn ra với các nguyên tử hydrogen chloromethane cho hỗn hợp các sản phẩm chloromethane, dichloromethane, trichloromethane và tetrachloromethane.
Ví dụ: Trộn methane với chlorine và chiếu ánh sáng tử ngoại, sản phẩm thu được là chloromethane.
CH4 + Cl2 ![]() CH3Cl + HCl
CH3Cl + HCl
Chloromethane
CH3Cl + Cl2 ![]() CH2Cl2 + HCl
CH2Cl2 + HCl
dichloromethane
CH2Cl2 + Cl2 ![]() CHCl3 + HCl
CHCl3 + HCl
trichloromethane
CHCl3 + Cl2 ![]() CCl4 + HCl
CCl4 + HCl
tetrachloromethane
Khi thực hiện phản ứng thế halogen vào các alkane có từ 3 nguyên tử carbon trở lên sẽ thu được hỗn hợp các sản phẩm thế monohalogen.
Ví dụ:
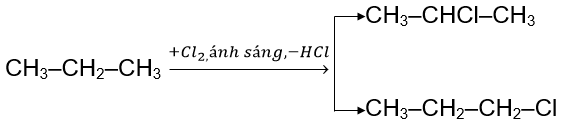
2. Phản ứng cracking
Cracking alkane là quá trình phân cắt liên kết C-C (bẻ gẫy mạch carbon) của các alkane mạch dài để tạo thành hỗn hợp các hydrocarbon có mạch carbon ngắn hơn.
Phản ứng được ứng dụng trong công nghiệp lọc dầu.
Ví dụ:
CH3-CH2-CH3 ![]() CH2=CH2 + CH4
CH2=CH2 + CH4
Tổng quát:
CnH2n+2 ![]() CaH2a+2 + CbH2b
CaH2a+2 + CbH2b
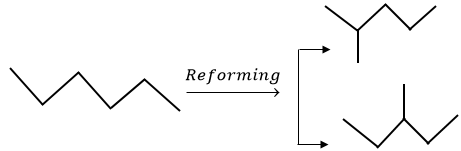
3. Phản ứng reforming
Reforming alkane là quá trình chuyển các alkane mạch không phân nhánh thành các alkane mạch phân nhánh và các hydrocarbon mạch vòng nhưng không làm thay đổi.
Ví dụ:
4. Phản ứng oxi hoá
4.1. Phản ứng oxi hoá hoàn toàn (phản ứng cháy)
Khi tiếp xúc với oxygen và có tin lớn khơi mào, alkane bị đốt cháy trở thành khí carbon dioxide, hai nước và giải phóng năng lượng.
Tổng quát:
![]()
Ví dụ:
CH4 + 2O2 ![]() CO2 + 2H2O
CO2 + 2H2O
C2H6 + 7/2O2 ![]() 2CO2 + 3H2O
2CO2 + 3H2O
4.2. Phản ứng oxi hoá không hoàn toàn
Ở nhiệt độ cao, có mặt xúc tác, alkane bị oxi hoá cắt mạch carbon bởi oxygen tạo thành hỗn hợp carboxylic acid.
RCH2-CH2R' + ![]() O2
O2 ![]() RCOOH + R'COOH + H2O
RCOOH + R'COOH + H2O
B. Câu hỏi bài tập trắc nghiệm AlKane
➡️ Chi tiết toàn bộ tài liệu nằm trong FILE TẢI VỀ
...................................................