Công thức của ancol etylic, axeton
Công thức của ancol etylic, axeton
Bài viết sau đây sẽ hướng dẫn các em viết công thức của ancol etylic, axeton một cách đơn giản và nhanh chóng, từ đó tiết kiệm thời gian khi gặp dạng bài này trong đề thi đại học. Mời các em cùng tham khảo.
- Amino axit là gì? - Đầy đủ kiến thức từ A-Z để ôn thi THPT QG 2020
- Axit amino glutaric là gì?
- Bài tập tổng hợp Ancol - Phenol
- Bài tập môn Hóa học lớp 12: Đồng phân và danh pháp của ancol và phenol
Ancol, xeton đều thuộc nhóm dẫn xuất hidrocacbon. Ancol etylic và axeton là 2 hợp chất đại diện có tính chất đặc trưng, khá thông dụng trong khoa học cũng như trong cuộc sống. Ancol etylic dùng pha chế các loại rượu, làm nhiên liệu cho động cơ, đèn cồn phòng thí nghiệm. Axeton dùng làm chất tẩy rửa các dụng cụ thí nghiệm, tẩy sơn móng tay, làm dung môi cho các phản ứng hữu cơ. Vậy chúng có công thức như thế nào?
- Ancol etylic có CTCT là C2H5OH, là chất lỏng không màu, không mùi.
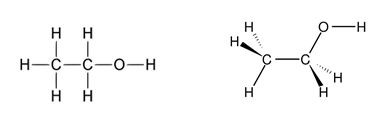
Trong không gian, các nguyên tử H không bị che lấp mà nằm xen kẽ nhau. Các liên kết xung quanh nguyên tử C đều là liên kết đơn, nên nguyên tử C ở dạng lai hóa sp3 có cấu tạo tứ diện. Các liên kết ở dạng này rất bền, khó bị bẻ gãy. Đồng thời độ âm điện của nguyên tử C và H không chênh lệch nhiều nên liên kết càng bền.
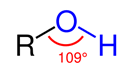
Điểm chú ý là liên kết C-O-H. Góc liên kết của chúng là 1090, là 1 trường hợp thiếu hụt của lai hóa sp3. Đồng thời, O có độ âm điện lớn dẫn tới sự chênh lệch độ âm điện giữa O và H nên nguyên tử H gắn với C rất linh động, dễ dàng tham gia các phản ứng thế. Vậy nên phản ứng đặc trung của ancol etylic cũng như các ancol khác đó là phản ứng thế.
Rượu etylic (ancol etylic) trong cuộc sống được “nấu” từ cơm, dùng men rượu làm xúc tác. Rượu này có mùi thơm nồng, vị cay. Khi uống gây cảm giác rát cổ họng.
- Axeton có CTCT là CH3COCH3, là chất lỏng không màu, dễ bay hơi.
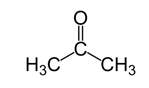
Điểm khác biệt trong công thức cấu tạo của axeton đó là liên kết C=O. Với cấu tạo đặc biệt này, phản ứng đặc trưng của axeton đó là phản ứng cộng. Liên kết đôi C=O gồm 1 liên kết s bền vững và liên kết p kém bền. Tất nhiên là liên kết p kém bền dễ bị bẽ gãy.
Trên đây, VnDoc.com đã giới thiệu tài liệu Hóa học 12: Công thức của ancol etylic, axeton, mời các bạn tham khảo thêm các tài liệu ôn thi THPT Quốc gia môn Hóa khác nhằm đạt kết quả cao trong kì thi THPT Quốc gia sắp tới.