Bài 28 Hóa 11: Bài thực hành số 3 Phân tích định tính nguyên tố và Điều chế và tính chất của metan
Bài thực hành số 3 Phân tích định tính nguyên tố và Điều chế và tính chất của metan
Bài 28 Hóa 11: Bài thực hành số 3 Phân tích định tính nguyên tố và Điều chế và tính chất của metan được VnDoc biên soạn hướng dẫn các bạn biết cách thực hiện các thao tác thí nghiệm trong bài thực hành cũng như viết kết quả báo cáo thí nghiệm bài thực hành số 3. Mời các bạn tham khảo.
>> Mời các bạn tham khảo một số nội dung tài liệu liên quan đến bài thực hành số 3 hóa 11
- Giải Hóa 11 bài 28: Bài thực hành số 3 Phân tích định tính nguyên tố. Điều chế và tính chất của metan
- Bản tường trình hóa học 11 Bài thực hành 3'
- Giải bài tập Hóa 11 Bài 29: Anken
I. Nội dung thí nghiệm và cách tiến hành
Thí nghiệm 1: Xác định định tính cacbon và hidro
Dụng cụ, hóa chất:
Dụng cụ: ống nghiệm, bộ giá thí nghiệm, đèn cồn, chậu thủy tinh, thìa lấy hóa chất, công tơ hút, giá để ống nghiệm, bông, nút cao su, ống dẫn khí,…
Hóa chất: đường saccrozo (C12H22O11), CuO, CuSO4 khan, nước vôi trong (Ca(OH)2)
Cách tiến hành:
Trộn đều khoảng 0,2 gam saccarozo với 1-2 g CuO sau đó cho hỗn hợp vào ống nghiệm.
Cho tiếp 1g CuO phủ hết bề mặt hỗn hợp trong ống nghiệm, lấy cục bông tẩm bột CuSO4 khan trắng để sát miệng ống nghiệm.
Dẫn khí thoát ra vào nước vôi trong, tiến hành lắp dụng cụ như hình vẽ: Đun ống nghiệm có chứa hỗn hợp chất rắn.
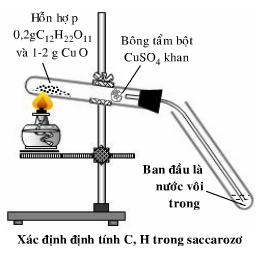
Quan sát hiện tượng.
Hiện tượng, giải thích:
Ta thấy nhúm bông chuyển dần sang màu xanh lam của muối đồng và dung dịch nước vôi trong xuất hiện vẩn đục.
Do CuO oxi hóa đường tạo thành CO2 và hơi nước. Hơi nước bay lên gặp miếng bông có chứa CuSO4 khan, gặp nước tạo thành màu xanh.
CO2 thoát ra ngoài tác dụng với nước vôi trong tạo kết tủa CaCO3
CO2 + Ca(OH)2 → CaCO3 + H2O
Thí nghiệm 2: Điều chế và thử tính chất của CH4
Dụng cụ, hóa chất:
Dụng cụ: ống nghiệm, bộ giá thí nghiệm, que đóm, chậu thủy tinh, thìa lấy hóa chất, công tơ hút, giá để ống nghiệm, bông, nút cao su, ống dẫn khí, ống vuốt nhọn…
Hóa chất: dung dịch brom, thuốc tím, natri axetat khan và vôi tôi xút,…
Cách tiến hành:
Cho vào ống nghiệm khô có nút và ống dẫn khí khoảng 4-5g hỗn hợp bột mịn đã được trộn đều gồm natri axetat khan và vôi tôi xút theo tỉ lệ 1 : 2 về khối lượng.
Lắp dụng cụ như hình 5.2. Đun nóng đáy ống nghiệm bằng ngọn lửa đèn cồn.
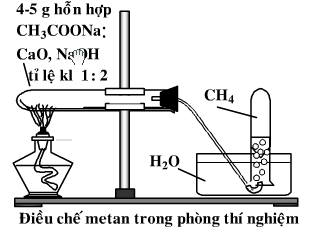
Thay ống dẫn khí bằng ống vuốt nhọn, rồi đốt khí thoát ra ở đầu ống dẫn khí. Quan sát màu ngọn lửa.

Dẫn dòng khí lần lượt vào các ống nghiệm đựng dung dịch brom hoặc dung dịch thuốc tím.
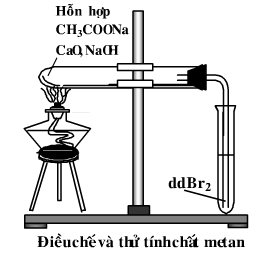
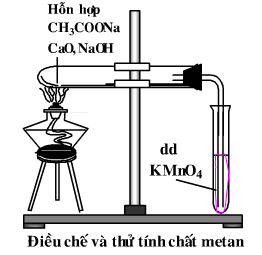
Hiện tượng, giải thích:
Khi điều chế khí CH4: Ta thấy bọt khí xuất hiện và cột nước trong uống nghiệm thu khí hạ dần xuống:
CH3COONa + NaOH ![]() \(\overset{t^{\circ } }{\rightarrow}\) CH4 + Na2CO3
\(\overset{t^{\circ } }{\rightarrow}\) CH4 + Na2CO3
Đốt cháy khí CH4: ta thấy ngọn lửa có màu xanh.
CH4 + 2O2 ![]() \(\overset{t^{\circ } }{\rightarrow}\) CO2 + 2H2O
\(\overset{t^{\circ } }{\rightarrow}\) CO2 + 2H2O
Dẫn dòng khí qua dung dịch thuốc tím (KMnO4) hay dung dịch brom: không có hiện tưởng gì, do CH4 là ankan nên không có phản ứng cộng với brom hay phản ứng oxi hóa với KMnO4
II. Viết tường trình bài thực hành 3 hóa 11
| Tên thí nghiệm | Dụng cụ hóa chất | Cách tiến hành | Hiện tượng | Phương trình |
| Thí nghiệm 1: Xác định định tính cacbon và hidro | ||||
| Thí nghiệm 2: Điều chế và thử tính chất của CH4 |
>> Nội dung chi tiết bản tưởng trình hóa học 11 bài thực hành số 3 được VnDoc trình bày chi tiết tại: Bản tường trình hóa học 11 Bài thực hành 3
III. Nhắc lại kiến thức nội dung Điều chế và tính chất của metan
Phản ứng đặc trưng của Metan
Các tính chất hóa học của metan quan trọng mà các bạn cần nhớ là phản ứng thế với halogen như clo, brom. Nó phản ứng với hơi nước và tạo ra khí hidro, khí metan tác dụng với oxi gây cháy và phản ứng phân hủy metan ra axetilen C2H2.
Phản ứng của metan thế H bằng halogen khi có ánh sáng
Khi có ánh sáng hoặc nhiệt độ, thì halogen có thể thế lần lượt từng phân tử H trong phân tử metan tạo thành dẫn xuất metyl halogen
CH3-H + X2 →hv/to CH3-X+ HX
Phản ứng có thể tiếp tục xảy ra để tạo sản phẩm di-, tri-, tetra halogen
Ví dụ: metan tác dụng brom
Br2 + CH4 → CH3Br + HBr
Clo hóa CH4 ở điều kiện ánh sáng có thể thu được CH3Cl, CH2Cl2, CHCl3, CCl4
Khả năng phản ứng của dãy halogen theo thứ tự F2 > Cl2 > Br2 > I2
Cách điều chế metan trong phòng thí nghiệm
Một số cách điều chế CH4 trong phòng thí nghiệm như sau:
Khi cần một lượng nhỏ metan, người ta nung natri axetat chung với vôi tôi xút, hoặc điều chế metan bằng cách cho nhôm cacbua tác dụng với nước:
Điều chế CH4 từ nhôm cacbua:
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
Phản ứng muối natri axetat với xút tạo khí metan (nhiệt phân muối natri của axit carboxylic):
CH3–COONa + NaOH ![]() \(\overset{CaO, to}{\rightarrow}\) Na2CO3 + CH4
\(\overset{CaO, to}{\rightarrow}\) Na2CO3 + CH4
.................................
Trên đây VnDoc đã giới thiệu tới các bạn Bài 28 Hóa 11: Bài thực hành số 3 Phân tích định tính nguyên tố và Điều chế và tính chất của metan. Để có thể nâng cao kết quả trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán 11, Chuyên đề Hóa học 11, Giải bài tập Hoá học 11. Tài liệu học tập lớp 11 mà VnDoc tổng hợp và đăng tải.
Để tiện trao đổi, chia sẻ kinh nghiệm giảng dạy và học tập môn học THPT, VnDoc mời các bạn truy cập nhóm riêng dành cho lớp 11 sau: Nhóm Tài liệu học tập lớp 11 để có thể cập nhật được những tài liệu mới nhất.
