Giải bài tập Hóa 11 Bài 33 : Luyện tập Ankin
Giải bài tập Hóa học 11: Luyện tập Ankin
VnDoc xin giới thiệu tới bạn đọc bộ tài liệu Giải bài tập Hóa học 11 Bài 33: Luyện tập Ankin, chắc chắn bộ tài liệu sẽ là nguồn thông tin hữu ích để giúp các bạn học sinh có kết quả cao hơn trong học tập. Mời thầy cô c ùng các bạn học sinh tham khảo.
Bài 1 trang 147 SGK hóa 11
Dẫn hỗn hợp khí gồm metan, etilen, axetilen đi qua dung dịch bạc nitrat trong dung dịch manoniac. Khí còn lại được dẫn vào dung dịch brom (dư). Nêu và giải thích các hiện tượng xảy ra trong thí nghiệm.
Đáp án hướng dẫn giải
Khi dẫn dòng khí từ từ đi vào dung dịch AgNO3/NH3 thì axetilen tác dụng với AgNO3/NH3 sinh ra kết tủa màu vàng nhạt:
CH≡CH + 2AgNO3 + 2NH3 → AgC≡CAg↓ +2NH4NO3
Hỗn hợp khí còn lại dẫn vào dung dịch nước brom thì etilen sẽ tác dụng với dung dịch nước brom, làm cho dung dịch nhạt màu:
CH2=CH2 + Br2 → CH2Br-CH2Br
(Dung dịch Br2 Dd nâu đỏ → Dung dịch CH2Br-CH2Br không màu)
Còn metan không có phản ứng nào.
Bài 2 trang 147 SGK Hóa 11
Viết phương trình phản ứng hoá học của phản ứng thực hiện sơ đồ chuyển hoá sau:
CH4 ![]() \(\overset{(1)}{\rightarrow}\) C2H2
\(\overset{(1)}{\rightarrow}\) C2H2 ![]() \(\overset{(2)}{\rightarrow}\) C4H4
\(\overset{(2)}{\rightarrow}\) C4H4 ![]() \(\overset{(3)}{\rightarrow}\) C4H6
\(\overset{(3)}{\rightarrow}\) C4H6 ![]() \(\overset{(4)}{\rightarrow}\) cao su buna
\(\overset{(4)}{\rightarrow}\) cao su buna
(polibutađien hay còn gọi là cao su buna)
Đáp án hướng dẫn giải
Phương trình phản ứng:
2CH4 ![]() \(\xrightarrow[1500^{\circ } C]{lamlanh nhanh}\) C2H2 + 3H2
\(\xrightarrow[1500^{\circ } C]{lamlanh nhanh}\) C2H2 + 3H2
2C2H2 ![]() \(\overset{NH_{4} Cl, CuCl_{2} }{\rightarrow}\)CH ≡ C - CH = CH2
\(\overset{NH_{4} Cl, CuCl_{2} }{\rightarrow}\)CH ≡ C - CH = CH2
CH ≡ C - CH = CH2 + H2 ![]() \(\overset{Pb,t^{\circ } }{\rightarrow}\) CH2 = CH - CH = CH2
\(\overset{Pb,t^{\circ } }{\rightarrow}\) CH2 = CH - CH = CH2
nCH2 = CH - CH = CH2 ![]() \(\overset{Na, t^{\circ } }{\rightarrow}\) (CH2 - CH = CH - CH2)n (Cao su buna)
\(\overset{Na, t^{\circ } }{\rightarrow}\) (CH2 - CH = CH - CH2)n (Cao su buna)
Bài 3 trang 147 SGK Hóa 11
Viết phương trình hoá học của các phản ứng từ axetilen và các chất vô cơ cần thiết điều chế các chất sau:
a. 1,2-đicloetan
b. 1,2-đibrometan
c. 1,1,2-tribrometan
d. 1,1-đicloetan
e. Buta-1,3-đien
Đáp án hướng dẫn giải
a. 1,2-đicloetan
CH≡CH + H2 ![]() \(\overset{Pd,PdCO_{3} ,t^{\circ } }{\rightarrow}\) CH2 = CH2
\(\overset{Pd,PdCO_{3} ,t^{\circ } }{\rightarrow}\) CH2 = CH2
CH2=CH2 + Cl2 → CH2Cl-CH2Cl
b. 1,1-đicloetan
CH≡CH + HCl ![]() \(\overset{t^{\circ } }{\rightarrow}\) CH2=CHCl
\(\overset{t^{\circ } }{\rightarrow}\) CH2=CHCl
CH2=CHCl + HCl ![]() \(\overset{t^{\circ },xt }{\rightarrow}\) CH3-CHCl2
\(\overset{t^{\circ },xt }{\rightarrow}\) CH3-CHCl2
c. 1,2-đbrometen
CH≡CH + Br2 → CHBr = CHBr
d. Buta-1,3-đien
2C2H2 ![]() \(\overset{NH_{4} Cl, CuCl_{2} }{\rightarrow}\) CH≡C-CH=CH2
\(\overset{NH_{4} Cl, CuCl_{2} }{\rightarrow}\) CH≡C-CH=CH2
CH≡C-CH=CH2 + H2 ![]() \(\overset{Pd, PdCO_{3} ,t^{\circ } }{\rightarrow}\) CH2=CH-CH=CH2
\(\overset{Pd, PdCO_{3} ,t^{\circ } }{\rightarrow}\) CH2=CH-CH=CH2
e. 1,1,2-tribrometan
CH ≡ CH + Br2 → CHBr = CHBr
CHBr = CHBr + HBr → CH2Br - CHBr2
Bài 4 trang 147 SGK Hóa 11
Khi thực hiện phản ứng nhiệt phân metan điều chế axetilen thu được hỗn hợp X gồm axetilen, hiđro và metan chưa phản ứng hết. Tỉ khối của X so với H2 bằng 4,44. Tính hiệu suất của phản ứng.
Đáp án hướng dẫn giải
Ta có: dhỗn hợp/H2 = 4,44 => Mhỗn hợp = 4,44.2 = 8,88
Gọi nCH4 ban đầu là 1
2CH4 ![]() \(\xrightarrow[1500^{\circ } C]{làm lạnh nhanh}\) C2H2 + H2
\(\xrightarrow[1500^{\circ } C]{làm lạnh nhanh}\) C2H2 + H2
nban đầu 1 0 0 (mol)
n phản ứng 2x x 3x (mol)
n sau phản ứng 1-2x x 3x (mol)
Tổng số mol khí sau phản ứng: 1 - 2x + x + 3x = 1 + 2x (mol)
Ta có phương trình:
![]() \(\frac{(1-2x).16+26.x+2.3x}{1+2x} =8,88=>x=0,4\)
\(\frac{(1-2x).16+26.x+2.3x}{1+2x} =8,88=>x=0,4\)
Vậy hiệu suất phản ứng = 0,4/1.100% = 40%
Bài 5 trang 147 SGK Hóa 11
Dẫn 6,72 lit hỗn hợp khí X gồm propan, etilen và axetilen đi qua dung dịch brom dư, thấy còn 1,68 lít khí không hấp thụ. Nếu dẫn 6,72 lit hỗn hợp khí X trên qua dung dịch AgNO3/NH3 thấy có 24,24 gam kết tủa. Các thể tích khí đo ở đktc.
a. Viết các phương trình hoá học giải thích các thí nghiệm trên.
b. Tính thành phần phần trăm theo thể tích và theo khối lượng của mỗi khí trong hỗn hợp.
Đáp án hướng dẫn giải
a) CH2=CH2 + Br2 → CH2Br-CH2Br
CH≡CH + Br2 → CHBr2-CHBr2
CH≡CH + 2AgNO3 + 2NH3 → AgC≡CAg↓vàng + 2NH4NO3
Khí không bị hấp thụ (hay không có phản ứng) là khí propan (C3H8)
b)
npropan = 1,68/22,4 = 0,075 (mol)
Ta có:
nAg2C2 = 2424/240 = 0,101 (mol)
nX = 6,72/22,4 = 0,3 (mol)
=> nC2H2 = 0,101 (mol)
nX = 6,72/22,4 = 0,3 (mol)
=> 0,3 - (0,075 + 0,101) = 0,124 (mol)
Thành phần phần trăm các khí theo thể tích trong hỗn hợp là:
=> %VC3H8 = %nC3H8 = 0,075/0,3.100% = 25%
%VC2H2 = %nC2H2 = 0,101/0,3.100% = 33,7%
=> %VC2H4 = 41,7%
Tổng khối lượng khí là:
mX = mC3H8 + mC2H4 + mC2H2 = 0,075.44 + 0,124.28 + 0,101.26 = 9,398(g)
Thành phần phần trăm các khí theo khối lượng là:
 \(\begin{array}{l}
= > \% {m_{{C_3}{H_8}}} = \frac{{{m_{{C_3}{H_8}}}}}{{{m_X}}}.100\% = \frac{{0,075.44}}{{9,398}}.100\% = 35,2\% \\
\% {m_{{C_2}{H_4}}} = \frac{{{m_{{C_2}{H_4}}}}}{{{m_X}}}.100\% = \frac{{0,124.28}}{{9,398}}.100\% = 36,9\% \\
= > \% {m_{{C_2}{H_2}}} = 100\% - (35,1\% + 36,9\% ) = 28,0\%
\end{array}\)
\(\begin{array}{l}
= > \% {m_{{C_3}{H_8}}} = \frac{{{m_{{C_3}{H_8}}}}}{{{m_X}}}.100\% = \frac{{0,075.44}}{{9,398}}.100\% = 35,2\% \\
\% {m_{{C_2}{H_4}}} = \frac{{{m_{{C_2}{H_4}}}}}{{{m_X}}}.100\% = \frac{{0,124.28}}{{9,398}}.100\% = 36,9\% \\
= > \% {m_{{C_2}{H_2}}} = 100\% - (35,1\% + 36,9\% ) = 28,0\%
\end{array}\)
Bài 6 trang 147 SGK Hóa 11
Đốt cháy hoàn toàn 2,24 lit hiđrocacbon X thu được 6,72 lit CO2 (đktc) X tác dụng với dung dịch AgNO3/NH3 sinh ra kết tủa Y. Công thức cấu tạo của X là:
A. CH3-CH=CH2
B. CH≡CH
C. CH3-C≡CH
D. CH2=CH-C≡CH
Đáp án hướng dẫn giải
Đáp án C
nX = 2,24/22,4 = 0,1 (mol); nCO2 = 6,72/22,4 = 0,3 (mol)
Gọi CTPT của X là CxHy
CxHy + (x+y/4)O2 → x CO2 + y/2H2O
Theo phương trình: 1 x (mol)
Theo đầu bài: 0,1 0,3 (mol)
=> x = 3 => C3Hy
Mà X tác dụng với AgNO3/NH3 sinh ra kết tủa Y, nên X là: CH3-C≡CH
=> Đáp án C
Bài 7 trang 147 SGK Hóa 11
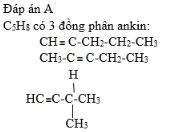
Ứng với công thức phân tử C5H8 có bao nhiêu ankin đồng phân của nhau?
A. 3
B. 4
C. 2
D. 5
Hãy chọn đáp án đúng.
Đáp án hướng dẫn giải
--------------------------------------
Trên đây VnDoc.com đã giới thiệu tới bạn đọc tài liệu: Giải bài tập Hóa 11 Bài 33 : Luyện tập Ankin. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Hóa học lớp 10, Giải bài tập Hóa học lớp 11, Thi thpt Quốc gia môn Văn, Thi thpt Quốc gia môn Lịch sử, Thi thpt Quốc gia môn Địa lý, Thi thpt Quốc gia môn Toán, đề thi học kì 1 lớp 11, đề thi học kì 2 lớp 11 mà VnDoc tổng hợp và đăng tải.
Để tiện trao đổi, chia sẻ kinh nghiệm giảng dạy và học tập môn học THPT, VnDoc mời các bạn truy cập nhóm riêng dành cho lớp 11 sau: Nhóm Tài liệu học tập lớp 11 để có thể cập nhật được những tài liệu mới nhất.
