Giải bài tập Hóa 11 bài 9: Axit nitric và muối nitrat
Giải bài tập hóa lớp 11 bài 9
Giải bài tập Hóa 11 bài 9: Axit nitric và muối nitrat. Tài liệu giúp bạn nắm được kiến thức cơ bản của bài Hóa 11 bài 9 thông qua việc nhắc lại những kiến thức cơ bản đồng thời hướng dẫn bạn vận dụng những kiến thức đã học đó vào việc giải các bài tập hóa 11 bài 9 sách giáo khoa. Mời các bạn tham khảo.
A. Tóm Hóa 11 bài 9: Axit nitric và muối nitrat
I. Axit nitric (HNO3, M = 63)
1. Tính chất vật lý
Axit nitric tinh khiết là chất lỏng không màu, bốc khói mạnh trong không khí ẩm. Axit HNO3 tan tốt trong nước theo bất kì tỉ lệ nào.
Axit nitric kém bền. Trong điều kiện thường, có ánh sáng, dung dịch axit đặc bị phân hủy 1 phần giải phóng khí nito dioxit, khí này lại tan trong dung dịch axit làm cho dung dịch có màu vàng => Bảo quản dung dịch HNO3 trong bình tối màu
2. Tính chất hóa học:
a. Axit HNO3 là một trong các axit mạnh:
- Làm quỳ tím hóa đỏ,
- Tác dụng với bazơ và oxit bazơ,
- Tác dụng với muối của axit yếu.
- Tác dụng với kim loại (không giải phóng khí H2)
VD: Fe2O3 + 2HNO3 → Fe2(NO3)3 + H2O
Ca(OH)2 + 2HNO3 → Ca(NO3)2 + 2H2O
BaCO3 + 2HNO3 → Ba(NO3)2 + CO2 + H2O
b. Axit HNO3 là chất oxi hóa mạnh (vì N có số oxi hóa là +5)
- Phản ứng với hầu hết các kim loại trừ Pt và Au:
 \(M + HN{O_3} \to M{(N{O_3})_n} + \left[ \begin{array}{l}
N{O_2}\\
NO\\
{N_2}\\
N{H_4}N{O_3}
\end{array} \right. + {H_2}O\)
\(M + HN{O_3} \to M{(N{O_3})_n} + \left[ \begin{array}{l}
N{O_2}\\
NO\\
{N_2}\\
N{H_4}N{O_3}
\end{array} \right. + {H_2}O\)- Một số phi kim, nhiều hợp chất vô cơ và hữu cơ.
(Một số hợp chất hữu cơ bốc cháy khi gặp HNO3 đặc)
Thí dụ:
C + 4HNO3 (đ) ![]() \(\overset{t^{\circ } }{\rightarrow}\) CO2 + 4NO2 + 2H2O
\(\overset{t^{\circ } }{\rightarrow}\) CO2 + 4NO2 + 2H2O
3. Điều chế axit nitric
a. Trong phòng thí nghiệm
Axit HNO3 được điều chế bằng cách cho NaNO3 hoặc KNO3 tác dụng với axit H2SO4 đặc, nóng:
b. Trong công nghiệp
Được sản xuất theo sơ đồ sau
N2 ![]() \(\overset{+H_{2} , xt, t^{\circ },p }{\rightarrow}\) NH3
\(\overset{+H_{2} , xt, t^{\circ },p }{\rightarrow}\) NH3 ![]() \(\xrightarrow[t^{\circ }, xt ]{+O_{2} }\) NO
\(\xrightarrow[t^{\circ }, xt ]{+O_{2} }\) NO ![]() \(\overset{+O_{2} }{\rightarrow}\) NO2
\(\overset{+O_{2} }{\rightarrow}\) NO2 ![]() \(\overset{+O_{2}+H_{2} O }{\rightarrow}\) HNO3
\(\overset{+O_{2}+H_{2} O }{\rightarrow}\) HNO3
4. Ứng dụng
Axit nitric là một trong những hóa chất cơ bản và quan trọng. Phần lớn axit này được dùng để sản xuất phân đạm. Ngoài ra nó được dùng để sản xuất thuốc nổ, thuốc nhuộm, dược phẩm.
II. Muối nitrat M(NO3)n
1. Tính chất vật lý
Tất cả các muối nitrat đều tan nhiều trong nước và là chất điện li mạnh.
M(NO3)n → Mn+ + nNO3-
2. Tính chất hóa học
Các muối nitrat kém bền với nhiệt, chúng bị phân hủy khi đun nóng
a. Muối nitrat có các tính chất hóa học chung của muối
- Tác dụng với axit:
AgNO3 + HCl → AgCl + HNO3
- Tác dụng với dung dịch bazo
Mg(NO3)2 + 2NaOH → Mg(OH)2 + 2NaNO3
- Tác dụng với dung dịch muối:
Mg(NO3)2 + Na2CO3 → MgCO3 + 2NaNO3
- Tác dụng với với kim loại
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
b. Muối nitrat dễ bị nhiệt phân
- Muối nitrat của các kim loại hoạt động mạnh đứng trước Mg (kali, natri,…) bị phân hủy thành muối nitrit và oxi
- Muối nitrat của kim loại từ Mg đến Cu bị phân hủy thành oxit kim loại tương ứng, NO2 và O2
- Muối nitrat của kim loại kém hoạt động (Sau Cu) bị phân hủy thành kim loại tương ứng, khí NO2 và O2.
Lưu ý: Một số muối nhiệt phân không theo quy luật trên như Fe(NO3)2, NH4NO3
c. Tính oxi hóa trong môi trường axit
Nếu muối nitrat tồn tại trong môi trường axit có tính oxi hóa mạnh như HNO3
Thí dụ: 3Cu + 8HCl + 2KNO3 → 3CuCl2 + 2KCl + 2NO + 4H2O
B. Giải bài tập trang 45 SGK Hóa học lớp 11
Bài 1 trang 45 SGK Hóa 11
Viết công thức electron, công thức cấu tạo của axit nitric. Cho biết nguyên tố nitơ có hóa trị và số oxi hóa bao nhiêu?
Đáp án hướng dẫn giải bài tập
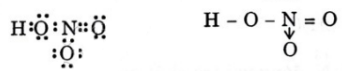
Trong HNO3, nitơ có số oxi hóa +5 và hóa trị là 4
Bài 2 trang 45 SGK Hóa 11
Lập các phương trình hóa học:
a) Ag + HNO3 (đặc) → NO2 + ? + ?
b) Ag + HNO3 (loãng) → NO + ? + ?
c) Al + HNO3 → N2O + ? + ?
d) Zn + HNO3 → NH4NO3 + ? + ?
e) FeO + HNO3 → NO + Fe(NO3)3 + ?
g) Fe3O4 + HNO3 → NO + Fe(NO3)3 + ?
Đáp án hướng dẫn giải bài tập
Trước hết, căn cứ vào tính chất, điền công thức các chất còn thiếu ở chỗ có dấu (?). Sau đó, cân bằng phương trình hóa học theo phương pháp thăng bằng electron, ta được kết quả sau:
a) Ag + 2HNO3 (đặc) → NO2 + AgNO3 + H2O
b) 3Ag + 4HNO3 (loãng) → NO + 3AgNO3 + 2H2O
c) 8Al + 30HNO3 → 3N2O + 8Al(NO3)3 + 15H2O
d) 4Zn + 10HNO3 → NH4NO3 + 4Zn(NO3)2 + 3H2O
e) 3FeO + 10HNO3 → NO + 3Fe(NO3)3 + 5H2O
g) 3Fe3O4 + 28HNO3 → NO + 9Fe(NO3)3 + 14H2O
Bài 3 trang 45 SGK Hóa 11
Hãy chỉ ra những tính chất hóa học chung và khác biệt giữa axit nitric và axit sunfuric. Viết các phương trình hóa học để minh họa.
Đáp án hướng dẫn giải
Axit nitric và axit sunfuric đặc đều có tính oxi hóa mạnh.
Ví dụ:
3FeO + 10HNO3 → 3Fe(NO3)3 + NO ↓ + 5H2O
2FeO + 4H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
Tuy nhiên nếu như HNO3 loãng vẫn có tính oxi hóa thì H2SO4 loãng lại không có tính oxi hóa.
Ví dụ:
3Fe3O4 + 28HNO3 → 9Fe(NO3)3 + NO ↓ + 14H2O
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
Bài 4 trang 45 SGK Hóa 11
a) Trong phương trình hóa học của phản ứng nhiệt phân sắt (III) nitrat, tổng các hệ số bằng bao nhiêu?
A. 5
B. 7
C. 9
D. 21
b) Trong phương trình hóa học của phản ứng nhiệt phân thủy ngân (II) nitrat, tổng các hệ số bằng bao nhiêu?
A. 5
B. 7
C. 9
D. 21
Đáp án hướng dẫn giải
a) Chọn D. 21
4Fe(NO3)3 ![]() \(\overset{t^{\circ } }{\rightarrow}\) 2Fe2O3 + 12NO2 + 3O2
\(\overset{t^{\circ } }{\rightarrow}\) 2Fe2O3 + 12NO2 + 3O2
b) Chọn A. 5
Hg(NO3)3 ![]() \(\overset{t^{\circ } }{\rightarrow}\) Hg + 2NO2 + O2
\(\overset{t^{\circ } }{\rightarrow}\) Hg + 2NO2 + O2
Bài 5 trang 45 SGK Hóa 11
Viết phương trình hóa học của các phản ứng thực hiện dãy chuyển hóa sau đây:
NO2 → HNO3 → Cu(NO3)2 → Cu(OH)2 → Cu(NO3)2 → CuO → Cu → CuCl2
Đáp án hướng dẫn giải
Phương trình hóa học
4NO2 + 2H2O → 4HNO3
CuO + 2HNO2 → Cu(NO3)2 + H2O
Cu(NO3)2 + 2NaOH → Cu(OH)2 ↓ + 2NaNO3
Cu(OH)2 + 2HNO3 → Cu(NO3)2 + 2H2O
Cu(NO3)2 ![]() \(\overset{t^{\circ } }{\rightarrow}\) CuO + 2NO2 ↑ + ½ O2 ↑
\(\overset{t^{\circ } }{\rightarrow}\) CuO + 2NO2 ↑ + ½ O2 ↑
CuO + H2 ![]() \(\overset{t^{\circ } }{\rightarrow}\) Cu + H2O
\(\overset{t^{\circ } }{\rightarrow}\) Cu + H2O
Bài 6 trang 45 SGK Hóa 11
Khi hòa tan 30,0 g hỗn hợp đồng và đồng (II) oxit trong 1,50 lít dung dịch axit nitric 1,00 M (loãng) thấy thoát ra 6,72 lít nitơ monoaxit (đktc). Xác định hàm lượng phần trăm của đồng (II) oxit trong hỗn hợp, nồng độ mol của đồng (II) nitrat và axit nitric trong dung dịch sau phản ứng, biết rằng thể tích dung dịch không thay đổi.
Đáp án hướng dẫn giải
nNO = 6,72/22,4 = 0,300 (mol)
nHNO3 = 1,00 x 1,5 = 1,5 (mol)
pthh: 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O (1)
Theo (1) ta tính được nCu = 0,45 mol => mCu = 28,8 gam
nHNO3 = 1,2 mol
nCu(NO3)2 = 0,45 mol
mCuO = 30 gam – 28,8 gam = 1,2 gam => nCuO = 0,015 mol
CuO + 2HNO3 → Cu(NO3)2 + H2O (2)
Theo (2) ta tính được nHNO3 là 0,030 mol,
nCu(NO3)2 là 0,015 mol
Phần trăm khối lượng CuO: % mCuO = 1,2/30.100% = 4,0%
Từ (1) và (2) ta tính được số mol HNO3 dư là 0,27 mol.
Nồng độ mol HNO3 sau phản ứng: 0,18 M
Nồng độ mol của Cu(NO3)2: 0,31 M
Bài 7 trang 45 SGK Hóa 11
Để điều chế 5,000 tấn axit nitric nồng độ 60,0% cần dùng bao nhiêu tấn amoniac? Biết rằng sự hao hụt amoniac trong quá trình sản xuất là 3,8%.
Đáp án hướng dẫn giải
Tính khối lượng HNO3 nguyên chất: 3,00 tấn.
Pthh: 4NH3 + 5O2 ![]() \(\xrightarrow[pt]{850-900^{o} C}\) 4NO + 6H2O (1)
\(\xrightarrow[pt]{850-900^{o} C}\) 4NO + 6H2O (1)
2NO + O2 → 2NO2 (2)
4NO2 + O2 + 2H2O → 4HNO3 (3)
Từ các phương trình trên ta có sơ đồ hợp thức: NH3 → HNO3 (4)
Theo (4), ta tính được khối lượng NH3 (hao hụt 3,8%): (3,00.17,0)/63,0 x (100/96,2) = 0,841 (tấn)
>> Mời các bạn tham khảo thêm giải hóa 11 bài tiếp theo tại: Giải bài tập Hóa 11 Bài 10: Photpho
............................
Trên đây VnDoc đã giới thiệu tới các bạn Giải bài tập Hóa 11 bài 9: Axit nitric và muối nitrat. Để có thể nâng cao kết quả trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán 11, Chuyên đề Hóa học 11, Giải bài tập Hoá học 11. Tài liệu học tập lớp 11 mà VnDoc tổng hợp và đăng tải.
Để tiện trao đổi, chia sẻ kinh nghiệm giảng dạy và học tập môn học THPT, VnDoc mời các bạn truy cập nhóm riêng dành cho lớp 11 sau: Nhóm Tài liệu học tập lớp 11 để có thể cập nhật được những tài liệu mới nhất.
