Giải bài tập Hóa 11 Bài 41: Phenol
Giải bài tập Hóa 11 trang 193 Phenol
VnDoc mời thầy cô cùng các bạn học sinh tham khảo tài liệu Giải bài tập Hóa 11 Bài 41: Phenol, chắc chắn bộ tài liệu sẽ là nguồn thông tin hữu ích để giúp các bạn học sinh rèn luyện giải bài tập Hóa học 11 một cách nhanh và chính xác nhất.
A. Tóm tắt Hóa 11 bài 41 Phenol
1. Định nghĩa, phân loại
Phenol là những hợp chất hữu cơ trong phân tử có nhóm -OH liên kết trực tiếp với nguyên tử C của vòng benzen
Cần phân biệt phenol và ancol thơm
Phân loại: Dựa vào số nhóm -OH trong phân tử, phenol chia thành 2 loại: phenol đơn chức và đa chức
2. Tính chất vật lí
Ở điều kiện thường, phenol là chất rắn màu trắng, nóng chảy ở 43 độ C. Để lâu, phenol bị oxi hóa chậm bởi không khí nên chuyển thành màu hồng
Phenol rất độc, khi dây vào tay có thể gây bỏng da
Phenol ít tan trong nước lạnh, nhưng tan nhiều trong nước nóng ( tan tốt nhất ở 66 độ C) và etanol
3. Tính chất hóa học của Phenol
Phản ứng thế nguyên tử H của nhóm –OH
Tác dụng với kim loại kiềm và dung dịch kiềm tạo muối phenolat:
C6H5-OH + NaOH → C6H5-ONa + H2O
C6H5-ONa + CO2 + H2O → C6H5-OH + NaHCO3
So sánh tính axit: CO2 > phenol > HCO3- > ancol.
Phản ứng ở vòng benzen
Phenol tác dụng với nước brom tạo kết tủa trắng.
Phản ứng thế vào nhân thơm ở phenol dễ hơn benzen nếu cho phenol phản ứng ở điều kiện êm dịu hơn thì thế được ở các vị trí para và ortho
Ví dụ: Dung dịch phenol tác dụng với dung dịch HNO3 cho 2,4,6-trinitrophenol kết tủa màu vàng
C6H5OH + 3HNO3 → C6H2(NO2)3OH + 3H2O
4. Ứng dụng
Phenol là nguyên liệu dùng để sản xuất các loại nhựa dùng để chế tạo các đồ dùng dân dụng
Phenol còn được dùng để sản xuất phẩm nhuộm, thuốc nổ, chất diệt nấm mốc,...
B. Giải bài tập Hóa 11 bài 41 Phenol
Bài 1 trang 193 SGK Hóa 11
Ghi Đ (đúng) hoặc S (sai) vào ô trống bên cạnh các câu sau:
a) Phenol C6H5-OH là một rượu thơm
b) Phenol tác dụng được với natri hidroxit tạo thành muối và nước.
c) Phenol tham gia phản ứng thế brom và thế nitro dễ hơn benzen
d) Dung dịch phenol làm quỳ tím hóa đỏ do nó là axit
e) Giữa nhóm –OH và vòng benzen trong phân tử phenol có ảnh hưởng qua lại lẫn nhau.
Đáp án hướng dẫn giải
S a) Phenol C6H5-OH là một rượu thơm
Đ b) Phenol tác dụng được với natri hidroxit tạo thành muối và nước.
Đ c) Phenol tham gia phản ứng thế brom và thế nitro dễ hơn benzen
S d) Dung dịch phenol làm quỳ tím hóa đỏ do nó là axit
Đ e) Giữa nhóm –OH và vòng benzen trong phân tử phenol có ảnh hưởng qua lại lẫn nhau.
Bài 2 trang 193 SGK Hóa 11
Từ benzen và các chất vô cơ cần thiết có thể điều chế được các chất sau:
2,4,6-tribomphenol (1) ; 2,4,6-trinitrophenol (2)
Viết phương trình hóa học của các phản ứng xảy ra.
Đáp án hướng dẫn giải
C6H6 ![]() \(\xrightarrow[Fe]{Br_{2} }\) C6H5Br
\(\xrightarrow[Fe]{Br_{2} }\) C6H5Br![]() \(\xrightarrow[t^{\circ } ,p]{ddNaOHđ }\) C6H5ONa
\(\xrightarrow[t^{\circ } ,p]{ddNaOHđ }\) C6H5ONa ![]() \(\overset{H^{+ } }{\rightarrow}\) C6H5OH
\(\overset{H^{+ } }{\rightarrow}\) C6H5OH ![]() \(\overset{H_{2} O}{\rightarrow}\) Br3C6H2OH
\(\overset{H_{2} O}{\rightarrow}\) Br3C6H2OH ![]() \(\overset{ddHNO_{3} }{\rightarrow}\) (NO2)3C6H2OH
\(\overset{ddHNO_{3} }{\rightarrow}\) (NO2)3C6H2OH
Bài 3 trang 193 SGK Hóa 11
Cho 14,0 gam hỗn hợp A gồm phenol và etanol tác dụng với natri dư thu được 2,24 lít khí hidro (đktc)
a. Viết các phương trình hóa học xảy ra.
b. Tính thành phần phần trăm khối lượng của mỗi chất trong A.
c. Cho 14,0 gam hỗn hợp A tác dụng với HNO3 thì thu được bao nhiêu gam axit picric (2,4,6- trinitrophenol)?
Đáp án hướng dẫn giải
a) Phương trình phản ứng:
2C6H5OH + 2Na → 2C6H5ONa + H2↑
x mol x/2mol
2C2H5OH + 2Na → 2C2H5OH + H2↑
y mol y/2
![]() \(\left\{ \begin{array}{l}
94x + 46y = 14\\
x + y = 0,2
\end{array} \right. = > \left\{ \begin{array}{l}
x = 0,1\\
y = 0,1
\end{array} \right.\)
\(\left\{ \begin{array}{l}
94x + 46y = 14\\
x + y = 0,2
\end{array} \right. = > \left\{ \begin{array}{l}
x = 0,1\\
y = 0,1
\end{array} \right.\)
%mphenol = 67,1%; %metanol = 32,9%
c) C6H5OH + 3HNO3 → (NO2)3C6H2OH + 3H2O
m(NO2)3C6H2OH = 0,100 x 229 = 22,9 g
Bài 4 trang 193 SGK Hóa 11
Cho từ từ phenol vào nước brom; stiren vào dung dịch brom trong CCl4. Nêu hiện tượng và viết các phương trình hóa học.
Đáp án hướng dẫn giải
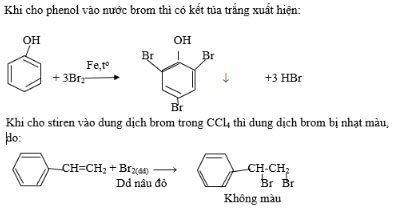
Bài 5 trang 193 SGK Hóa 11
Sục khí CO2 vào dung dịch natri phenolat thấy dung dịch vẩn đục, trong dung dịch có NaHCO3 được tạo thành. Viết phương trình hóa học của phản ứng xảy ra và giải thích. Nhận xét về tính axit của phenol.
Đáp án hướng dẫn giải
C6H5ONa + CO2 + H2O ![]() \(\overset{t^{\circ } }{\rightarrow}\) C6H5OH + NaHCO3
\(\overset{t^{\circ } }{\rightarrow}\) C6H5OH + NaHCO3
Dung dịch bị vẩn đục là do phản ứng tạo ra phenol.
Nhận xét về tính axit của phenol: Phenol có tính axit yếu hơn nấc thứ nhất của axit cacbonic H2CO3, nên bị axit cacbonic đẩy ra khỏi dung dịch muối.
Bài 6 trang 193 SGK Hóa 11
Viết các phương trình hóa học điều chế: phenol từ benzen (1); stiren từ etylbenzen (2). Các chất vô cơ cần thiết coi như có đủ.
Đáp án hướng dẫn giải
(1) Điều chế phenol phenol từ benzen:
C6H6 + Br2![]() \(\xrightarrow[Fe]{t^{\circ } }\) C6H5Br + HBr
\(\xrightarrow[Fe]{t^{\circ } }\) C6H5Br + HBr
C6H5Br + 2NaOHđặc ![]() \(\xrightarrow[p]{t^{\circ } }\) C6H5ONa + NaBr + H2O
\(\xrightarrow[p]{t^{\circ } }\) C6H5ONa + NaBr + H2O
C6H5ONa + CO2 + H2O ![]() \(\xrightarrow[]{t^{\circ } }\) C6H5OH + NaHCO3
\(\xrightarrow[]{t^{\circ } }\) C6H5OH + NaHCO3
(2) Điều chế stiren từ etybenzen
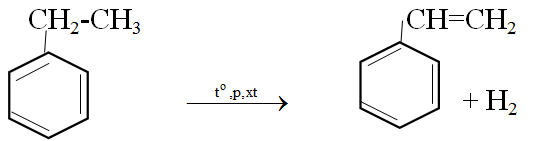
-------------------------------------
Trên đây VnDoc.com đã giới thiệu tới bạn đọc tài liệu: Giải bài tập Hóa 11 Bài 41: Phenol. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Hóa học lớp 10, Giải bài tập Hóa học lớp 11, Thi thpt Quốc gia môn Văn, Thi thpt Quốc gia môn Lịch sử, Thi thpt Quốc gia môn Địa lý, Thi thpt Quốc gia môn Toán, đề thi học kì 1 lớp 11, đề thi học kì 2 lớp 11 mà VnDoc tổng hợp và đăng tải.
Để tiện trao đổi, chia sẻ kinh nghiệm giảng dạy và học tập môn học THPT, VnDoc mời các bạn truy cập nhóm riêng dành cho lớp 11 sau: Nhóm Tài liệu học tập lớp 11 để có thể cập nhật được những tài liệu mới nhất.

