Bài thực hành số 2 hóa 10
Bài thực hành 2 hóa 10: Tính chất hóa học của khí Clo và hợp chất của Clo
Bài thực hành số 2 hóa 10 được VnDoc biên soạn, hướng dẫn các bạn học sinh chuẩn bị bài cũng như các thao tác chuẩn bị, cách thực hiện thí nghiệm giúp buổi thực hành của các bạn tốt hơn. Bên cạnh đó tài liệu sẽ hướng dẫn các bạn cách viết bản tường trình hóa 10 bài thực hành số 2.
Mời các bạn tham khảo các bài thực hành có trong chương trình hóa học 10
- Bài thực hành số 1 hóa 10: Phản ứng oxi hóa khử
- Bài thực hành số 3 Hóa học 10: Tính chất hóa học của brom và iot
- Bài thực hành số 4 hóa 10: Tính chất của oxi lưu huỳnh
1. Nội dung thí nghiệm và cách tiến hành
Thí nghiệm 1: Điều chế khí Clo – Tính tẩy màu của khí clo ẩm
a. Dụng cụ, hóa chất:
Dụng cụ: ống nghiệm, nút cao sụ, kẹp gỗ,…
Hóa chất: Tinh thể KMnO4, dung dịch HCl đậm đặc, giấy quỳ.
b. Cách tiến hành:
Cho vào ống nghiệm khô một vài tinh thể KMnO4, nhỏ tiếp vào ống nghiệm vài giọt dung dịch HCl đặc.
Đậy nhanh ống nghiệm bằng nút cao su có đính một băng giấy màu ẩm.
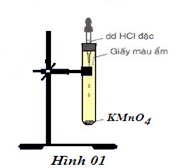
Hiện tượng – giải thích:
Hiện tượng: Có khí màu vàng thoát ra. Quỳ tím ẩm dần dần bị mất màu.
Giải thích: Khí màu vàng là do clo được tạo thành do phản ứng:
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Sau đó clo tan vào nước tạo ra HClO (axit có tính oxi hóa mạnh) làm mất màu quỳ tím.
Cl2 + H2O ⥩ HCl + HClO
Thí nghiệm 2: Điều chế axit clohidric
Dụng cụ, hóa chất:
Dụng cụ: ống nghiệm, đèn cồn, ống dẫn khí, nút cao su, giá đỡ ống nghiệm, bông,…
Hóa chất: NaCl, H2SO4 đặc, nước cất, giấy quỳ.
Cách tiến hành:
Cho vào ống nghiệm (1) một ít muối ăn rồi rót dung dịch H2SO4 đặc. Rót khoảng 8ml nước cất vào ống nghiệm (2)
Đun nhẹ ống nghiệm chứa NaCl rắn và H2SO4 đặc.
Nếu thấy sủi bọt mạnh thì ngừng đun.
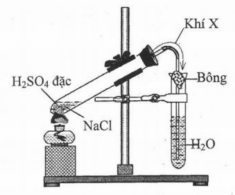
Hiện tượng – giải thích:
Khi đun ống nghiệm chứa NaCl rắn và H2SO4 đặc có khói trắng bay lên ( khí HCl) sau đó dẫn sang ống nghiệm chứa H2O
PTHH: NaCl(rắn) + H2SO4(đặc) ![]() \(\overset{t^{\circ } }{\rightarrow}\) NaHSO4 + HCl
\(\overset{t^{\circ } }{\rightarrow}\) NaHSO4 + HCl
Cho giấy quỳ tím vào ống nghiệm chứa H2O (đã hấp thụ khí HCl) giấy quỳ chuyển sang màu đỏ do dung dịch HCl là dung dịch axit mạnh.
Thí nghiệm 3: Bài tập thực nghiệm phân biệt các dung dịch: HCl, NaCl, HNO3
Cách 1:
Dùng quỳ tím phân biệt được NaCl vì không có hiện tượng
Dùng tiếp dung dịch AgNO3 phân biệt được HCl vì có kết tủa trắng
Phương trình hóa học: AgNO3 + HCl → AgCl↓ + HNO3
Cách 2:
Dùng AgNO3 phân biệt được HNO3 vì không có hiện tượng
AgNO3 + HCl → AgCl↓ + HNO3
AgNO3 + NaCl → AgCl↓ + NaNO3
Dùng tiếp quỳ tím phân biệt được NaCl vì không có hiện tượng.
2. Bản tường trình hóa 10 bài thực hành số 2
| Cách tiến hành | Hiện tượng, giải thích | Phương trình hóa học | |
| Thí nghiệm 1: Điều chế khí Clo – Tính tẩy màu của khí clo ẩm | |||
| Thí nghiệm 2: Điều chế axit clohidric | |||
| Thí nghiệm 3: Bài tập thực nghiệm phân biệt các dung dịch: HCl, NaCl, HNO3 |
.........................................................
Lưu ý
Trên đây VnDoc đã gửi tới bạn đọc chi tiết nội dung Hóa 10 Bài 27: Bài thực hành số 2 Tính chất hóa học của khí clo và hợp chất của clo gồm 3 thí nghiệm:
- Thí nghiệm 1: Điều chế khí Clo – Tính tẩy màu của khí clo ẩm
- Thí nghiệm 2: Điều chế axit clohidric
- Thí nghiệm 3: Bài tập thực nghiệm phân biệt các dung dịch: HCl, NaCl, HNO3
Để có thể hoàn thành tốt bài thực hành thí nghiệm trên lớp một cách tốt nhất, cũng như biết cách viết báo cáo sau khi thực hành một cách chính xác bạn đọc cần:
Nắm được các nội quy của phòng thí nghiệm, cũng như cách sử dụng, dụng cụ thí nghiệm hóa chất, tránh gây đổ vỡ, mất an toàn. Tuyệt đối tuân theo sự hướng dẫn của giáo viên bộ môn.
Trong quá trình thực hành để thu được kết quả tốt nhất các bạn học sinh cần chú ý:
+ Tập trung quan sát giáo viên bộ môn hướng dẫn
+ Chú ý các thao tác cầm kẹp gỗ, sử dụng giá ống nghiệm, hay cách lấy hóa chất, ....
+ Chuẩn bị đọc bài thật kĩ, trước khi đến lớp.
Trên đây VnDoc đã giới thiệu Bài thực hành số 2 hóa 10. Để có kết quả học tập tốt và hiệu quả hơn, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa học 10, Chuyên đề Vật Lý 10, Chuyên đề Hóa học 10, Giải bài tập Toán 10. Tài liệu học tập lớp 10 mà VnDoc tổng hợp biên soạn và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THPT miễn phí trên Facebook, mời bạn đọc tham gia nhóm Tài liệu học tập lớp 10 để có thể cập nhật thêm nhiều tài liệu mới nhất.
