Hóa học 10 Bài 7: Bảng tuần hoàn các nguyên tố hóa học
Hóa học 10 Bài 7: Bảng tuần hoàn các nguyên tố hóa học được VnDoc biên soạn là nội dung trọng tâm kiến thức hóa 10 bài 7, giới thiệu bảng tuần hoàn hóa học tới các bạn, biết cấu tạo cũng như sự sắp xếp các nguyên tố hóa học như thế nào.
Bảng tuần hoàn các nguyên tố hóa học
Hy vọng qua tài liệu sẽ giúp các bạn nắm chắc kiến thức từu đó vận dụng vào giải các bài tập. Mời các bạn tham khảo
A. Tóm tắt lý thuyết Hóa 10 Bài 7
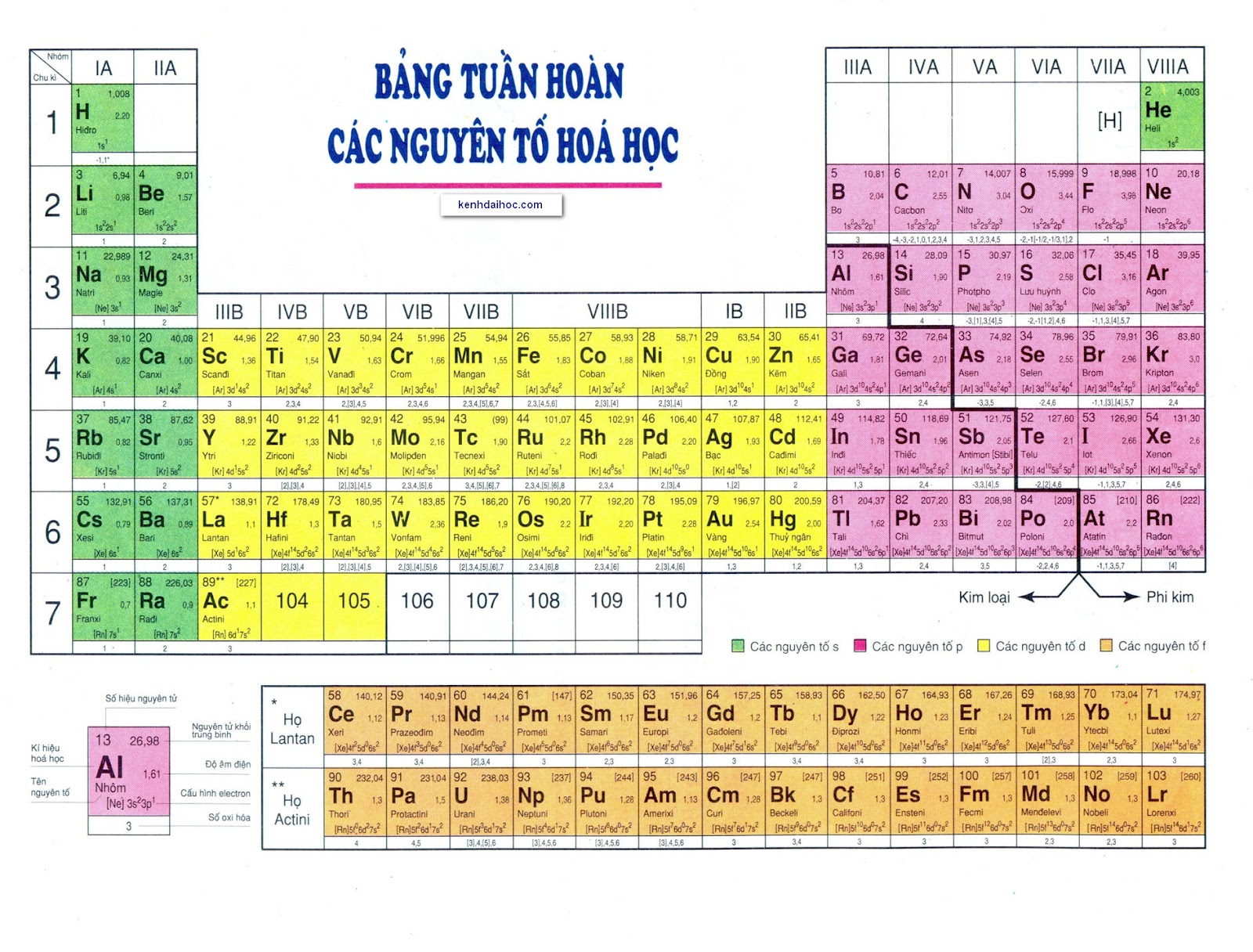
I. Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn
- Các nguyên tố được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử.
- Các nguyên tố có cùng số lớp electron trong nguyên tử được sắp xếp thành một hàng (chu kì)
- Các nguyên tố có số electron hóa trị trong nguyên tử như nhau được xếp thành một cột (nhóm)
II. Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
1. Ô nguyên tố
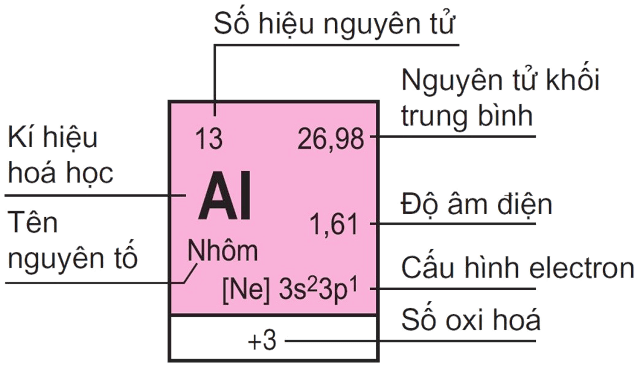
Mỗi nguyên tố hóa học được xếp vào một ô của bảng gọi là ô nguyên tố.
Số thứ tự của ô nguyên tố đúng bằng số hiệu nguyên tử của nguyên tố đó.
2. Chu kì
- Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được sắp xếp theo chiều điện tích hạt nhân tăng dần.
Chu kì 1: gồm 2 nguyên tố H (Z=1) đến He (Z=2).
Chu kì 2: gồm 8 nguyên tố Li (Z=3) đến Ne (Z=10).
Chu kì 3: gồm 8 nguyên tố Na (Z=11) đến Ar (Z=18).
Chu kì 4: gồm 18 nguyên tố K (Z=19) đến Kr (Z=36).
Chu kì 5: gồm 18 nguyên tố Rb (Z=37) đến Xe (Z=54).
Chu kì 6: gồm 32 nguyên tố Cs (Z=55) đến Rn (Z=86).
Chu kì 7: Bắt đầu từ nguyên tố Fr (Z=87) đến nguyên tố có Z = 110, đây là một chu kì chưa hoàn thành.
- Chu kì 1, 2, 3 là các chu kì nhỏ.
- Chu kì 4, 5, 6, 7 là các chu kì lớn.
3. Nhóm nguyên tố
- Nhóm nguyên tố là tập hợp các nguyên tố mà nguyên tử có cấu hình electron tương tự nhau, do đó có tính chất hóa học gần giống nhau và được sắp xếp thành một cột.
- Có 2 loại nhóm nguyên tố là nhóm A và nhóm B
Nhóm A: bao gồm các nguyên tố s và p.
Nhóm A gồm 8 nhóm từ IA đến VIIIA
Các nguyên tố nhóm A gồm nguyên tố s và nguyên tố p
Số thứ tự nhóm A = tổng số e lớp ngoài cùng
Nhóm B: bao gồm các nguyên tố d và f có cấu hình e nguyên tử tận cùng (n-1)dxnsy
Nếu (x+y) = 3 => 7 thì nguyên tố thuộc nhóm (x+y)B.
Nếu (x+y) = 8 => 10 nguyên tố thuộc nhóm VIIIB
Nếu (x+y) > 10 thì nguyên tố thuộc nhóm (x+y-10)B
Các nguyên tố nhóm B là tập hợp các nguyên tố có electron hóa trị nằm trên phân lớp d và f
Mời các bạn tham khảo thêm lý thuyết hóa 10 bài tiếp theo tại: Hóa học 10 Bài 8: Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học
B. Bài tập Hóa 10 bài 7
1. Phần câu hỏi trắc nghiệm
Câu 1. Trong bảng tuần hoàn, các nguyên tố hóa học được sắp xếp theo chiều
A. Tăng dần của điện tích hạt nhân nguyên tử
B. Tăng dần của nguyên tử khối
C. Giảm dần của điện tích hạt nhân nguyên tử
D. Giảm dần của nguyên tử khối
Câu 2. Trong bảng tuần hoàn, số thứ tự của ô chính là
A. Số khối
B. Khối lượng nguyên tử
C. Số hiệu nguyên tử
D. Tất cả đều đúng
Câu 3. Các nguyên tô xếp ở chu kì 6 có số lớp electron trong nguyên tử là
A. 3
B. 5
C. 6
D. 7
Câu 4. Nguyên tử X có số thứ tự là 16, vị trí của nguyên tố X trong bảng tuần hoàn là?
A. Chu kỳ 2, nhóm IIA
B. Chu kỳ 3, nhóm IIIA
C. Chu kỳ 3, nhóm VIA
D. Chu kỳ 3, nhóm IVA
Câu 5. Nguyên tố M thuộc chu kì 3, nhóm IVA của bảng tuần hoàn. Số hiệu nguyên tử của nguyên tố M là:
A. 14
B. 16
C. 33
D. 35
2. Phần bài tập tự luận
Câu 1: Cho nguyên tử có kí hiệu 1632X
a. Xác định các giá trị A, Z, p, n, e? Tên X? Cấu hình e?
b. Xác định vị trí X trong bảng tuần hoàn?
Đáp án hướng dẫn giải chi tiết
a. A = 32, Z = 16, p = e = 16, n = 16
b. X là lưu huỳnh
Bài 2: Nguyên tố Y thuộc chu kì 3, nhóm VA.
a. Y có bao nhiêu lớp e? Y có bao nhiêu e hóa trị? Các e hóa trị này thuộc lớp e nào?
b. Viết cấu hình e nguyên tử của Y?
Đáp án hướng dẫn giải chi tiết
a. Y có 3 lớp 2, có 5 e hóa trị thuộc lớp p
b. Cấu hình e của Y là (Ne) 3s23p3
Bài 3: Nguyên tố X thuộc chu kì 4, nhóm IIIB.
a. X có bao nhiêu lớp e? X có bao nhiêu e hóa trị? Các e hóa trị này thuộc lớp e nào?
b. Viết cấu hình e nguyên tử của X?
Đáp án hướng dẫn giải chi tiết
a. X có 4 lớp e, X có 2 hóa trị, các hóa trị này thuộc lớp s
b. Cấu hình e của X là (Ar)3d14s2
Bài 4: Tổng số hạt proton, nơtron, electron trong nguyên tử X thuộc nhóm VIIA là 52. Viết cấu hình e và xác định vị trí của nguyên tố trong BTH?
Đáp án hướng dẫn giải chi tiết
2p + n = 52 => n = 52 - 2p
p ≤ n = 52 - 2p ≤ 1,5p
Giải bất phương trình
p nhận giá trị: 15 và 17
Khi p = 15 (Photpho: P) thuộc nhóm IVA loại
Khi p = 17 (Clo: Cl) thuộc nhóm VIIA nhận
Cấu hình e Cl: (Ne)3s23p5
Nằm ở ô số 17, chu kì 3 nhóm VIIA
Bài 5: Một nguyên tử R có tổng số các hạt là 115. Số hạt mang điện nhiều hơn số hạt không mạng điện là 25 hạt. Xác định vị trí của R trong BTH?
Đáp án hướng dẫn giải chi tiết
2p + n = 115 (1)
2p - n = 25 (2)
Từ (1) và (2)
p = e = 35, n = 45 Vậy R là Br
C. Trắc nghiệm hóa 10 bài 7: Bảng tuần hoàn các nguyên tố hóa học
Nhằm giúp các bạn học sinh củng cố, nâng cao kiến thức và vận dụng thật tốt kiến thức, VnDoc đã biên soạn bộ câu hỏi trắc nghiệm Hóa 10 bài 7 tại: Trắc nghiệm Hóa học 10 bài 7: Bảng tuần hoàn các nguyên tố hóa học
D. Giải bài tập Hóa 10 bài 7: Bảng tuần hoàn các nguyên tố hóa học
Ngoài các dạng câu hỏi bài tập sách giáo khoa hóa 10 bài 7, để nâng cao củng cố cũng như vận dụng tốt kiến thức lý thuyết hóa 10 bài 7. Các bạn học sinh cần làm thêm các dạng câu hỏi bài tập sách giáo khoa hóa 10 bài 7. Để giúp bạn đọc nắm được các phương pháp giải bài tập. VnDoc đã biên soạn hướng dẫn bạn đọc giải bài tập Giải bài tập Hóa 10 Bài 7: Bảng tuần hoàn các nguyên tố hóa học
...............................
Mời các bạn tham khảo thêm một số tài liệu liên quan
- Giải Hóa 10 bài 8: Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học
- Hóa 10 bài 9: Sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học. Định luật tuần hoàn
- Giải Hóa 10 Bài 9: Sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học
Trên đây VnDoc đã giới thiệu Hóa học 10 Bài 7: Bảng tuần hoàn các nguyên tố hóa học tới các bạn. Để có kết quả học tập tốt và hiệu quả hơn, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa học 10, Chuyên đề Vật Lý 10, Chuyên đề Hóa học 10, Giải bài tập Toán 10. Tài liệu học tập lớp 10 mà VnDoc tổng hợp biên soạn và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THPT miễn phí trên Facebook, mời bạn đọc tham gia nhóm Tài liệu học tập lớp 10 để có thể cập nhật thêm nhiều tài liệu mới nhất.
