Giải bài tập Hóa 12 nâng cao bài 21
Hóa học 12 - Luyện tập: Tính chất của kim loại
VnDoc xin giới thiệu tới bạn đọc tài liệu Giải bài tập Hóa 12 nâng cao bài 21, tài liệu chắc chắn sẽ là nguồn thông tin hữu ích để phục vụ công việc học tập của các bạn học sinh được tốt hơn. Mời thầy cô và các bạn học sinh cùng tham khảo.
Giải bài tập Hóa 12 nâng cao bài 17
Giải bài tập Hóa 12 nâng cao bài 18
Giải bài tập Hóa 12 nâng cao
Bài 1 (trang 125 sgk Hóa 12 nâng cao): a) Phản ứng hóa học xảy ra trong pin điện hóa:
2Cr + 3Cu2+ → 2Cr3+ + 3Cu
Eo của pin điện hóa là:
A. 0,40V
B. 1,08V
C. 1,25V
D. 2,5V
Biết Eo(Cu2+/Cu) = +0,34; Eo(Cr3+/Cr) = -0,74 V
b) Phản ứng hóa học xảy ra trong pin điện hóa:
2Au3+ + 3Ni → 2Au + 3Ni2+
Eo của pin điện hóa là:
A. 3,75 V
B. 2,25 V
C. 1,75 V
D. 1,25 V
Lời giải:
a) Đáp án B
b) Đáp án C
Bài 2 (trang 125 sgk Hóa học 12 nâng cao): a. Chất nào sau đây có thể oxi hóa thành Zn2+?
A. Fe
B. Ag+
C. Al3+
D. Ca2+
b. Kim loại Zn có thể khử được các ion nào sau đây?
A. Na+
B. H+
C. Ca2+
D. Mg2+
Lời giải:
a) Đáp án B
b) Đáp án B
Bài 3 (trang 125 sgk Hóa 12 nâng cao): Trong quá trình pin điện hóa Zn – Ag hoạt động, ta nhận thấy:
A. khối lượng của điện cực Zn tăng
B. Khối lượng của điện cực Ag giảm
C. Nồng độ của ion Zn2+ trong dung dịch tăng
D. Nồng độ của ion Ag+ trong dung dịch tăng
Lời giải:
A – Sai
B – Đúng
C – Đúng
D – Sai
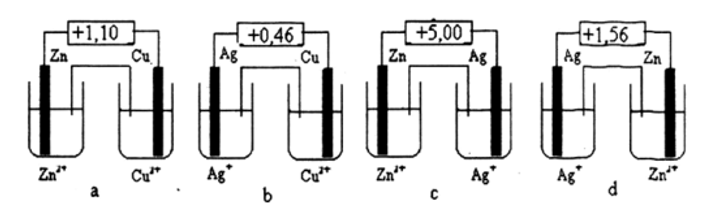
Bài 4 (trang 125 sgk Hóa 12 nâng cao): Dưới đây là hình vẽ của 4 sơ đồ pin điện hóa chuẩn. Hãy cho biết sơ đồ nào được vẽ và chú thích đúng, sai. Đề nghị sửa lại những chỗ sai.
Cho biết Eo(Ag+/Ag) = +0,80 V
Eo(Cu2+/Cu) = +0,34 V
Eo(Zn2+/Zn) = -0,76 V
Lời giải:
1) Sơ đồ (a) vẽ đúng, suất điện động chuẩn của pin ghi đúng
2) Sơ đồ (b) vẽ sai, suất điện động chuẩn của pin ghi đúng
3) Sơ đồ (c) vẽ đúng, suất điện động chuẩn của pin ghi sai
4) Sơ đồ (d) vẽ sai, suất điện động chuẩn của pin ghi đúng
Sửa lại như sau:
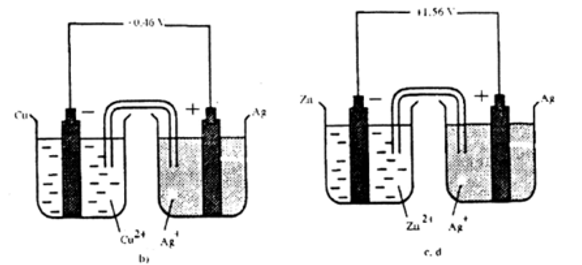
Bài 5 (trang 125 sgk Hóa 12 nâng cao): Khi nhúng một lá Zn vào dung dịch muối Co2+, nhận thấy có một lớp kim loại Co phủ ngoài lá kẽm. Khi nhúng lá Pb và dung dịch muối trên, không nhận thấy hiện tượng nào xảy ra.
a. Kim loại nào có tính khử mạnh nhất trong số 3 kim loại trên
b. Cation nào có tính oxi hóa mạnh nhất trong số 3 cation kim loại trên
c. Sắp xếp cặp oxi hóa – khử của những kim loại trên theo chiều tính oxi hóa của cation tăng dần.
d. Viết phương trình hóa học của phản ứng xảy ra giữa các cặp oxi hóa – khử
Lời giải:
a. Zn đẩy dược Co; Pb không đẩy được Co
=> Zn có tính khử mạnh nhất
b. Pb2+ có tính oxi hóa mạnh nhất
c. Xếp theo chiều tăng dần tính oxi hóa của cation: Zn2+/Zn; Co2+/Co; Pb2+/Pb
d. Các phản ứng xảy ra giữa các cặp oxi hóa khử
Zn + Co2+ → Zn2+ + Co
Zn + Pb2+ → Zn2+ + Pb
Co + Pb2+ → Co2+ + Pb
Bài 6 (trang 126 sgk Hóa 12 nâng cao): Hãy giải thích hiện tượng thí nghiệm: Ngâm một lá Zn nhỏ, tinh khiết trong dung dịch HCl thấy bọt khí H2 thoát ra ít và chậm. Nếu nhỏ thêm vài giọt dung dịch CuSO4 thấy bọt khí H2 thoát ra rất nhiều và nhanh.
Lời giải:
Zn + 2HCl → ZnCl2 + H2
Bọt khí hidro thoát ra ít và chậm do H2 sinh ra trên bề mặt lá kẽm cản trở phản ứng. Khi thêm CuSO4: Zn + CuSO4 → ZnSO4 + Cu
Cu được giải phóng bám trên viên kẽm hình thành cặp pin điện hóa Zn – Cu trong đó
Zn là cực âm và bị ăn mòn Zn → Zn2+ + 2e
Electron đến cực dương là Cu, tại đây 2H+ + 2e → H2
Bọt khí hidro thoát ra ở cực dương nhiều và liên tục
Bài 7 (trang 126 sgk Hóa 12 nâng cao): Cho cặp oxi hóa – khử sau : Ag+/Ag; Fe2+/Fe; Zn2+/Zn
1) Hãy viết các phản ứng biến đổi qua lại giữa cation kim loại và nguyên tử kim loại trong mỗi cặp
2) Hãy cho biết trong các cặp oxi hóa – khử đã cho, chất nào có tính
a. oxi hóa mạnh nhất?
b. oxi hóa yếu nhất ?
c. Khử mạnh nhất?
d. Khử yếu nhất?
Lời giải:
1. Ag+ + e → Ag
Fe2+ + 2e → Fe
Zn2+ + 2e → Zn
2. Chất oxi hóa mạnh nhất: Ag+
Chất oxi háo yếu nhất: Zn2+
Chất khử mạnh nhất: Zn
Chất khử yếu nhất: Ag
Bài 8 (trang 126 sgk Hóa 12 nâng cao): Hãy tính thế điện cực chuẩn của cặp oxi hóa – khử Eo (Zn2+/Zn). Biết rằng EpđhoZn-Cu = 1,10 V và Eo (Cu2+/Cu ) = +0,34 V
Lời giải:
Epđho = EoCu2+/Cu - EoZn2+/Zn = +1,1 V => EoZn2+/Zn = +0,34 – 1,1 = -0,76 V
Bài 9 (trang 126 sgk Hóa 12 nâng cao): Có những pin điện hóa được tạo thành từ những cặp oxi hóa – khử sau:
1) Pb2+/Pb và Fe2+/Fe
2) Ag+/Ag và Fe2+/Fe
3) Ag+/Ag và Pb2+/Pb
Hãy tính suất điện động chuẩn của mỗi pin điện hóa
Biết rằng: Eo (Ag+/Ag) = +0,80 V
Eo (Pb2+/Pb ) = -0,13 V
Eo (Fe2+/Fe) = -0,44 V
Lời giải:
1, EoFe-Pb = EoPb2+/Pb - EoFe2+/Fe = -0,13 – (-0,44) = +0,31 V
2, EoFe-Ag= EoAg+/Ag - EoFe2+/Fe = +0,8 – (-0,44) = + 1,24 V
3, EoPb-Ag= EoAg+/Ag - EoPb2+/Pb = +0,8 – (-0,13) = +0,93 V
Bài 10 (trang 126 sgk Hóa 12 nâng cao): Có những pin điện hóa được ghép bởi những cặp oxi hóa – khử chuẩn sau:
a) Pb2+/Pb và Zn2+/Zn
b) Cu2+/Cu và Hg2+/Hg biết EoHg2+/Hg = +0,85
c) Mg2+/Mg và Pb2+/Pb
1) Xác định điện cực âm và điện cực dương của mỗi pin điện hóa
2) Viết phương trình hóa học của các phản ứng xảy ra ở các điện cực của mỗi pin và phương trình hóa học dạng ion thu gọn của mỗi pin điện hóa khi phóng điện
3) Xác định suất điện động chuẩn của các pin điện hóa
Lời giải:
1. Phản ứng trong pin điện hóa: Zn + Pb2+ → Zn2+ + Pbv
Zn → Zn2+ +2e
Zn: Cực âm, anot
Pb2+ + 2e → Pb
Pb: cực dương, catot
EoZn-Pb = -0,13 – (-0,76) = +0,63 V
2, Phản ứng trong pin điện hóa: Cu + Hg2+ → Cu2+ + Hg
Cu → Cu2+ +2e
Cu: Cực âm, anot
Hg2+ + 2e → Hg
Hg: cực dương, catot
EoCu-Hg = 0,85 – 0,34 = +0,51 V
3, Phản ứng trong pin điện hóa: Mg + Pb2+ → Mg2+ + Pb
Mg → Mg2+ +2e
Pb: Cực âm, anot
Pb2+ + 2e → Pb
Ag: cực dương, catot
EoMg-Pb = -0,13 – (-2,37) = +2,24 V
----------------------------------
Trên đây VnDoc.com đã giới thiệu tới bạn đọc tài liệu: Giải bài tập Hóa 12 nâng cao bài 21. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán lớp 12, Giải bài tập Hóa học lớp 12, Giải bài tập Vật Lí 12 mà VnDoc tổng hợp và đăng tải.