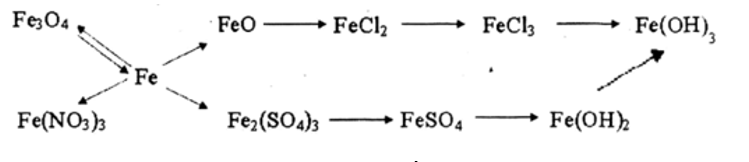Giải bài tập Hóa 12 nâng cao bài 41
Hóa học 12 - Một số hợp chất của sắt
VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa 12 nâng cao bài 41, tài liệu gồm 4 bài tập trang 202 SGK kèm theo đáp án sẽ giúp các bạn học sinh học tốt môn Hóa học một cách đơn giản hơn.
Giải bài tập Hóa 12 nâng cao bài 35
Giải bài tập Hóa 12 nâng cao bài 38
Giải bài tập Hóa 12 nâng cao
Bài 1 (trang 202 sgk Hóa học 12 nâng cao): a. Tính chất hóa học chung của hợp chất sắt (II) là gì? Dẫn ra những phản ứng hóa học để chứng minh những điều đã khẳng định (viết phương trình hóa học).
b. Tính chất hóa học chung cho hợp chất sắt (III) là gì? Dẫn ra những phản ứng hóa học để chứng minh những điều khẳng định (viết phương trình hóa học).
Lời giải:
a. Hợp chất Fe(II) vừa có tính oxi hóa, vừa có tính khử
+ Tính khử:
FeCl2 + Cl2 → FeCl3
3FeO + 10HNO3 → 3Fe(NO3)3 + NO + 5H2O
+ Tính oxi hóa Zn + FeSO4 → Fe + ZnSO4
b. Hợp chất Fe(III) có tính oxi hóa:
Fe2O3 + CO → 2FeO + CO2
Fe2SO4 + Cu → 2FeSO4 + CuSO4
Bài 2 (trang 202 sgk Hóa 12 nâng cao): Hãy dẫn ra những phản ứng hóa học để chứng minh rằng các oxit sắt (II) là oxit bazo, các hidroxit sắt (II) là bazo (Viết các phương trình phản ứng hóa học)
Lời giải:
FeO là oxi bazo: có phản ứng với axit
FeO + 2HCl → FeCl2 + H2O
Fe(OH)3 + 2HCl → FeCl2 + 2H2O
Bài 3 (trang 202 sgk Hóa 12 nâng cao): Viết các phương trình hóa học biểu diễn những chuyển đổi hóa học sau:
Lời giải:
Các phương trình hóa học
3Fe + O2 → Fe3O4
3Fe3O4 + 8Al → 4Al2O3 + 9Fe
Fe + 4HNO3 → Fe(NO3)3 + NO + H2O
Fe + H2O → FeO + H2
2FeCl2 + Cl2 → FeCl3
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
2Fe + 6H2SO4 đặc → Fe2(SO4)3 + 3SO2 + H2O
Fe2(SO4)3 + Fe → 3FeSO4
FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4
4Fe(OH)2 + O2 + H2O → 4Fe(OH)3
Bài 4 (trang 202 sgk Hóa 12 nâng cao): Hòa tan 10 gam FeSO4 có lẫn tạp chất là Fe2(SO4)3 trong nước, được 200 cm3 dung dịch. Mặt khác, 20 cm3 dung dịch này được axit hóa bằng H2SO4 loãng đã làm mất màu tím của 25 cm3 dung dịch KMnO4 0,03 M
a. Viết phương trình hóa học dạng ion rút gọn và cho biết vai trò của ion Fe2+ và ion MnO4-?
b. Có bao nhiêu mol ion Fe2+ tác dụng với 1 mol MnO4-
c. Có bao nhiêu mol Fe2+ tác dụng với 25 cm3 dung dịch KMnO4 0,03 M
d. Có bao nhiêu gam ion Fe2+ trong 200 cm3 dung dịch ban đầu?
e. Tính phần trăm theo khối lượng của FeSO4 tinh khiết?
Lời giải:
a. 5Fe2+ + MnO4- + 8H+ → 5Fe3+ + Mn2+ + 4H2O
Fe2+ → Fe3+ + e
Fe2+ là chất khử
MnO4- + 8H+ + 5e → Mn2+ + 4H2O
MnO4- là chất oxi hóa
b. Để tác dụng với 1 mol MnO4- cần 5 ml Fe2+
c. ![]() \(n_{KMnO_4}\) = 0,025.0,03 = 7,5.10-4 (mol)
\(n_{KMnO_4}\) = 0,025.0,03 = 7,5.10-4 (mol)
![]() \(n_{Fe^{2+}}\) = 5.
\(n_{Fe^{2+}}\) = 5.![]() \(n_{MnO_4^-}\)= 3,75. 10-3 (mol) trong 20 cm3
\(n_{MnO_4^-}\)= 3,75. 10-3 (mol) trong 20 cm3
d. Số mol Fe2+ trong 200 cm3 là 3,75.10-3.10 = 0,0375 mol
→ ![]() \(m_{_{Fe^{2+}}}\) = 0,0375.56 = 2,1 (g)
\(m_{_{Fe^{2+}}}\) = 0,0375.56 = 2,1 (g)
e. ![]() \(m_{FeSO_4}\) tinh khiết = 0,0375.152 = 5,7 gam
\(m_{FeSO_4}\) tinh khiết = 0,0375.152 = 5,7 gam
%FeSO4 = 5,7 : 10 x 100 = 57%
----------------------------------
Trên đây VnDoc.com đã giới thiệu tới bạn đọc tài liệu: Giải bài tập Hóa 12 nâng cao bài 41. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán lớp 12, Giải bài tập Hóa học lớp 12, Giải bài tập Vật Lí 12 mà VnDoc tổng hợp và đăng tải.