Hóa học 10 bài 5: Cấu hình electron nguyên tử
Chuyên đề Hóa học lớp 10: Cấu hình electron nguyên tử được VnDoc sưu tầm và giới thiệu tới các bạn học sinh cùng quý thầy cô tham khảo. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết
Lý thuyết: Cấu hình electron nguyên tử
A/ Lý thuyết Hóa học 10 bài 5
I. Thứ tự các mức năng lượng trong nguyên tử
1. Các nguyên lý và quy tắc phân bố electron trong nguyên tử
a/ Nguyên lý Pauli: Trên 1 obitan có tối đa 2e và 2e này chuyển động tự quay khác chiều nhau:
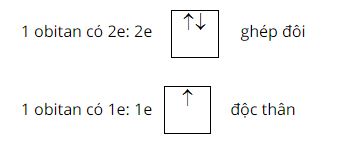
b/ Nguyên lý vững bền: Ở trạng thái cơ bản, trong nguyên tử các electron chiếm lần lượt các obitan có mức năng lượng từ thấp đến cao.
c/ Quy tắc Hund: Trong 1 phân lớp, các electron sẽ phân bố trên các obitan sao cho số electron độc thân là tối đa và có chiều tự quay giống nhau.
Ví dụ:
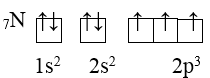
d/ Trật tự các mức năng lượng nguyên tử: Trong nguyên tử, các electron trên các obitan khác nhau, nhưng cùng 1 phân lớp có mức năng lượng như nhau. Các mức năng lượng nguyên tử tăng dần theo trình tự:
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p
II. Cấu hình electron nguyên tử
Cấu hình electron nguyên tử biểu diễn sự phân bố electron trên các phân lớp của các lớp electron khác nhau.
a/ Cách viết cấu hình electron nguyên tử
- Xác định số electron trong nguyên tử.
- Phân bố các electron theo trật tự mức năng lượng AO tăng dần.
- Viết cấu hình electron theo thứ tự các phân lớp electron trong một lớp.
Ví dụ: 26Fe. Viết theo trật tự mức năng lượng AO tăng dần:
1s22s22p63s23p64s23d6
- Sau đó viết lại theo thứ tự các phân lớp electron trong 1 lớp:
1s22s22p63s23p63d64s2
- Viết gọn: [Ar] 3d6 4s2
* Chú ý: Khi viết cấu hình electron để dễ nhớ trật tự các mức năng lượng, ta viết theo thứ tự lớp với 2 phân lớp s, p như sau:
1s 2s2p 3s3p 4s ... 4p 5s ... 5p 6s ... 6p 7s ... 7p
- Sau đó thêm 3d vào giữa lớp 4s ... 4p
- Thêm 4d vào giữa lớp 5s ... 5p
- Thêm 4f 5d vào giữa lớp 6s ... 6p
- Thêm 5f 6d vào giữa lớp 7s ... 7p
- Ta sẽ được: 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p
b/ Đặc điểm của lớp electron ngoài cùng
- Các electron lớp ngoài cùng quyết định tính chất hóa học của một nguyên tố.
- Số electron lớp ngoài cùng tối đa là 8e
+ Các nguyên tử kim loại có: 1e, 2e, 3e lớp ngoài cùng.
+ Các nguyên tử phi kim có: 5e, 6e, 7e lớp ngoài cùng.
+ Các nguyên tử khí hiếm có: 8e (He có 2e) lớp ngoài cùng.
+ Các nguyên tử có 4e lớp ngoài cùng có thể là kim loại (Ge, Sn, Pb) có thể là phi kim (C, Si).
B/ Trắc nghiệm Hóa học 10 bài 5
A. s B. p C. d D. f
A. Khi tham gia phản ứng R vừa có tính oxi hóa, vừa có tính khử.
B. Số oxi hóa cao nhất của R trong hợp chất là +6.
C. Hợp chất khí của R với hidro có tính khử mạnh.
D. R ở chu kì 2 nhóm VIA.
A. 7. B. 6. C. 5. D. 8.
A. 8. B. 7. C. 6. D. 5.
A. Ô số 14, chu kì 3, nhóm VIA.
B. Ô số 8, chu kì 2, nhóm VIA.
C. Ô số 16, chu kì 3, nhóm VIA.
D. Ô số 8, chu kì 2, nhóm IVA.
A. s B. p C. d D. f
A. 1s22s22p63s23p4.
B. 1s22s22p53s23p4.
C. 1s22s22p63s13p5.
D. 1s22s22p63s23p5.
B. Lớp thứ hai (Lớp L) có 8 electron.
C. Lớp thứ ba (Lớp M) có 3 electron.
D. Lớp ngoài cùng có 1 electron.
A. 11.
B. 23.
C. 12.
D. 15.
A. 2 và 2
B. 2 và 1
C. 3 và 2
D. 2 và 3
Trong phần chuyên đề trên đây chúng ta có thể hiểu biết thêm về Cấu hình electron nguyên tử gồm các khái niệm về sự chuyển động của electron trong nguyên tử, các lớp electron và phân lớp electron.
Như vậy VnDoc đã giới thiệu các bạn tài liệu Lý thuyết Hóa học lớp 10 bài 5: Cấu hình electron nguyên tử. Mời các bạn tham khảo thêm tài liệu: Trắc nghiệm Sinh học 10, Giải bài tập Sinh học lớp 10, Giải Vở BT Sinh Học 10, Giải bài tập Sinh học 10 ngắn nhất, Tài liệu học tập lớp 10.
Để tiện trao đổi, chia sẻ kinh nghiệm về giảng dạy và học tập các môn học lớp 10, VnDoc mời các thầy cô giáo, các bậc phụ huynh và các bạn học sinh truy cập nhóm riêng dành cho lớp 10 sau: Nhóm Tài liệu học tập lớp 10. Rất mong nhận được sự ủng hộ của các thầy cô và các bạn.
